
Wdrożenie eCTD 4.0 stanowi kluczowy krok w kierunku modernizacji zgłoszeń regulacyjnych na całym świecie. Dzięki korzyściom, takim jak ulepszone śledzenie dokumentów i wydajność oparta na Metadanych, nie dziwi, że globalne agencje przyjmują tę zmianę.
Ale gdzie w tym wszystkim jest EMA? W przeciwieństwie do FDA, która określiła jasne fazy wdrożenia, EMA przyjmuje bardziej wyważone podejście, rozpoczynając od programów pilotażowych i ocen technicznych. W tym blogu przedstawiamy plany EMA dotyczące eCTD 4.0, jego potencjalny wpływ na zgłoszenia regulacyjne oraz to, jak Twoja firma może pozostać na czele.
Co ważniejsze, czy EMA już nakazała stosowanie eCTD 4.0? Przyjrzyjmy się temu.
Co to jest eCTD 4.0 i czym różni się od eCTD 3.2.2?
Elektroniczny Wspólny Dokument Techniczny (eCTD) to międzynarodowo akceptowany format dla zgłoszeń regulacyjnych. Standaryzuje sposób, w jaki firmy farmaceutyczne składają wnioski o dopuszczenie leków i zarządzają aktualizacjami cyklu życia na różnych rynkach.
Obecna wersja, eCTD 3.2.2, jest używana od lat. Jednakże, organy regulacyjne, w tym EMA, pracują nad eCTD 4.0, który jest oparty na standardzie Health Level 7 (HL7) Regulated Product Submission (RPS). Ta aktualizacja zwiększa efektywność zgłoszeń i zarządzanie cyklem życia regulacyjnego.
Kluczowe różnice między eCTD 3.2.2 a eCTD 4.0:
- Lepsze zarządzanie cyklem życia: Ulepszone śledzenie wersji dokumentów, ograniczające powielanie.
- Bardziej elastyczna granularność: Umożliwia ponowne wykorzystanie ustrukturyzowanych dokumentów w różnych zgłoszeniach.
- Ulepszona obsługa Metadata: Bardziej ustrukturyzowane Metadata, co ułatwia interakcje regulacyjne.
- Większa interoperacyjność: Zaprojektowane, aby lepiej współpracować z ewoluującymi cyfrowymi systemami regulacyjnymi na całym świecie.
- Chociaż te zmiany oferują liczne korzyści, przejście na eCTD 4.0 wymaga przygotowania, inwestycji i zrozumienia oczekiwań regulacyjnych.
Stanowisko EMA w sprawie przyjęcia eCTD 4.0
Wielkie pytanie, które wszyscy sobie zadają, brzmi: Czy EMA nakazała stosowanie eCTD 4.0? Odpowiedź brzmi: jeszcze nie, ale proces przechodzenia jest w toku.
Obecny status eCTD 4.0 w UE:
- Obecnie eCTD 3.2.2 pozostaje obowiązkowym standardem dla zgłoszeń w UE.
- EMA aktywnie ocenia eCTD 4.0, ale nie wydała jeszcze oficjalnego nakazu jego stosowania.
- Agencja współpracuje z innymi organami regulacyjnymi, takimi jak FDA i japońska PMDA, w celu ujednolicenia globalnych standardów.
- Nie ustalono oficjalnych terminów przejściowych, ale EMA wskazała, że eCTD 4.0 ostatecznie stanie się obowiązkowe.
Podejście EMA: Stopniowe wdrażanie z programem pilotażowym
W przeciwieństwie do USFDA, która przedstawiła plan wdrożenia etapowego, EMA przyjmuje ustrukturyzowane podejście. Agencja uruchomiła Techniczny Program Pilotażowy w celu przetestowania wdrożenia eCTD 4.0 z udziałem interesariuszy branżowych.
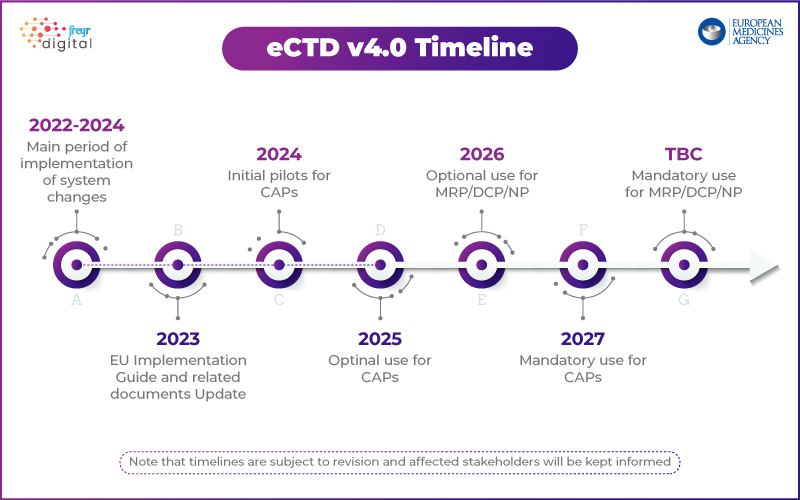
Główne założenia strategii EMA dotyczącej eCTD 4.0:
- Krok 1: Skoncentruj się na interoperacyjności technicznej z narzędziami regulacyjnymi.
- Przyszłe fazy: Zgłoszenia próbne, zarządzanie cyklem życia i zgłoszenia grupowe.
- Dostępny jest projekt pakietu wdrożeniowego zawierający kontrolowane słownictwo i kryteria walidacji.
EMA jest zaangażowana w zapewnienie płynnego przejścia, a firmy z sektora nauk przyrodniczych powinny śledzić aktualizacje na oficjalnej stronie EMA dotyczącej eCTD.
Wyzwania i kwestie do rozważenia dla firm z branży nauk przyrodniczych
Chociaż eCTD 4.0 oferuje wyraźne korzyści, jego wdrożenie wiąże się z wyzwaniami. Poniżej przedstawiono kluczowe kwestie do rozważenia dla firm farmaceutycznych i biotechnologicznych:
- Złożoność regulacyjna
- Stopniowe przejście EMA oznacza, że firmy muszą być przygotowane na podwójne procesy składania dokumentów (eCTD 3.2.2 i eCTD 4.0).
- Różne regiony będą miały różne harmonogramy wdrożeń, co wymaga od firm elastyczności.
- Wyzwania techniczne.
- Migracja danych z eCTD 3.2.2 do 4.0 wymaga starannego planowania.
- Zasady walidacji ulegną znaczącym zmianom, co będzie wymagało zaktualizowanego oprogramowania i narzędzi.
- Firmy muszą inwestować w automatyzację i rozwiązania oparte na sztucznej inteligencji, aby zapewnić zgodność.
- Ryzyka zgodności
- Nieprawidłowe mapowanie metadanych lub niezgodność z nowymi wymaganiami dotyczącymi szczegółowości dokumentów może prowadzić do odrzucenia wniosku.
- Zespoły regulacyjne potrzebują odpowiedniego szkolenia, aby zrozumieć nowe zasady walidacji.
- Wpływ na istniejące procesy pracy
- Firmy będą musiały dostosować wewnętrzne procesy do eCTD 4.0.
- Zwiększona współpraca między zespołami regulacyjnymi, IT i odpowiedzialnymi za zgłoszenia będzie konieczna.
Kluczowy wniosek? Firmy muszą zacząć się przygotowywać już teraz, mimo że EMA nie wprowadziła jeszcze obowiązkowego eCTD 4.0.
Jak firmy mogą przygotować się na przejście EMA na eCTD 4.0
Chociaż EMA nie ustaliła oficjalnego terminu, proaktywne firmy skorzystają na wczesnym przygotowaniu. Oto jak:
- Ocena Obecnych Procesów Zgłoszeniowych
- Zidentyfikować luki w istniejących procesach eCTD 3.2.2.
- Oceń, jak nowe zasady zarządzania cyklem życia produktu wpłyną na bieżące zgłoszenia.
- Zainwestuj w odpowiednie narzędzia eCTD 4.0
- Wybierz oprogramowanie do zgłoszeń regulacyjnych zgodne z eCTD 4.0.
- Zapewnij, że oprogramowanie obsługuje standardy HL7 RPS i automatyzację Metadata.
- Szkolenie zespołów regulacyjnych i IT
- Prowadzenie warsztatów i sesji szkoleniowych dotyczących zmian w eCTD 4.0.
- Dostarczyć wytyczne dotyczące tagowania Metadata i śledzenia cyklu życia.
- Współpracuj z EMA i przedstawicielami branży.
- Uczestnicz w programach pilotażowych i konsultacjach regulacyjnych EMA.
- Bądź na bieżąco z najnowszymi wytycznymi i aktualizacjami regulacyjnymi EMA.
- Przeprowadzanie testów i walidacji
- Przeprowadzaj wewnętrzne zgłoszenia testowe, wykorzystując struktury eCTD 4.0.
- Zidentyfikować potencjalne problemy w granularności dokumentów i mapowaniu Metadata przed ostatecznym mandatem EMA.
Zaczynając już teraz, firmy mogą zapewnić płynne przejście bez zakłóceń w zgłoszeniach regulacyjnych.
Co dalej? Przyszłość eCTD 4.0 w Europie
Chociaż pełny harmonogram przejścia pozostaje niejasny, długoterminowa strategia EMA obejmuje:
- Standaryzacja zgłoszeń na rynkach globalnych, poprawiająca spójność i wydajność.
- Skracanie terminów zatwierdzenia dzięki lepszemu śledzeniu cyklu życia zgłoszeń.
- Integracja AI i automatyzacji w procesach regulacyjnych w celu zwiększenia zgodności.
W ciągu najbliższych kilku lat możemy spodziewać się większej jasności od EMA, w tym oficjalnych harmonogramów przejścia i nowych kryteriów walidacji.
Podsumowanie
Chociaż EMA nie wprowadziła jeszcze obowiązkowego eCTD 4.0, jest tylko kwestią czasu, zanim stanie się ono standardem dla zgłoszeń regulacyjnych w UE. Firmy, które proaktywnie się przygotują, zyskają przewagę konkurencyjną, zapewniając zgodność i unikając przeszkód regulacyjnych w ostatniej chwili.
Kluczowe wnioski
- eCTD 3.2.2 pozostaje obecnym standardem, ale eCTD 4.0 jest już w zasięgu ręki.
- EMA przyjmuje stopniowe podejście, bez oficjalnego nakazu do tej pory.
- Firmy powinny już teraz rozpocząć przygotowania, aby zapewnić płynne przejście.
- Kluczowe będzie inwestowanie w nowe technologie, szkolenie zespołów i testowanie zgłoszeń.
Wezwanie do działania
Bądź na bieżąco z ogłoszeniami regulacyjnymi EMA i zacznij oceniać swoją gotowość na eCTD 4.0. Im wcześniej się przygotujesz, tym łatwiejsze będzie przejście, gdy wejdzie w życie obowiązek.
Czy potrzebujesz pomocy w wyborze oprogramowania zgodnego z eCTD 4.0 lub zrozumieniu, jak ta zmiana wpłynie na Twoją firmę? Zapraszamy do kontaktu z nami.









