
US FDA opublikowała dokument wytycznych, który pomoże branży i personelowi Agencji Zdrowia (HA) określić, kiedy zmiana oprogramowania w wyrobie medycznym wymaga od producenta złożenia i uzyskania zgody FDA na nowe zgłoszenie przed wprowadzeniem do obrotu (510(k)). Wytyczne te mają na celu zwiększenie przewidywalności, spójności i przejrzystości procesu podejmowania decyzji „kiedy złożyć”, poprzez zapewnienie najmniej uciążliwego podejścia oraz opisanie ram regulacyjnych, polityk i praktyk leżących u podstaw takiej decyzji, szczególnie w odniesieniu do zmian oprogramowania. Przyjrzyjmy się szczegółowo wytycznym FDA.
Zasady przewodnie i schemat blokowy FDA
W celu pomocy producentom wyrobów medycznych w stosowaniu głównych zasad, dokument zawiera schemat blokowy, dodatkowe wyjaśnienia i przykłady potrzebne do podjęcia decyzji w sprawie nowego zgłoszenia przed wprowadzeniem do obrotu 510(k) dotyczącego zmiany oprogramowania w już zatwierdzonym wyrobie w US. Dodatkowo, należy przestrzegać kilku zasad przewodnich podczas korzystania z tych wytycznych w celu określenia, czy należy złożyć nowe zgłoszenie 510(k) w celu zmiany istniejącego wyrobu. Niektóre z nich są powszechnie znane i wywodzą się z obecnej polityki FDA 510(k), a inne są niezbędne do zastosowania schematu logicznego wspomnianego w tych wytycznych. Zgodnie z wytycznymi, przedstawiony schemat nie może objąć wszystkich możliwych zawiłości związanych z takimi zmianami i ich wpływem na decyzję. Dlatego, aby określić konieczność nowego zgłoszenia przed wprowadzeniem do obrotu 510(k), producenci wyrobów medycznych powinni wziąć pod uwagę ogólne zasady i schemat blokowy, jak podsumowano poniżej.
- Zmiany wpływające na bezpieczeństwo lub skuteczność wyrobu medycznego
- Wstępna ocena ryzyka
- Nieprzewidziane konsekwencje zmian
- Stosowanie zarządzania ryzykiem
- Rola testowania (czynności weryfikacji i walidacji) w ocenie, czy zmiana mogłaby znacząco wpłynąć na bezpieczeństwo i skuteczność
- Ocena jednoczesnych zmian w celu ustalenia, czy wymagane jest złożenie nowego zgłoszenia 510(k)
- Odpowiednie urządzenie porównawcze i skumulowany efekt zmian
- Wymóg dotyczący dokumentacji (21 CFR Part 820)
- Zgłoszenia 510(k) dla zmodyfikowanych wyrobów
- Ustalenia istotnej równoważności
- Złożenie nowego zgłoszenia 510(k) jest prawdopodobnie wymagane, jeśli producent modyfikuje swoje urządzenie w sposób wpływający na jego bezpieczeństwo lub skuteczność. Jednakże zmiany, które nie mają na celu wpływu na bezpieczeństwo lub skuteczność urządzenia, powinny być nadal oceniane.
- Aby określić, czy zmiana lub modyfikacja mogłaby znacząco wpłynąć na bezpieczeństwo lub skuteczność, producent powinien najpierw przeprowadzić ocenę ryzyka, aby dowiedzieć się, czy zmiana mogłaby wpłynąć na bezpieczeństwo lub skuteczność urządzenia, zarówno pozytywnie, jak i negatywnie. Ta ocena ryzyka powinna zidentyfikować i przeanalizować wszystkie nowe ryzyka oraz zmiany w istniejących ryzykach wynikające ze zmiany urządzenia i prowadzić do wstępnej decyzji, czy wymagane jest złożenie nowego 510(k).
- Czasami podczas zgłaszania oprogramowania mogą wystąpić dodatkowe, niezamierzone lub nieplanowane konsekwencje. Schemat blokowy powinien ocenić te konsekwencje, aby ustalić, czy wymagane jest zgłoszenie nowego 510(k).
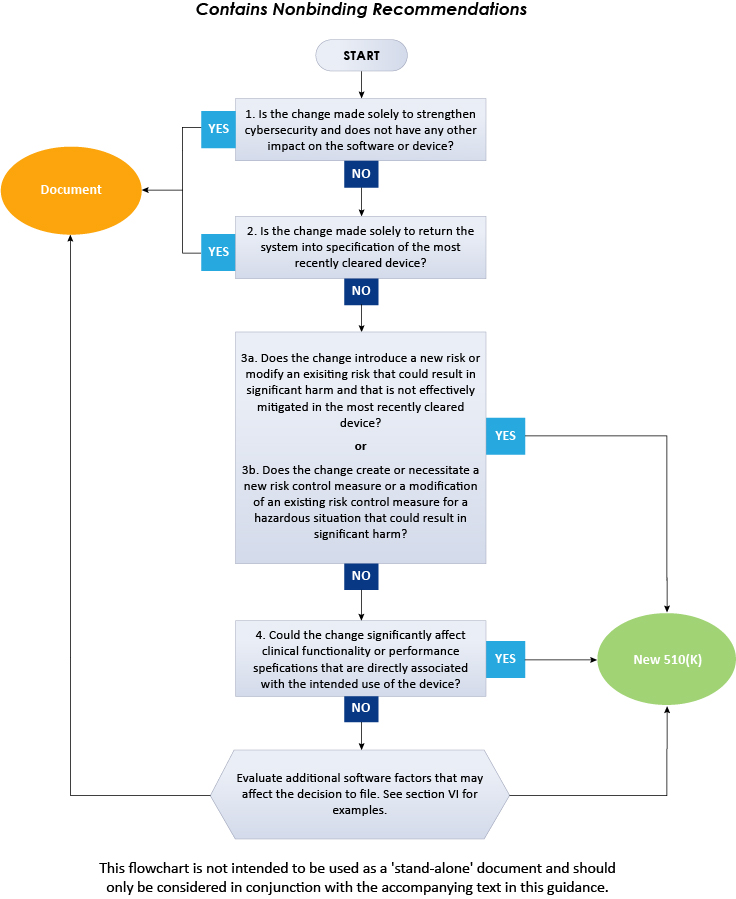
Powyższy schemat blokowy ilustruje procedurę krok po kroku, którą należy zastosować, aby podjąć decyzję o złożeniu wniosku 510(k) w przypadku zmian oprogramowania w istniejących urządzeniach. Podsumowując, obecne wytyczne FDA szczegółowo opisują podejście, jakie powinni przyjąć producenci wyrobów medycznych, decydując, czy zmiany oprogramowania w istniejącym wyrobie medycznym wymagają złożenia nowego wniosku 510(k). Aby uzyskać dalsze informacje na temat wytycznych FDA, skonsultuj się z Freyr - sprawdzonym ekspertem ds. regulacji. Bądź na bieżąco. Zachowaj zgodność.









