
Świat regulacji farmaceutycznych czeka znacząca modernizacja wraz z wdrożeniem eCTD 4.0. Ten ustandaryzowany format obiecuje sprawniejszy proces składania wniosków o nowe leki do organów regulacyjnych. Jednak dla firm, które chcą zdobyć część japońskiego rynku farmaceutycznego o wartości 141,5 miliarda dolarów, jest kluczowy zwrot akcji – Japonia przyspiesza harmonogram wdrożenia!
Poniżej przedstawiono analizę tych kluczowych punktów:
- Obowiązkowe wdrożenie: W przeciwieństwie do innych obszarów, gdzie przed obowiązkowym przyjęciem istnieją fazy dobrowolne, Japonia dąży do tego, aby do 2026 roku korzystanie z eCTD 4.0 stało się obowiązkowe.
- Kluczowe jest przygotowanie: Przygotowanie jest kluczowe ze względu na ograniczenia czasowe i brak bezpośredniej ścieżki migracji z japońskiego formatu PMDA JP1.0 do eCTD 4.0; skupienie się na lepszym systemie pomoże japońskim firmom farmaceutycznym w procesie przejściowym. Kroki te obejmują aktualizację oprogramowania, szkolenie personelu i przygotowanie plików PDF do nowego formatu.
- Dostępne zasoby: Japońska Agencja ds. Produktów Farmaceutycznych i Wyrobów Medycznych (PMDA) opublikowała zasoby, które mogą pomóc firmom w przejściu przez tę zmianę, takie jak “ICH Electronic Common Technical Document eCTD 4.0 Implementation Guide”, zawierające wyjaśnienia dotyczące wprowadzonych zmian i dostępne najlepsze praktyki.
Oto kilka powodów, dla których nie powinieneś przegapić tej gry z liczbami:
- Szybka ścieżka do eCTD 4.0: W przeciwieństwie do innych regionów, gdzie proces jest etapowy, Japonia dąży do obowiązkowego przyjęcia eCTD 4.0 już w 2026 roku. To trzy lata przed terminem wyznaczonym przez US FDA na 2029 rok! Tak agresywny harmonogram oznacza, że Japonia objęła prowadzenie w zakresie globalnego wdrażania eCTD.
- Brak miejsca na błędy: JP nie mogło być bezpośrednio konwertowane do eCTD 4.0, w przeciwieństwie do poprzednich wersji. Oznacza to, że firmy farmaceutyczne muszą być na to szczególnie przygotowane, aby zapobiec opóźnieniom w składaniu wniosków, które mogą kosztować je miliony przychodów.
- Wsparcie dla płynnego wejścia na rynek: Japońska Agencja ds. Produktów Farmaceutycznych i Wyrobów Medycznych (PMDA) rozumie wyzwania. Opracowała zasoby, takie jak przewodniki wdrożeniowe, mające na celu łatwe przeprowadzenie firm przez te zmiany i zapewnienie im sukcesu na japońskim rynku. (https://www.pmda.go.jp/english/).
Jeśli opracowujesz leki na ogromny rynek japoński, czas się przygotować! Oto Twoja lista kontrolna przed startem:
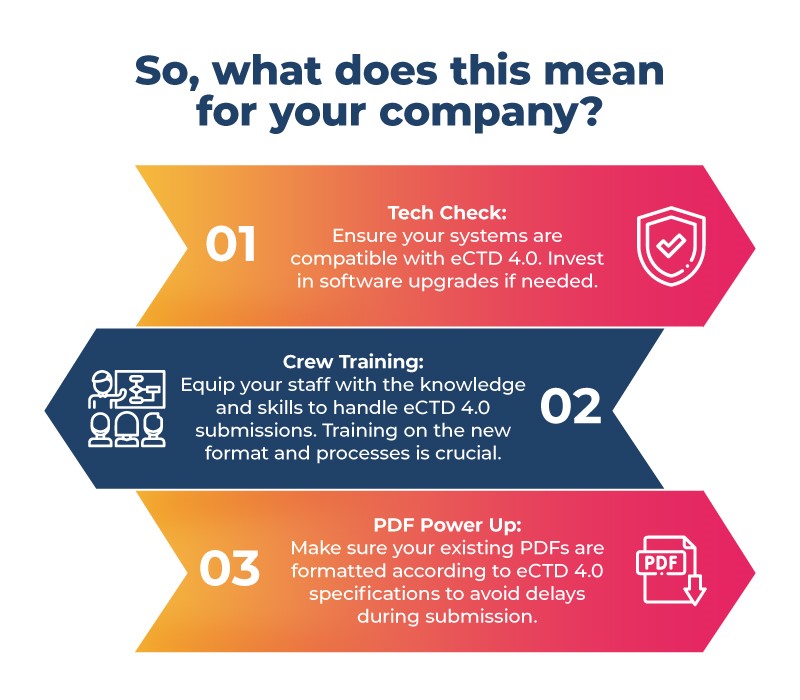
Przejście na eCTD 4.0 obiecuje zwiększoną wydajność i globalną standaryzację w całym procesie zatwierdzania leków farmaceutycznych. Twoja firma może przewidzieć ten krok w Japonii, aby zapewnić płynne przejście i skorzystać z niezliczonych możliwości oferowanych przez tę nową erę. Pamiętaj, że brak przygotowania to przygotowanie do porażki – bądź więc gotowy na sukces z eCTD 4.0 w Japonii.
Uzyskane korzyści i możliwości są atrakcyjne dla przemysłu farmaceutycznego. Jednakże wiąże się to z pewnymi trudnościami, które należy rozwiązać. Aby sprawnie poruszać się w ciągle zmieniającym się środowisku regulacyjnym, firmy mogą szukać partnerstwa z wiarygodnymi konsultantami, takimi jak Freyr. Odkryj przyszłość zgłoszeń regulacyjnych w Japonii dzięki naszemu niezrównanemu oprogramowaniu eCTD, Freyr SUBMIT PRO, które jest zgodne ze standardami 21 CFR Part 11 i posiada elastyczny model wdrożenia. Skontaktuj się z nami już dziś, aby dowiedzieć się więcej i wyruszyć w podróż ku zwiększonej wydajności i sukcesowi. Poproś o demo już dziś.









