
Skuteczna komunikacja zawsze zapewniała bezpieczeństwo i jakość opieki nad pacjentami. Przez lata nadal istnieje niezaspokojona potrzeba dostarczania tłumaczeń etykiet osobom, które nie posługują się biegle językiem angielskim. Zapotrzebowanie na etykiety produktów w wielu językach regionalnych wzrosło wykładniczo, ponieważ producenci farmaceutyczni dążą do zmian w kierunku lokalizacji i lepszej komunikacji.
Spełnienie tych wymagań zwiększy bezpieczeństwo pacjentów, jednocześnie umożliwiając zgodność z krajowymi wymogami regulacyjnymi. Brak ważnych informacji medycznych w dokumentacji regionalnej stanowi dodatkowe obciążenie dla farmaceutów i pracowników służby zdrowia, którzy muszą pokonać barierę językową.
Urząd Regulacji Produktów Zdrowotnych (HPRA) nadzoruje zgodność regulacyjną w Irlandii. HPRA ułatwia i współpracuje z interesariuszami, przestrzegając wytycznych dotyczących najlepszych praktyk w zakresie wielojęzycznego etykietowania, wydanych przez Grupę Koordynacyjną ds. Procedur Wzajemnego Uznawania i Zdecentralizowanych – Ludzkich (CMDh). Ponadto HPRA złagodziła również niektóre warunki etykietowania, które obejmują:
- Użycie mL w Irlandii (IE) w porównaniu do ml w innych państwach UE.
- Stosowanie separatorów dziesiętnych w objętości lub mocy produktu oraz kropka w IE w porównaniu do przecinka w UE. Producenci leków mogą przezwyciężyć tę rozbieżność, grupując nazwę własną, moc i postać leku jako jedną jednostkę w każdym języku.
- Stosowanie separatora w mocy lub objętości produktu – kropka w UE w porównaniu do przecinka w IE. Użycie przecinków jako separatora jest dozwolone na bezpośrednim opakowaniu zewnętrznym, aby uniknąć ryzyka pomyłek wśród irlandzkich pacjentów.
- Małe opakowania bezpośrednie, tj. pojemniki o pojemności mniejszej lub równej 50 ml, mają ograniczone miejsce i mogą pomieścić minimalne wymagane informacje, jeśli jest to uzasadnione, w więcej niż dwóch (02) językach.
- Informacje dotyczące krajów trzecich – tam, gdzie warunki informacji o produkcie są podobne w Wielkiej Brytanii i Irlandii, opakowania wielokrajowe są akceptowalne. Dodatkowe wymagania specyficzne dla danego kraju umieszczane są w „niebieskiej ramce”.
- Koordynacja oceny z innymi Member States – Oceny makiet etykiet przeprowadzane przez Member States zapewniają zgodność oznakowania. Wnioskodawcy mogą koordynować działania z Member States, aby uzyskać jasność co do wymaganych zmian przed złożeniem wniosków do HPRA.
- Wspólne nazwy - Podkreślenie proponowanej nazwy wymyślonej dla Member States musi zostać zgłoszone do HPRA.
HPRA przedstawia dodatkowe sugestie dotyczące etykietowania wielojęzycznego w następujący sposób:
- Informacje podane w języku angielskim muszą być zgrupowane w bloku.
- Należy podać wymagania „niebieskiej skrzynki” dla wszystkich krajów na tym samym panelu, jeśli kilka krajów współdzieli jedno opakowanie.
- Informacje skierowane do irlandzkich pacjentów muszą być wyraźnie podane w kodzie owalnym.
- Wnioskodawcy mogą umieścić perforowaną sekcję na opakowaniu, pod warunkiem, że usuwalne dane nie są w języku angielskim. Musi to być wspomniane w zgłoszeniu.
- Wnioskodawcy muszą przesłać plik PDF ulotki dołączonej do opakowania do HPRA na koniec procesu w celu jej aktualizacji na stronie internetowej.
Kryteria dla opakowania wielojęzycznego:
- Nazwa produktu i jego moc muszą być takie same we wszystkich językach.
- Informacje zawarte w oznakowaniu i ulotce dołączonej do opakowania muszą być zgodne z Charakterystyką Produktu Leczniczego (SmPC).
- Informacje wydrukowane na etykietach i ulotce dołączonej do opakowania muszą być dokładne i czytelne.
- Status prawny leku musi być podobny w obu krajach.
Przykład wielojęzycznego opakowania:
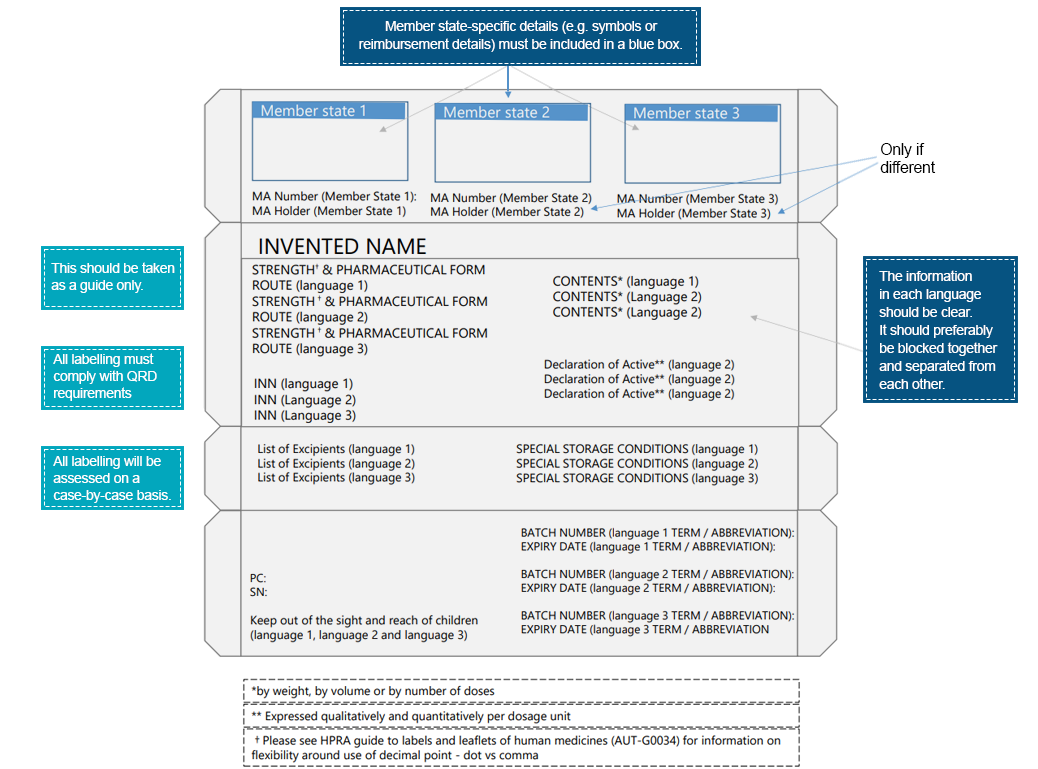
Pacjenci mają kontakt z etykietami leków na długo przed kontaktem z samym produktem leczniczym. Takie interakcje dodatkowo podkreślają znaczenie przekazywania kluczowych informacji za pośrednictwem różnych elementów etykiety leku. Aby zapewnić lepszą czytelność i udoskonalenie elementów etykiet, firmy farmaceutyczne muszą podjąć niezbędne działania. Języki regionalne stanowią środek do przekazywania instrukcji medycznych dotyczących produktu leczniczego, co gwarantuje bezpieczne i skuteczne stosowanie przepisanego produktu. Eksperci regulacyjni z poszczególnych krajów mogą pomóc w tłumaczeniu informacji na etykietach zgodnie z lokalnymi/regionalnymi przepisami. Eksperci Freyr są doskonale przygotowani, aby pomóc w wypełnianiu luk między informacjami medycznymi a językiem. Skontaktuj się z nami, aby uzyskać zgodną z przepisami ścieżkę etykietowania.










