
Opracowywanie i zatwierdzanie leków dla dzieci jest krytycznym aspektem pediatrycznej opieki zdrowotnej. Jednak ze względu na względy etyczne i praktyczne, badania kliniczne z udziałem dzieci są często ograniczone. W rezultacie, etykietowanie leków pediatrycznych odgrywa kluczową rolę w zapewnieniu bezpiecznego i właściwego stosowania leków w tej wrażliwej populacji. W tym blogu porównamy wymagania dotyczące etykietowania leków pediatrycznych w Unii Europejskiej (UE) i w US, aby lepiej zrozumieć podobieństwa i różnice między tymi dwoma (02) ramami regulacyjnymi.
Wymogi dotyczące etykietowania produktów pediatrycznych w UE
UE ma specyficzne wymagania dotyczące etykietowania Produktów leczniczych przeznaczonych dla dzieci. Wymagania te zapewniają, że leki przeznaczone dla dzieci są odpowiednio testowane, autoryzowane i oznakowane, aby zapewnić bezpieczne i skuteczne opcje leczenia dla pacjentów pediatrycznych.
Zapewnij bezpieczeństwo leków pediatrycznych. Skontaktuj się z nami
Zapewnienie bezpieczeństwa leków pediatrycznych już teraz
Oto niektóre aspekty wymogów dotyczących etykietowania produktów pediatrycznych w UE:
- Plany Badań Pediatrycznych (PIP): Plan Badań Pediatrycznych (PIP) musi zostać złożony do Europejskiej Agencji Leków (EMA) zanim lek zostanie zatwierdzony do stosowania u dzieci. Określa on badania i dane wymagane do oceny bezpieczeństwa, skuteczności i dawkowania leku w populacjach pediatrycznych.
- Pozwolenie na dopuszczenie do obrotu produktu leczniczego do stosowania u dzieci (PUMA): Jeśli lek został przebadany u dzieci i spełnia wymagania, może otrzymać PUMA. To pozwolenie umożliwia wprowadzanie leku na rynek do stosowania u dzieci.
- Formulacje odpowiednie dla wieku: Leki do stosowania u dzieci powinny być dostępne w formulacjach odpowiednich dla różnych grup wiekowych, takich jak płyny, tabletki do żucia lub urządzenia dozujące odpowiednie dla wieku.
- Specyficzne dla pediatrii streszczenie właściwości produktu (SmPC): SmPC to dokument zawierający szczegółowe informacje o leku. W przypadku produktów pediatrycznych powinien zawierać szczegółowe informacje dotyczące dawkowania, podawania i kwestii bezpieczeństwa dla różnych grup wiekowych.
- Ostrzeżenia i środki ostrożności dotyczące stosowania u dzieci: Oznakowanie powinno zawierać wszelkie specyficzne ostrzeżenia lub środki ostrożności związane ze stosowaniem leku u dzieci, takie jak potencjalne działania niepożądane lub interakcje z innymi lekami powszechnie stosowanymi u pacjentów pediatrycznych.
- Ciągłe monitorowanie i aktualizacje: Po zatwierdzeniu leku do stosowania u dzieci, mogą być wymagane badania poautoryzacyjne w celu zebrania dodatkowych danych dotyczących jego bezpieczeństwa i skuteczności. Może to prowadzić do niezbędnych aktualizacji w etykietowaniu.
Wymagania dotyczące etykietowania pediatrycznego w US
W US Food and Drug Administration (FDA) wdrożyła ustawę Pediatric Research Equity Act (PREA) oraz ustawę Best Pharmaceuticals for Children Act (BPCA) w celu promowania badań i etykietowania leków pediatrycznych. PREA wymaga od firm farmaceutycznych przeprowadzania badań pediatrycznych dla niektórych leków, które prawdopodobnie będą stosowane u dzieci. BPCA przyznaje dodatkowe sześć (06) miesięcy wyłączności rynkowej firmom przeprowadzającym te badania.
FDA egzekwuje dalsze wytyczne w celu zapewnienia bezpieczeństwa, skuteczności i właściwego dawkowania leków pediatrycznych w następujący sposób:
- Plany badań pediatrycznych (PSPs): Producenci muszą przedstawić plany określające badania pediatryczne w celu oceny bezpieczeństwa i skuteczności leków.
- Informacje specyficzne dla wieku: Etykiety powinny zawierać dawkowanie specyficzne dla wieku, wskazania i kwestie bezpieczeństwa.
- Dawkowanie oparte na masie ciała: Zalecenia dotyczące dawkowania zależnego od masy ciała zapewniają dokładne podawanie.
- Działania niepożądane: Dostarczyć dane dotyczące działań niepożądanych specyficznych dla pediatrii oraz dane dotyczące bezpieczeństwa.
- Formulacje specyficzne dla pediatrii: Leki mogą wymagać form dawkowania dostosowanych do dzieci (np. płyny i tabletki do żucia).
- Inżynieria czynnika ludzkiego: Etykiety powinny uwzględniać łatwość podawania przez opiekunów.
- Ulotki informacyjne dla pacjenta: Wymagane są jasne instrukcje dotyczące podawania, dawkowania i działań niepożądanych.
Poniższa tabela przedstawia różnice i podobieństwa między wymaganiami dotyczącymi etykietowania w US i UE:
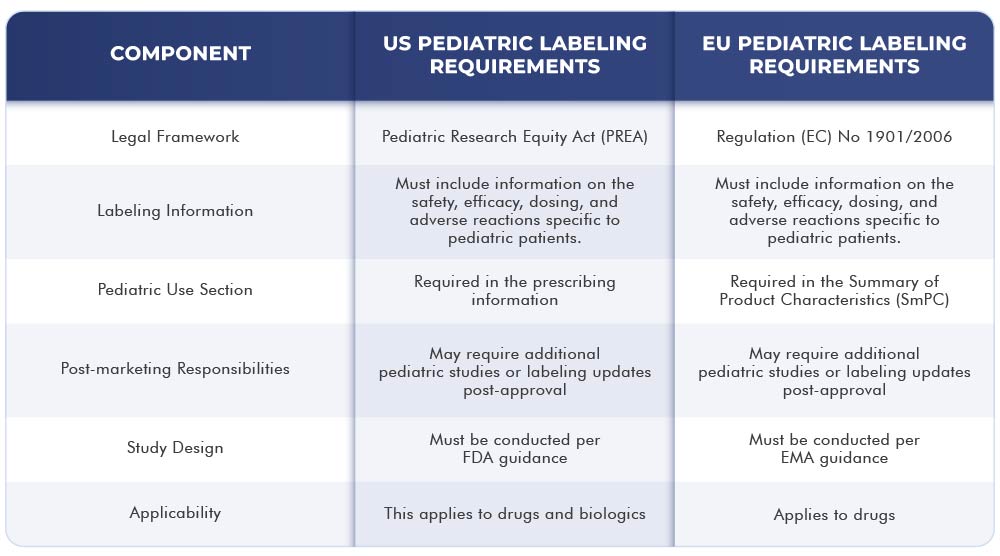
Podsumowanie
Wymogi dotyczące etykietowania leków pediatrycznych w UE i US mają na celu zapewnienie bezpiecznego i właściwego stosowania leków u dzieci. Chociaż istnieją podobieństwa między dwoma ramami regulacyjnymi, takie jak potrzeba badań pediatrycznych i włączenie informacji specyficznych dla dzieci do etykietowania leków, istnieją również znaczące różnice. Zrozumienie tych podobieństw i różnic jest kluczowe dla firm farmaceutycznych, dostawców opieki zdrowotnej i organów regulacyjnych, aby zapewnić dzieciom dostęp do bezpiecznych i skutecznych leków.
Skonsultuj się ze sprawdzonym ekspertem w dziedzinie etykietowania, takim jak Freyr, aby zapewnić zgodność z wymogami etykietowania specyficznymi dla danego kraju.










