
Etykiety leków stanowią podstawowy przewodnik dla użytkowników i pomagają w prawidłowym stosowaniu produktów. Dlatego niezwykle ważne jest, aby informacje dostępne na etykietach były spójne, łatwe do odczytania, wolne od błędów i zgodne z globalnymi standardami. Aby to osiągnąć, Therapeutic Goods Administration (TGA) wprowadziła kilka zmian w sposobie prezentowania informacji na etykietach produktów. Celem wprowadzenia tych zmian jest poprawa przejrzystości i spójności informacji dostarczanych pracownikom służby zdrowia.
Jakie są nowe zmiany w oznakowaniu?
Chociaż nowe informacje są już brane pod uwagę i wdrażane przez producentów, warto je szczegółowo poznać dla kompleksowej prezentacji. Poniżej przedstawiono kilka z nich, nad którymi producenci muszą pracować, definiując etykiety swoich leków.
1. Informacje o Składniku Aktywnym
Zgodnie z nową zasadą, składniki aktywne powinny być:
- Umieszczone bardziej widocznie na przedniej stronie opakowania leku
- Powinien być umieszczony poniżej lub obok nazwy leku na przedniej stronie opakowania leku
- Musi być łatwo porównywalne między lekami
2. Informacje o lekach
Aby użytkownicy i pracownicy służby zdrowia mogli podejmować świadome decyzje, informacje o leku powinny być jaśniejsze pod względem:
- Kluczowe informacje zdrowotne na wyróżniających się etykietach
- Wszystkie obowiązkowe informacje muszą być przedstawione w sposób bardziej przejrzysty i rozpoznawalny na tle koloru tła, aby poprawić ich czytelność.
- Substancje podlegające deklaracji, takie jak alergeny, muszą być wymienione na etykiecie
3. Krytyczne informacje zdrowotne
Kluczowe informacje zdrowotne pomagają konsumentom bezpiecznie używać leku, dostarczając ważnych danych. Informacje zawarte w tabeli kluczowych informacji zdrowotnych zawsze będą w tej samej kolejności, chociaż może występować niewielka różnica w sposobie ich przedstawienia. Kluczowe informacje zdrowotne zawierają następujące nagłówki i dane w tej samej kolejności:
- Składniki Aktywne: Nazwa składnika aktywnego i jego ilość
- Wskazania: Stosowanie leku
- Ostrzeżenia: Zawiera oświadczenia ostrzegawcze, zalecenia i dodatkowe ostrzeżenia dotyczące stosowania leku w sekcji „Sposób użycia”.
- Instrukcja użycia: Zawiera informacje dotyczące bezpiecznego stosowania leku.
- Inne informacje: Obejmują szczegóły dotyczące przechowywania, zabezpieczenia przed otwarciem, dane kontaktowe sponsora, listę składników itp. Ta część może nie występować na każdym leku.
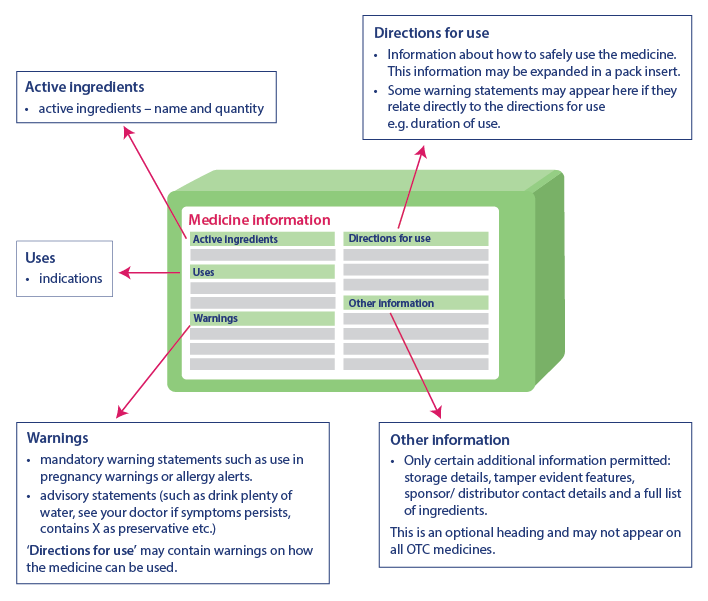
Źródło: TGA
4. Wydawanie leków w aptece
Zgodnie z nową zasadą, wprowadza się następujące zmiany w dozownikach leków:
- Aby poprawić identyfikację leków, opakowania leków na receptę muszą zawierać ich nazwę na trzech nieprzylegających stronach.
- Etykiety leków na receptę muszą mieć wydzielone miejsce o wymiarach 70x30 milimetrów, chyba że są dostarczane w opakowaniu pierwotnym lub zestawie startowym.
5. Informacje o alergenach
Na etykietach leków muszą być podane następujące informacje:
- Jeśli obecne w leku, wszystkie substancje muszą być zadeklarowane na etykiecie.
- Dodatkowe substancje, takie jak skorupiaki, ryby, jaja, soja, mleko i orzechy drzewne, muszą być zadeklarowane na etykiecie
- W przypadku nowych alergenów, producenci mogą ich nie uwzględniać do końca 4-letniego okresu przejściowego.
Chociaż TGA opublikowała te informacje dla pracowników służby zdrowia, uważamy to za kluczowy wymóg również dla producentów, aby kompleksowo etykietowali swoje produkty. Dzięki temu pracownicy służby zdrowia mogą zapoznać się ze zaktualizowanymi informacjami bez żadnych niejasności i doradzać pacjentom w kwestii bezpiecznego spożycia. Powszechnie wiadomo, że TGA zapewniła producentom czteroletni okres przejściowy na wdrożenie tych zmian. Po upływie określonej daty, etykiety leków muszą być zgodne z nowymi wymogami dotyczącymi etykietowania. Bądź na bieżąco. Zachowaj zgodność.










