
Las tareas de presentación y publicación reglamentarias han sido tradicionalmente laboriosas, implicando horas de esfuerzo manual para formatear documentos, generar PDF conformes a la agencia, realizar controles de calidad, ensamblar documentos para las presentaciones, etc. Con los plazos exigentes, las empresas de ciencias de la vida siempre se apresuran para realizar presentaciones a tiempo. En todo el mundo, los organismos reglamentarios se están preparando para adoptar los desarrollos recientes como eCTD v4.0 para la presentación de expedientes, enmiendas y otros informes. eCTD v4.0 es un cambio incremental que probablemente impactará el futuro de las presentaciones reglamentarias, con cada país preparándose para aceptarlo e implementarlo.
Considerando todos los desafíos en torno a las presentaciones normativas, la necesidad actual es una solución tecnológicamente avanzada para impulsar el proceso de presentación y revisión de medicamentos. Dado que las organizaciones ya están considerando la automatización para que sea una parte integral del proceso de presentación normativa, es crucial considerar cómo puede mejorar la productividad durante la transición a eCTD 4.0.
¿Cómo ayuda la automatización en la transición a eCTD 4.0?
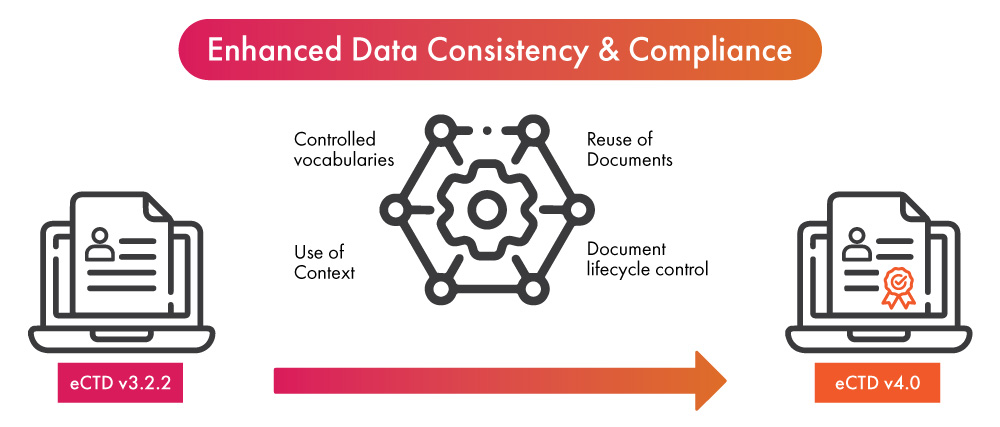
- En el umbral de la adopción de la última versión del eCTD, la implementación de la automatización en el proceso de presentación reglamentaria puede aportar dobles beneficios a las empresas de ciencias de la vida, que incluyen asegurar el cumplimiento del eCTD v4.0 en un tiempo más rápido por un lado (01) y mejorar la coherencia de los datos y la optimización del proceso de presentación por otro lado.
- Una vez que los datos han sido finalizados para su uso en una (01) presentación reglamentaria, la automatización permite que los datos se rellenen en otras presentaciones o actualizaciones. Aprovecha la nueva característica del eCTD v4.0, que ahora permite reemplazos de datos de muchos a uno y de muchos a muchos, lo que permite la reutilización de los datos de forma simplificada.
- Las notificaciones automáticas eliminan la necesidad de enviar mensajes o hacer llamadas telefónicas cuando se requiere una actividad. Esto permite una comunicación más rápida y clara, lo que lleva a vocabularios controlados, un componente esencial de eCTD v4.0.
- La automatización en la presentación de documentos ayudará a facilitar aún más el proceso de actualización de contenido ya presentado. Mejorará el control del ciclo de vida de los documentos presentados.
- La automatización en grupos de contexto puede acelerar el proceso de organizar múltiples archivos destinados a ser utilizados para presentaciones reglamentarias.
En medio de la transición a eCTD v4.0, es crucial que las organizaciones de ciencias de la vida se asocien con proveedores que estén preparados para el nuevo estándar y comprendan cómo automatizar y optimizar el proceso de publicación reglamentaria. Las empresas deben prepararse para adoptar las últimas tecnologías habilitadas por la automatización para obtener beneficios destacados y una ventaja competitiva en el mercado. eCTD v4.0 es un cambio importante que ha llegado después de mucho tiempo. Las organizaciones deben comenzar su prueba de concepto para tantear el terreno, ya que pronto será aceptado en muchos países de todo el mundo, dependiendo de los plazos de cada país.
En Freyr estamos a la vanguardia impulsando la innovación a través de la tecnología y estamos preparados para apoyar a nuestros clientes haciendo que nuestro software de presentación y publicación reglamentaria - Freyr SUBMIT PRO esté listo para eCTD v4.0.
Para saber más sobre la preparación de Freyr para eCTD 4.0, por favor, haga clic aquí para descargar la sesión archivada del seminario web.









