
Los Asuntos Regulatorios (RA) desempeñan un papel fundamental para garantizar la seguridad, eficacia y calidad de los productos farmacéuticos en el dinámico panorama de la industria. Los Asuntos Regulatorios (RA) de Química, Fabricación y Controles (CMC) son esenciales para el cumplimiento normativo. Su objetivo es proteger la salud del paciente y fomentar la confianza pública en los productos farmacéuticos, asegurando la coherencia y la calidad en todo el proceso de fabricación del medicamento.
CMC RA abarca los requisitos de documentación y cumplimiento relacionados con la fabricación, el control de calidad y la estabilidad de los productos farmacéuticos. Implica atención al detalle y el cumplimiento de las directrices normativas a lo largo de todo el ciclo de vida del desarrollo del fármaco. Para saber más sobre la importancia de CMC RA, consulte con nuestros expertos.
En este blog, profundizaremos en los fundamentos de CMC RA y exploraremos su importancia para lograr el cumplimiento y mantener altos estándares de calidad.
El papel de CMC en el desarrollo de medicamentos
Las consideraciones de CMC comienzan temprano en el proceso de desarrollo de fármacos y continúan a lo largo de todas las etapas, desde la investigación preclínica hasta la comercialización. Los datos y la documentación de CMC son componentes críticos de las presentaciones normativas, como las solicitudes de Investigational New Drug (IND), las New Drug Applications (NDA) y las Solicitudes de Autorización de Comercialización (MAA). Las autoridades normativas revisan los datos de CMC para evaluar la seguridad, identidad, potencia y calidad de un producto farmacéutico, así como la fiabilidad y consistencia del proceso de fabricación.
Garantizar el cumplimiento con CMC RA
El cumplimiento de los requisitos reglamentarios de CMC es fundamental para una entrada exitosa en el mercado. Las autoridades reglamentarias, como la Administración de Alimentos y Medicamentos de los Estados Unidos (USFDA), la Agencia Europea de Medicamentos (EMA) y otras Autoridades Sanitarias (HA) regionales, son responsables de establecer directrices y estándares que deben seguirse. Estas directrices cubren varios aspectos, incluyendo las prácticas de fabricación, los sistemas de calidad, los métodos analíticos, las pruebas de estabilidad y la validación. El cumplimiento implica una documentación meticulosa, la adhesión a las Buenas Prácticas de Fabricación (GMP) y la implementación de Sistemas de Gestión de Calidad (QMS) eficaces.
Función del cumplimiento CMC en el éxito de una empresa farmacéutica
Mantener altos estándares de cumplimiento CMC ofrece varias ventajas a las empresas farmacéuticas. Algunos de los beneficios clave son:
- Mitigar los riesgos reglamentarios.
- Apoyando las aprobaciones reglamentarias exitosas.
- Reducir la probabilidad de retiradas de productos.
- Fomentar una reputación positiva de calidad y fiabilidad.
Aspectos a considerar para una función exitosa de RA CMC:
- Mantenerse al día con el conocimiento reglamentario: Los requisitos reglamentarios en evolución de las Autoridades Sanitarias exigen mantenerse al día con las últimas directrices. El monitoreo continuo de las actualizaciones reglamentarias y su incorporación en las prácticas de CMC es crucial para mantener el cumplimiento.
- Establecimiento de Sistemas de Calidad: Esto incluye el desarrollo y mantenimiento de Procedimientos Operativos Estándar (SOPs) completos, procedimientos de control de documentos, procesos de control de cambios y programas de capacitación para asegurar que los empleados comprendan y sigan los protocolos establecidos.
- Evaluación y mitigación de riesgos: Las empresas deben identificar los riesgos potenciales a lo largo de los procesos de desarrollo y fabricación de medicamentos e implementar estrategias adecuadas de mitigación de riesgos. Esto incluye evaluar los parámetros críticos del proceso, la variabilidad de las materias primas, las posibles impurezas y los riesgos de la cadena de suministro, lo que garantiza el cumplimiento.
- Documentación e integridad de los datos: Mantener una documentación precisa y completa es esencial para demostrar el cumplimiento. Las empresas deben establecer prácticas de documentación robustas, incluyendo el mantenimiento de registros de lotes, datos analíticos, estudios de estabilidad e informes de validación. Asegurar la integridad, trazabilidad y seguridad de los datos es fundamental para evitar problemas de cumplimiento.
- Gestión eficaz de cambios: Las empresas deben contar con procedimientos de control de cambios bien definidos para evaluar y documentar los cambios, valorar su impacto en la calidad del producto y el cumplimiento reglamentario, y buscar las aprobaciones necesarias antes de implementar los cambios.
- Asociaciones y gestión sólidas con proveedores: Esto implica seleccionar proveedores cualificados, realizar auditorías y establecer acuerdos de calidad que describan las responsabilidades y expectativas. Realizar evaluaciones periódicas del cumplimiento de los proveedores con los requisitos de las Buenas Prácticas de Fabricación actuales (cGMP) es esencial.
- Preparación para auditorías e inspecciones: Las empresas deben realizar autoevaluaciones para identificar áreas de mejora y asegurar la preparación para auditorías reglamentarias. De hecho, abordar los hallazgos de la auditoría con prontitud e implementar acciones correctivas son clave para mantener el cumplimiento.
- Mejora Continua: Esto se puede lograr fomentando la participación de los empleados, proporcionando formación y educación sobre los requisitos reglamentarios y promoviendo una mentalidad orientada a la calidad en todos los niveles de la organización.
- Abordar las Acciones Correctivas y Preventivas (CAPA): Al abordar sistemáticamente el incumplimiento utilizando la metodología CAPA, las empresas farmacéuticas pueden demostrar su compromiso con la mejora continua y el cumplimiento.
- Conocimiento de los Cambios Reglamentarios Post-aprobación: Comprender los requisitos reglamentarios para los cambios post-aprobación es esencial para garantizar el cumplimiento. Implementar procesos adecuados de gestión de cambios y comunicarse eficazmente con las HAs puede ayudar a gestionar estos cambios garantizando el cumplimiento.
Función de un proveedor reglamentario en el proceso de cumplimiento CMC
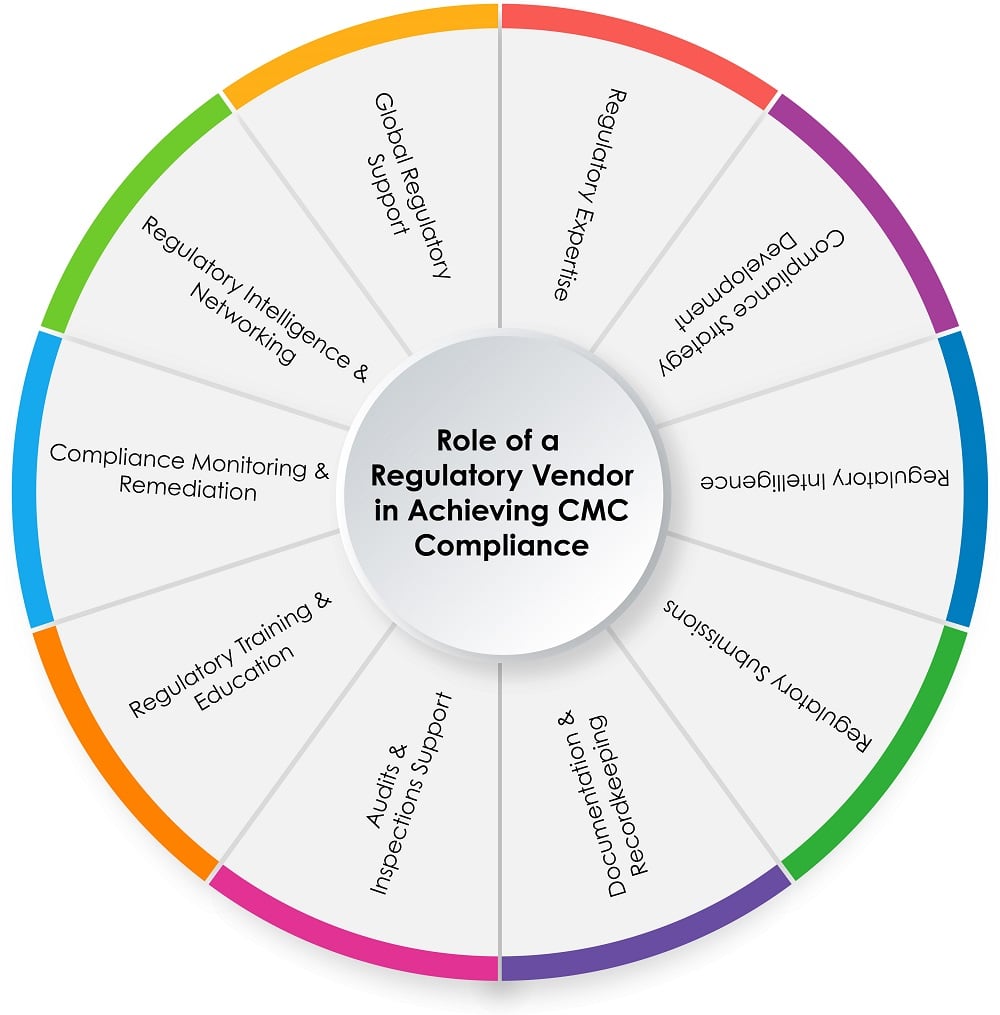
El gráfico circular a continuación (Figura 1) muestra el papel de un proveedor reglamentario en el proceso de cumplimiento de CMC:
Figura 1: Función de un proveedor reglamentario para lograr el cumplimiento de CMC
Conclusión
Lograr y mantener el cumplimiento de los requisitos de CMC exige un enfoque estratégico, que implica colaboración interfuncional, sistemas de calidad sólidos e inteligencia reglamentaria (RI) continua. También es esencial para un acceso exitoso al mercado y la disponibilidad continua del producto. Una comprensión profunda de los fundamentos de la RA de CMC y la implementación de estrategias de cumplimiento efectivas pueden ayudar a las empresas farmacéuticas a navegar por el panorama reglamentario, obtener aprobaciones y mantener los más altos estándares de calidad y seguridad del paciente. Las asociaciones reglamentarias estratégicas pueden sinergizar estos pasos cruciales ofreciendo experiencia de primera clase para mantener el cumplimiento. Contáctenos para obtener más información sobre nuestros servicios.









