
Además de completar las presentaciones de datos xEVMPD requeridas, las organizaciones de ciencias de la vida ahora deberán utilizar un formulario de solicitud basado en la web llamado Digital Application Dataset Integration (DADI). La Agencia Europea de Medicamentos (EMA) diseñó DADI como un reemplazo a largo plazo para el formulario de solicitud electrónico (eAF) basado en PDF, que se creó para respaldar las presentaciones eCTD.
La EMA ha publicado recientemente los plazos para esta transición. DADI reemplazará el formulario para las variaciones de productos medicinales en el año 2022. Otros formularios de envío para Productos Autorizados Centralmente (CAP) y Productos Autorizados Nacionalmente (NAP) le seguirán pronto en 2023. El proyecto también reemplazará los formularios utilizados para los procedimientos clave de la UE, incluyendo el Procedimiento Centralizado (CP), el Procedimiento de Reconocimiento Mutuo (MRP), el Procedimiento Descentralizado (DCP) y el Procedimiento Nacional (NP).
Los formularios web (incluido el Formulario de Variaciones Humanas (HVF) para productos medicinales destinados a humanos) uniformarán las entradas para los eAFs, proporcionando datos maestros de productos estándar para medicamentos. Permitirán tanto la salida existente legible por humanos como la nueva salida legible por máquinas para el procesamiento digital, basándose en el estándar de intercambio de datos Fast Healthcare Interoperability Resources (FHIR) para productos medicinales. También utilizarán los datos maestros de productos existentes de los Servicios de Gestión de Productos (PMS) para rellenar previamente los campos del formulario siempre que sea aplicable.
Los formularios web DADI están destinados a permitir un procesamiento más metódico de una solicitud, reduciendo así la carga de trabajo de la organización. Por ejemplo, se reducirán los errores y las discrepancias gracias a que los formularios facilitan el escrutinio de las solicitudes presentadas por las Autoridades Sanitarias. Los formularios también allanarán el camino para que los datos “correctos a la primera” se introduzcan en las bases de datos, haciendo así que la integración de sistemas y el intercambio de datos entre las Autoridades Sanitarias sea más sencillo. Además, los nuevos formularios reemplazarán la tecnología arcaica.
Beneficios de DADI
El objetivo de DADI y esta transformación de los procesos regulatorios impulsada por datos se puede resumir de la siguiente manera:
- Para mejorar la eficiencia en todas las funciones reglamentarias, de I+D y de fabricación.
- Para comunicarse con las Autoridades Sanitarias de una manera más rápida.
- Para permitir la toma de decisiones basada en datos tanto para las empresas como para las autoridades.
- Para tener una mejor comprensión y previsión de los resultados del negocio y el rendimiento general
De manera integral, esto busca ser beneficioso para los pacientes, los organismos reguladores y la industria.
Últimos cambios en los plazos por la EMA
- La fecha de entrada en vigor para los HVF se ha pospuesto a octubre de 2022 desde la fecha límite previamente establecida de abril de 2022.
- Actualmente, el HVF está siendo sometido a pruebas de aceptación de usuario (UAT) cerradas por un grupo de expertos en la materia de DADI.
- Posteriormente, se realizará una prueba de aceptación de usuario (UAT) integrada con un grupo más amplio de diversas partes interesadas en el segundo trimestre de 2022.
- Una vez que entre en funcionamiento, habrá una fase de transición de seis (06) meses en la que se aceptarán en paralelo tanto los eAFs (versión PDF antigua) como los formularios web. Después de esto, solo se aceptará el HVF.
Consulte la siguiente infografía para conocer los plazos de implementación de HVF (actualizado en febrero de 2022, sujeto a cambios por parte de la EMA):
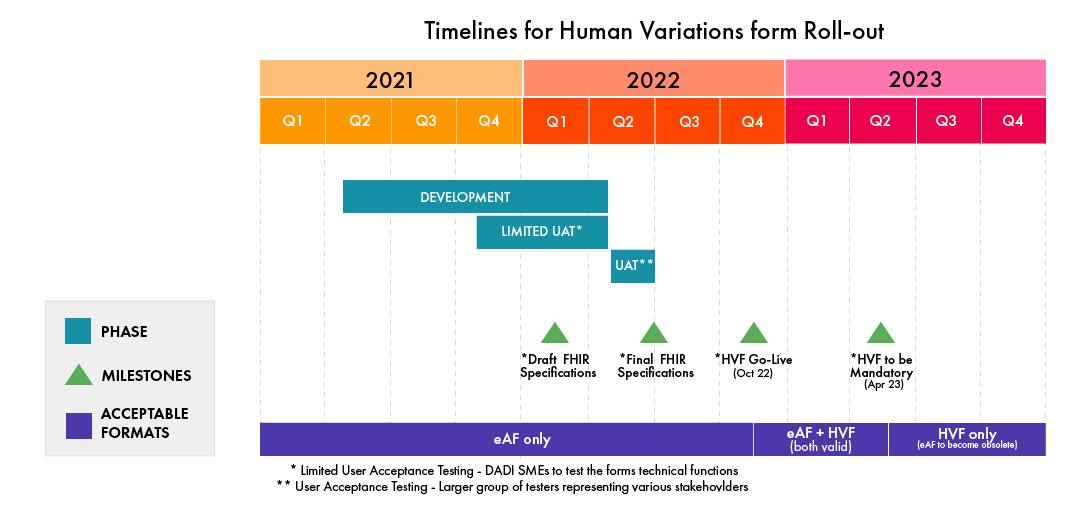
(fuente: EMA)
Asegurar la adaptabilidad al entorno reglamentario dinámico.
Todas las principales autoridades sanitarias están avanzando ahora hacia la presentación de conjuntos de datos y documentos de alta calidad. Es importante que las organizaciones los mantengan en un sistema unificado.
También es crucial tener una comprensión clara de todo el ciclo de vida de la presentación: sus requisitos, las personas y los procesos asociados a él, y la ubicación actual de los datos de origen mediante una evaluación exhaustiva de las necesidades. La limpieza y el enriquecimiento de datos deben priorizarse si la evaluación indica una necesidad.
Es imperativo contar con un Sistema de Gestión de Información Reglamentaria (RIMS) que se adapte a las regulaciones y directrices en evolución, sea flexible para reconfigurar las necesidades actuales de la organización y cumpla con el entorno reglamentario dinámico. Para saber más sobre el conjunto de soluciones reglamentarias de Freyr, que prepararán a su organización para DADI y otras alteraciones de procesos similares, visítenos en Freyr Digital.









