
El 9 de febrero de 2022, la Agencia Europea de Medicamentos (EMA) inició el establecimiento de un Centro de Coordinación para el Análisis de Datos y la Red de Integración del Mundo Real (DARWIN EU®). Es el primer paso hacia la integración de la Evidencia del Mundo Real (RWE) en la evaluación de medicamentos en toda la Unión Europea (UE). Garantizar la seguridad y eficacia de los medicamentos es la actividad principal de cualquier Agencia Reglamentaria, y la RWE está demostrando ser una fuente fiable para recopilar evidencia en tiempo real de las bases de datos sanitarias globales. Por lo tanto, esta medida de la EMA tiene como objetivo mejorar la calidad de los medicamentos en la región de la UE y hacerlos disponibles más rápidamente.
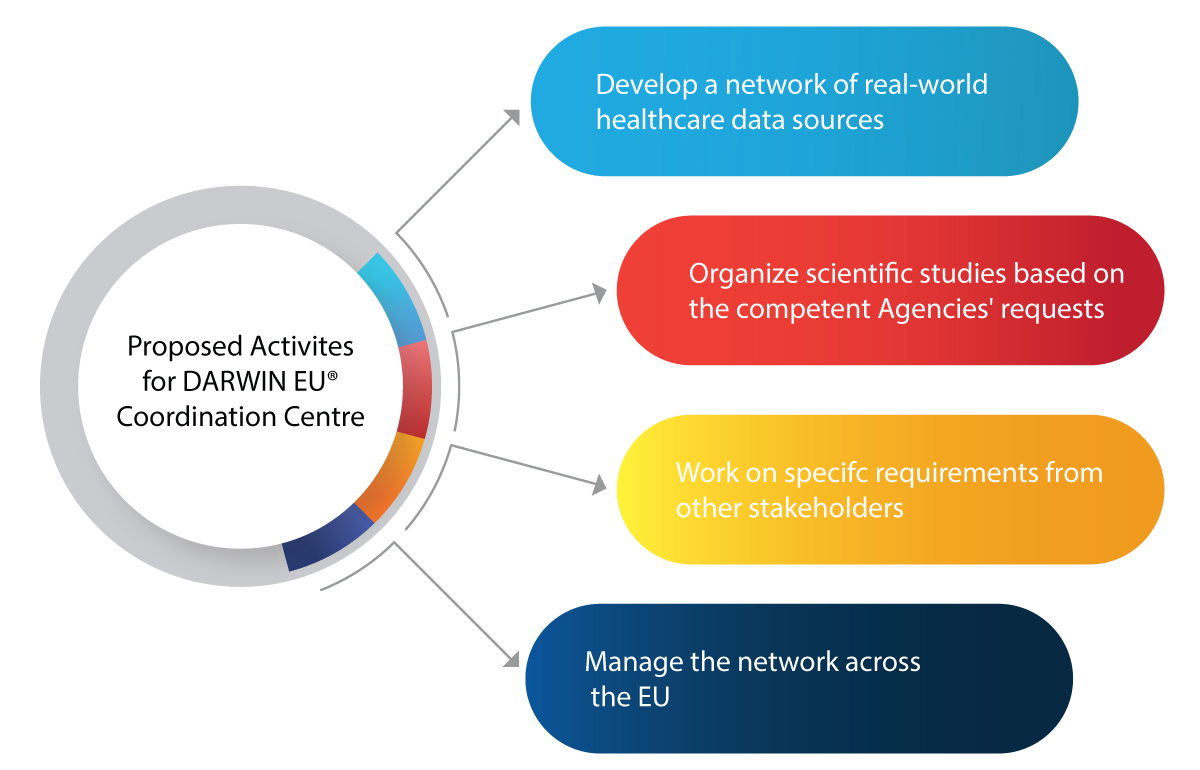
Principales actividades planificadas para el Centro de Coordinación de DARWIN EU®
¿Cómo va a ayudar DARWIN EU® a la EMA y a las autoridades pertinentes en el ámbito regulatorio?
Los medicamentos innovadores que están fácilmente disponibles para los pacientes son una necesidad urgente. Los procesos reglamentarios para el desarrollo, aprobación, comercialización y vigilancia post-comercialización requieren una cantidad considerable de tiempo, lo que hace que la demanda de medicamentos novedosos no se satisfaga. Reducir el tiempo de comercialización, al mismo tiempo que se garantiza la seguridad, eficacia y calidad de los medicamentos innovadores, es el camino a seguir. Varias Autoridades Sanitarias globales están identificando los beneficios de integrar la RWE en sus aprobaciones reglamentarias, y DARWIN EU® es la iniciativa de la EMA.
La EMA planea conectar la red reglamentaria europea de medicamentos al Espacio Europeo de Datos Sanitarios (EHDS) para un mejor intercambio de datos y un acceso mejorado a varios tipos de datos de salud bajo este programa. También establecerá estándares para las evaluaciones científicas y la toma de decisiones reglamentarias.
Estas son algunas de las actividades que DARWIN EU® se propone lograr:
- Uso de RWE en actividades de toma de decisiones para la regulación de nuevos medicamentos, vacunas, etc.
- Integración de la evidencia del mundo real (RWE) en todo el ciclo de vida de un medicamento, como el desarrollo, la autorización y la vigilancia post-comercialización
- Prepararse para cualquier emergencia médica futura, como pandemias
- Beneficiar a la industria farmacéutica con RWE perspicaz y fiable sobre pacientes, enfermedades y el uso de medicamentos
- Tomar decisiones reglamentarias informadas basadas en RWE para el uso seguro y eficaz de los medicamentos
- Mejorar la accesibilidad de medicamentos que salvan vidas a los pacientes que los necesitan gracias a un análisis de datos preciso y oportuno
Plazos propuestos para que DARWIN EU® sea una red completamente funcional en la UE
La EMA también especifica los plazos para que DARWIN EU® esté plenamente operativo, y son los siguientes:
- 2021 – Inicio del proyecto
- 2022 – Establecimiento de DARWIN EU®
- 2023 – Desarrollo de DARWIN EU® y la definición de sus usos
- 2024 – Puesta en pleno funcionamiento de DARWIN EU®
- 2025 – Mejorar los usos reglamentarios de los datos de atención médica aumentando los alcances en términos de medicamentos, geografía, etc.
La EMA está colaborando con el Centro Médico Universitario Erasmus de Róterdam para el establecimiento de DARWIN EU®. El objetivo de esta asociación es el establecimiento del Centro de Coordinación para crear una red de datos distribuida. Ambos también han asumido las tareas de realizar estudios científicos, apoyar los procesos de toma de decisiones reglamentarias y gestionar un catálogo de fuentes de datos del mundo real.
¿Qué significa el inicio de DARWIN EU® para el futuro?
La EMA y los Jefes de Agencias de Medicamentos (HMA) siempre han trabajado juntos para identificar los desafíos, establecer metas con plazos definidos y definir prioridades en sus documentos de estrategia quinquenales (05 años). Su objetivo es proporcionar una dirección estratégica a las actividades llevadas a cabo por la red reglamentaria europea de medicamentos.
La puesta en marcha de DARWIN EU® es un paso importante hacia la implementación de la Estrategia de Red de la EMA. Los objetivos principales son realizar estudios científicos para responder a preguntas de investigación, apoyar la evaluación de medicamentos en la UE y mantener Metadata para las actividades reglamentarias de los medicamentos. Se prevé que DARWIN EU® sea un actor principal en la regulación de medicamentos en Europa, y se propone que los estudios piloto estén listos para finales de 2022.
Si es un fabricante de medicamentos y desea saber más sobre RWE y cómo está configurando el futuro de la toma de decisiones reglamentarias, contacte con los expertos en Asuntos Regulatorios de Freyr.









