
La Administración de Productos Terapéuticos (TGA) de Australia tiene normas estrictas para el registro de nuevos medicamentos de venta con receta con ingredientes activos novedosos. Recientemente, la TGA ha ideado un proceso revisado para mejorar la eficacia de los medicamentos de venta con receta que salvan vidas y ponerlos a disposición de los pacientes más rápidamente. Estos cambios son pertinentes para las solicitudes que deben estar respaldadas por datos no clínicos, clínicos y/o de bioequivalencia (categoría 1 y categoría 2). La TGA publicó un documento en agosto con los detalles de los requisitos reglamentarios al respecto.
Características destacadas en el nuevo proceso de registro para medicamentos de prescripción.
- La TGA ha ideado un proceso de registro por fases y ha denominado las etapas como hitos. Cada una de ellas sigue una vía separada.
- El nuevo proceso tiene como objetivo mejorar la calidad del expediente. Los expedientes se preparan siguiendo un formato de documento técnico común (CTD) y cumplen con todos los requisitos reglamentarios.
- La fase de planificación previa a la presentación es importante ya que los solicitantes presentan los detalles de la solicitud prospectiva. Esto se realiza al menos dos meses y cuarto (02 ¼) antes de la presentación del expediente completo. Esta etapa tiene como objetivo ayudar a la TGA a establecer las fechas de los hitos posteriores y a preparar los recursos para gestionar el CTD.
- La siguiente fase es la presentación. Una vez hecho esto, la TGA no permite al solicitante ofrecer datos o información adicional después de la fecha de presentación. Es obligatorio presentar un expediente completo que sea correcto y de alta calidad.
- Según la sección 31 de la Ley de Productos Terapéuticos de 1989, la TGA solicita información adicional en la etapa de evaluación. Después de la evaluación inicial, todas las solicitudes se recopilan y se envían al solicitante.
Para comprender los hitos en el proceso renovado, consulte los siguientes diagramas de flujo.
Hito 1
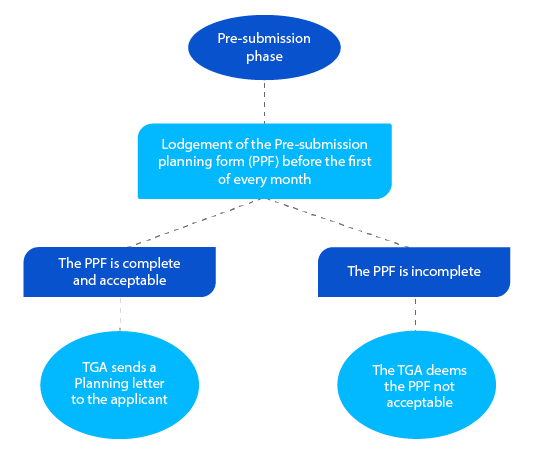
La carta de planificación contiene la fecha prevista en la que la TGA espera la presentación del expediente y otras fechas clave para la solicitud de medicamentos de prescripción.
Hito 2
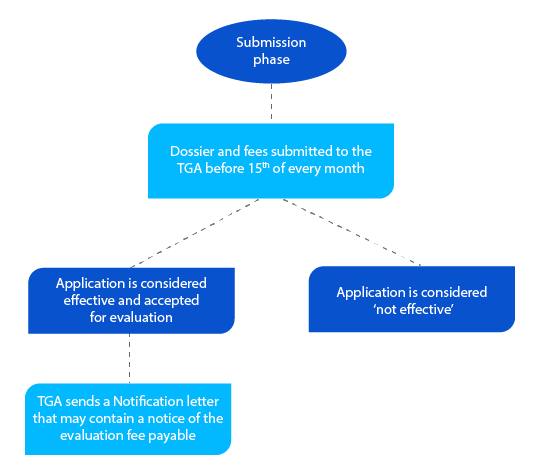
El expediente contiene información que ayuda a la TGA a evaluar la solicitud, y si todo es aceptable, se envía una carta de notificación antes de finalizar el mes en que el solicitante presentó el expediente.
Hito 3
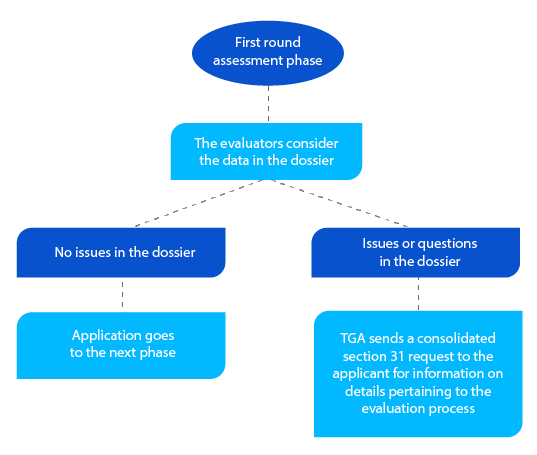
Además de la sección consolidada 31, cuando corresponda, la TGA envía copias de los informes de evaluación preparados por los evaluadores de calidad, no clínicos, clínicos y de los Planes de Gestión de Riesgos (RMP).
Hito 4
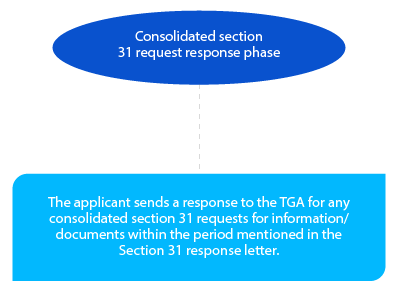
El solicitante puede designar el plazo de respuesta de la sección 31. Puede ser de treinta (30) o sesenta (60) días y debe destacarse en el PPF. Este período debe ser confirmado por la TGA en la Carta de Planificación. El formato aceptable de la respuesta es CTD, y la misma debe enviarse en formato de copias impresas y electrónicas.
Dado que esta es la última oportunidad para que el solicitante proporcione cualquier información faltante a la TGA, debe hacerse de manera conforme a la normativa.
Hito 5
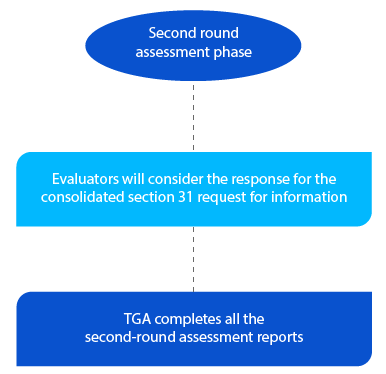
La TGA dispone de dos (02) meses para las solicitudes de nuevos medicamentos genéricos en la segunda ronda de informes de evaluación y un (01) mes para todos los demás tipos de solicitud. Los informes se envían a los solicitantes correspondientes una vez finalizada la segunda evaluación.
Hito 6
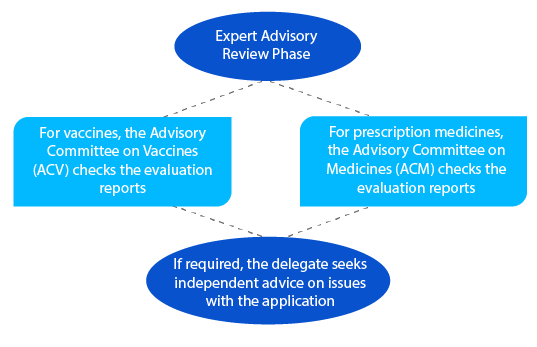
Tras la revisión consultiva, la TGA envía una notificación con los detalles de la recomendación que recibe del ACV o del ACM.
Hito 7
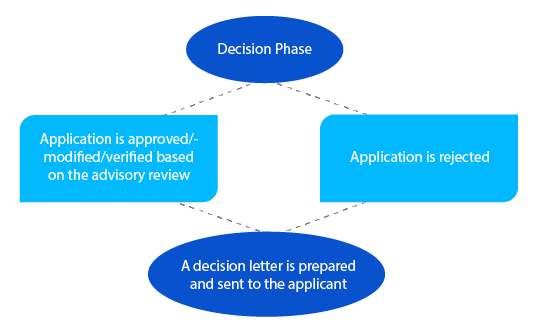
En caso de problemas pendientes, el delegado puede comunicarse con el solicitante en esta fase antes de tomar una decisión. Para las solicitudes bajo la sección 23 de la Ley de Productos Terapéuticos de 1989 (medicamentos listados recientemente evaluados en el Registro Australiano de Productos Terapéuticos (ARTG)), se envía una notificación al solicitante dentro de los veintiocho (28) días siguientes a la toma de la decisión.
Hito 8
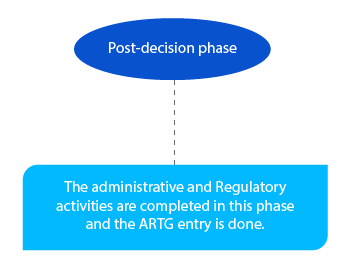
Los pagos pendientes se gestionan en esta etapa. Y deben completarse antes de que finalice el mes siguiente a la decisión del delegado.
Con la TGA tomando todas las precauciones para garantizar la seguridad, eficacia y calidad de los medicamentos recetados mientras reduce su tiempo de comercialización, la responsabilidad recae en el solicitante de realizar las presentaciones pertinentes para un proceso de registro sin problemas. Sea cual sea la etapa, colaborar con un proveedor de servicios reglamentarios End-to-End que sea experto en el registro de medicamentos recetados es la situación ideal. Contacte a una entidad reglamentaria experimentada para una vía de cumplimiento; manténgase actualizado y cumpla con la normativa.










