
Los ensayos ciegos son la piedra angular de la integridad de los ensayos clínicos, ya que eliminan los sesgos y garantizan una evaluación objetiva de los productos en investigación. Sin embargo, tras el rigor científico se esconde un componente creativo fundamental: las etiquetas de los envases para ensayos clínicos. Para artwork regulatorio, el diseño para ensayos ciegos supone encontrar el equilibrio entre el cumplimiento normativo, la confidencialidad y la claridad.
En Freyr Solutions, nos especializamos en artwork que cumplen con la normativa y están preparados para auditorías, artwork ensayos clínicos internacionales. En este blog, analizamos cómo artwork de los envases para ensayos clínicos artwork adaptarse para satisfacer las exigencias específicas de los estudios ciegos.
Por qué Artwork en los estudios ciegos
El diseño de etiquetas de envases para estudios ciegos (normalmente en ensayos clínicos) implica procesos específicos para mantener el enmascaramiento y garantizar el cumplimiento de los requisitos normativos y propios del ensayo.
A diferencia de los productos comerciales, el artwork los estudios ciegos debe ocultar la identidad del producto, pero al mismo tiempo proporcionar información clara y aprobada por las autoridades reguladoras a los usuarios finales, como investigadores, farmacéuticos y pacientes. Cualquier discrepancia —ya sea en el color, la forma, la tipografía o el contenido del etiquetado— puede desvelar involuntariamente el estudio.
Por lo tanto, Artwork los estudios ciegos debe tener unos objetivos clave:
- Garantizar la ceguera del estudio: La etiqueta no debe revelar ninguna información que pueda desvelar la identidad del tratamiento. Debe mantenerse la coherencia visual en todos los grupos del estudio.
- Usabilidad: Garantizar un uso seguro y correcto (por ejemplo, una aplicación adecuada por parte del personal del centro). Evitar la diferenciación del producto mediante elementos de diseño.
- Gestionar los datos variables: deben estar disponibles los elementos clave de los datos variables, tales como los códigos de aleatorización, las fechas de caducidad, los números de kit, las identificaciones de los pacientes y la información específica de cada visita.
- Cumplimiento normativo: Cumplir con la normativa global y regional sobre ensayos clínicos
- Trazabilidad: Garantizar una vinculación clara con el ensayo y el paciente sin revelar el tipo de producto. Debe estar sujeta a control de versiones y permitir la auditabilidad.
Proceso de creación de etiquetas para envases en ensayos clínicos ciegos
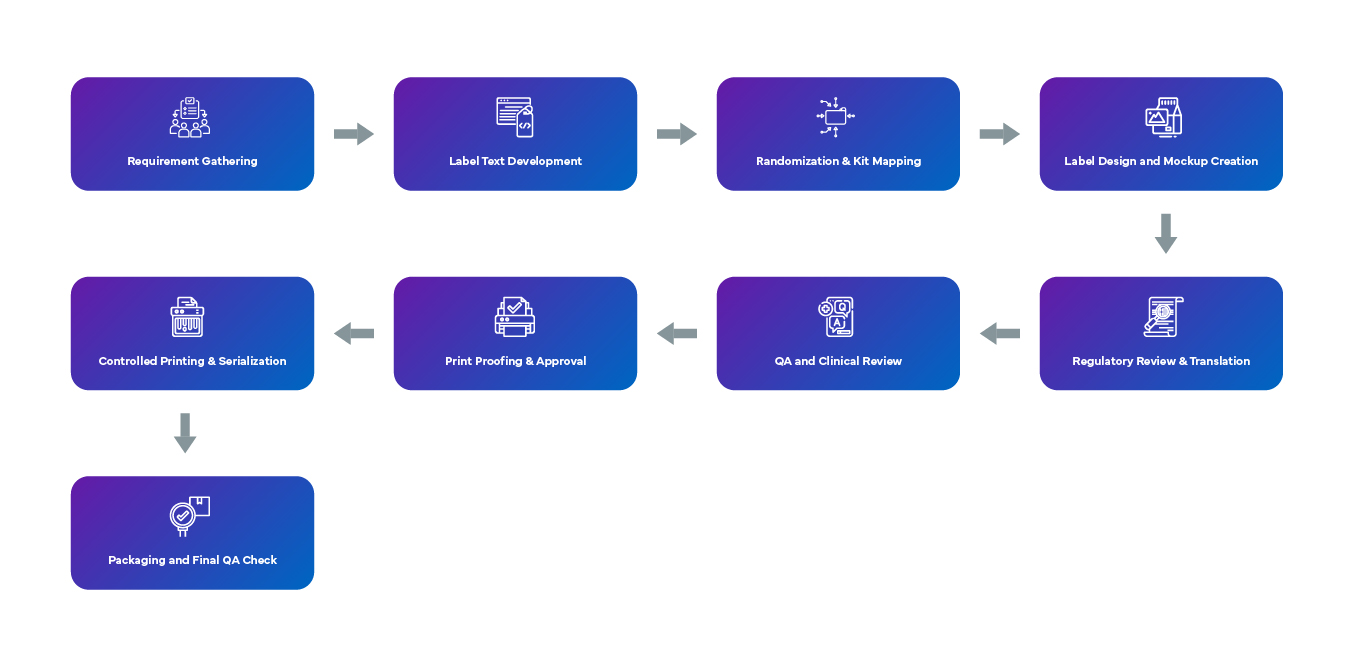
El proceso de diseño de etiquetado ciego comienza con la recopilación de requisitos mediante la revisión del protocolo y las aportaciones de las partes interesadas, lo que garantiza el cumplimiento de la normativa específica de cada país. El texto de las etiquetas neutras se elabora utilizando términos como «Medicamento del estudio» e incluye información esencial, como los números de ensayo, las fechas de caducidad y las advertencias, al tiempo que se evitan los identificadores que puedan revelar el tratamiento. La aleatorización y la asignación de kits se gestionan de forma segura, con etiquetas diseñadas para mantener el enmascaramiento, a menudo utilizando códigos de barras. Se crean maquetas de diseño teniendo en cuenta el tamaño del envase, las necesidades multilingües y los requisitos de superposición. Las revisiones normativas y de traducción garantizan el cumplimiento a nivel mundial. Los equipos QA clínicos verifican la alineación con el protocolo, mientras que las pruebas de las etiquetas se someten a comprobaciones electrónicas y aprobaciones formales. La estrategia de aplicación de etiquetas —ya sea primaria, secundaria o sobreetiquetado— tiene en cuenta las limitaciones ambientales. La impresión controlada, a menudo justo a tiempo, garantiza la trazabilidad serializada y el envasado final se completa bajo QA para confirmar la precisión de la etiqueta, la adhesión y la integridad del enmascaramiento.
Artwork clave a tener en cuenta en Artwork de las etiquetas de los estudios ciegos
| Artwork | Requisitos de diseño en los ensayos ciegos | Artwork de Freyr |
| Paleta de colores | Evita la diferenciación por colores que podría indicar los grupos de tratamiento | Paletas de colores uniformes en todas las ramas; se prefieren los tonos en escala de grises o neutros |
| Fuentes y tipografía | Estilo y tamaño de fuente uniformes en todas las variantes para evitar pistas visibles | Las directrices tipográficas predefinidas se aplican de manera uniforme en todos los diseños de las etiquetas |
| Diseño y jerarquía de las etiquetas | Colocación del texto y los elementos gráficos según las directrices técnicas | Diseños basados en plantillas para garantizar la uniformidad |
| Etiquetado de placebo frente a etiquetado activo | No debe presentar ninguna diferencia visual | Utilice plantillas de etiquetas idénticas; solo los campos variables difieren en función de los datos codificados. |
| Códigos de aleatorización/seguimiento | Debe estar presente, pero no debe ser interpretable por el usuario final | Capacidad para generar cualquier tipo de código de barras. |
| Gestión lingüística | El contenido multilingüe no debe introducir sesgos de maquetación | Los bloques de texto se han diseñado con una disposición simétrica. |
| Campos de datos dinámicos | Datos como el número de lote, la fecha de caducidad y el ID del componente varían según el envase | Campos de marcador de posición o según lo acordado por el equipo de diseño para su ubicación |
| Material y formato de la etiqueta | Debe permitir el enmascaramiento y el desenmascaramiento según las necesidades del estudio | Utilización de etiquetas en folleto, etiquetas adhesivas o sobreetiquetas, según sea necesario |
| Control de versiones y aprobación | Las etiquetas se actualizan con frecuencia debido a modificaciones en los protocolos | artwork centralizada artwork con control de versiones de las etiquetas y gestión de aprobaciones |
Referencias de organismos reguladores para el etiquetado de ensayos clínicos
Región | Organismo reglamentario | Referencia de la guía |
| UE | EMA | Anexo VI del Reglamento (UE) n.º 536/2014 |
| US | FDA | 21 CFR, parte 312.6 |
| Reino Unido | MHRA | Guía de buenas prácticas clínicas |
| Canadá | Health Canada | Documento de orientación para promotores de ensayos clínicos |
Errores habituales en Artwork de los estudios ciegos Artwork y cómo evitarlos)
✗ Uso de etiquetas de diferentes dimensiones para el grupo activo y el de placebo
✓ Estandarizar el tamaño y la forma en todos los grupos
✗ La ubicación de los idiomas varía según el país
✓ Utiliza bloques de idiomas duplicados con un formato coherente
✗ Identificadores de lote/producto visibles en artwork del producto
✓ Utilizar datos codificados y códigos de barras para ocultar los identificadores visibles
¿Por qué colaborar con Freyr en Artwork creación de Artwork para estudios ciegos?
- Experiencia en el diseño de etiquetas ciegas para ensayos clínicos a nivel mundial
- Disponibilidad de información sobre normativa en US, la Unión Europea, el Reino Unido, Canadá y la región de Asia-Pacífico
- Uso de la herramienta Artwork , si es necesario. La herramienta se puede personalizar para adaptarse a los requisitos de los ensayos clínicos.
- Archivos con control de versiones, conformes con las normas y listos para auditorías
- Servicios de traducción multilingüe y revisión técnica de etiquetas para cualquier país o región










