
La necesidad médica no cubierta (UMN) es una de las prioridades más apremiantes de los sistemas de salud. La ciencia y la tecnología en constante evolución en torno a la atención médica han albergado el potencial para explorar diversas opciones terapéuticas. Las autoridades sanitarias fomentan terapias innovadoras que prometen beneficios significativos para la calidad de vida de los pacientes. Basándose en la priorización de la innovación y la focalización en las necesidades no cubiertas de los pacientes para el desarrollo de fármacos, la Agencia Europea de Medicamentos (EMA) introdujo la vía de Medicamentos Prioritarios (PRIME) en 2016. Desde entonces, la vía PRIME ha sido un método para conceder aprobaciones a terapias innovadoras en un plazo acelerado. Este tipo de vía facilitada puede ser explorada por cualquier empresa, desde empresas emergentes hasta biotecnológicas de tamaño medio y grandes organizaciones multinacionales. Sin embargo, la calificación para esta vía se limita a productos en desarrollo y que aún no han solicitado una autorización de comercialización a través del procedimiento centralizado. Los criterios de calificación se aplican rigurosamente. Entre marzo de 2016 y abril de 2022, solo el 24% de las solicitudes recibieron el respaldo, mientras que el 72% de las solicitudes PRIME fueron rechazadas. Del 24% que fue seleccionado para la vía PRIME, la mayoría pertenecía al área terapéutica de oncología.
Los innovadores que buscan autorizaciones de comercialización para enfermedades raras o medicamentos huérfanos a menudo pueden tener conjuntos de datos limitados disponibles como evidencia para respaldar sus solicitudes de nuevos medicamentos, según lo exigen los reguladores. Las solicitudes de medicamentos de terapia avanzada (ATMP) y medicamentos huérfanos suelen enfrentar tales desafíos. Debido a los datos limitados de la población de pacientes, se fomenta la interacción constante con los reguladores para permitir una mejor comprensión de los requisitos de revisión científica y aprobación. La vía PRIME puede ser útil para dichas terapias debido a la participación temprana de los reguladores en la provisión de apoyo proactivo y orientación para la recopilación de datos y la evaluación de riesgos y beneficios.
Ventajas de seguir la vía PRIME-Pathway
- Ayuda a los innovadores a desarrollar un plan de desarrollo bien elaborado.
- Beneficia a los innovadores al involucrar a las Autoridades Sanitarias en la etapa temprana de desarrollo; esto contribuye a la elaboración de solicitudes de autorización de comercialización de alta calidad.
- Acelera la evaluación general al reducir el tiempo promedio de evaluación para que los medicamentos puedan llegar a los pacientes más rápidamente.
- Apoya a los innovadores para que centren su atención en el desarrollo de medicamentos que mejoren los resultados de los pacientes y aborden sus necesidades no cubiertas.
Detalle del tiempo de evaluación.
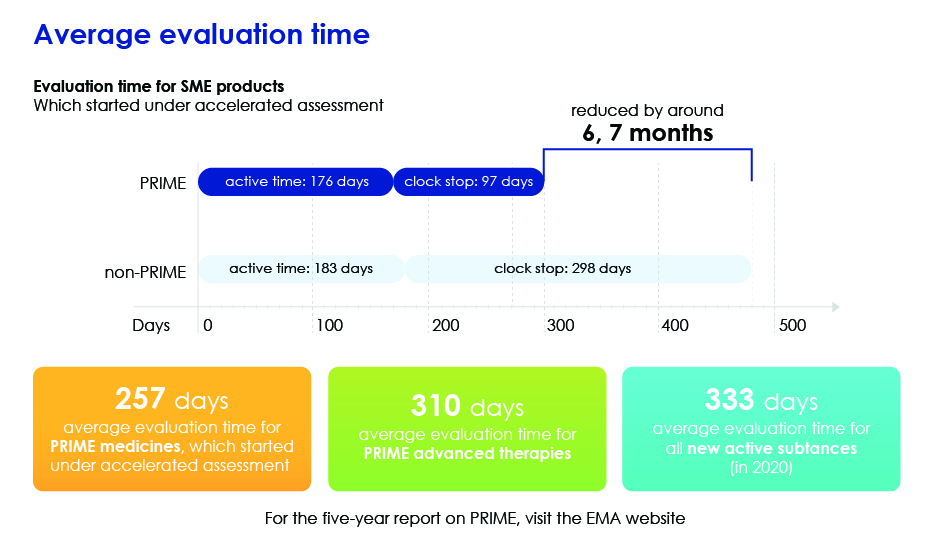
Solicitudes para la vía PRIME
La vía PRIME prioriza las necesidades médicas no cubiertas. De las 384 solicitudes PRIME recibidas desde marzo de 2016, solo 18 llegaron hasta la autorización de comercialización en junio de 2021.

¿Está listo para PRIME?
La existencia de la vía PRIME se debe a importantes necesidades médicas no cubiertas y al enfoque en cerrar las brechas por parte de la Red Reglamentaria Europea de Medicamentos (EMRN). Para evaluar la idoneidad de un producto para la vía PRIME, se debe considerar lo siguiente:
- Hallazgos: Los solicitantes deben indicar la necesidad médica no cubierta y proporcionar un argumento convincente sobre cómo su producto abordará el problema.
- Potencial: Los solicitantes deben demostrar el potencial beneficioso de la terapia según los criterios de necesidad médica no cubierta.
- Datos preclínicos: Los solicitantes deben presentar algunos datos sobre la eficacia o el rendimiento de la terapia en el sistema biológico humano. Los modelos no clínicos, por muy precisos que sean, no proporcionan una visión exacta de su comportamiento en el sistema biológico humano.
- Etapa de desarrollo: El solicitante debe identificar la etapa correcta para ingresar a la vía PRIME y obtener una orientación óptima de los reguladores, y así continuar con la solicitud.
Después de la subvención PRIME
Una vez que a un solicitante se le haya concedido la oportunidad de acceder a la vía facilitada, la EMA hará lo siguiente:
- Asignar un ponente del Comité de Medicamentos de Uso Humano (CHMP) o del Comité de Terapias Avanzadas (CAT) en el caso de terapias avanzadas.
- Organizar una reunión de inicio con el ponente del CHMP/CAT y un grupo multidisciplinar de expertos para proporcionar orientación sobre el plan de desarrollo general y la estrategia normativa.
- Asignar un único punto de contacto para el solicitante.
- Proporcionar asesoramiento científico en cada hito clave del desarrollo, involucrando a un conjunto adicional de partes interesadas, como los organismos de evaluación de tecnologías sanitarias, para acelerar el acceso de los pacientes al nuevo medicamento.
- Confirmar el potencial de evaluación acelerada en el momento de una solicitud al considerar la autorización de comercialización.
¿Está lista su solicitud para la vía de Medicamentos Prioritarios (PRIME-ready)? Contacte con Freyr hoy mismo y evalúe. Obtenga más información sobre cómo podemos ayudarle con su estrategia reglamentaria y la designación de la vía PRIME. Manténgase informado. Manténgase conforme.









