
Las innovaciones en las combinaciones de fármacos y dispositivos han dado lugar a avances significativos en la atención al paciente. Los productos farmacéuticos combinados con Dispositivos Médicos ofrecen una administración dirigida de fármacos, mejores resultados terapéuticos y una mayor adherencia del paciente. Sin embargo, navegar por el panorama reglamentario para las combinaciones de fármacos y dispositivos puede ser complejo.
Este blog explorará las consideraciones y desafíos asociados con las operaciones reglamentarias para productos combinados de fármacos y dispositivos, lo que ofrece información para optimizar los procesos.
Panorama general y marco reglamentario para combinaciones de fármacos y dispositivos
Los productos combinados fármaco-dispositivo combinan los efectos terapéuticos de los fármacos con las capacidades de administración de los Dispositivos Médicos. Las combinaciones fármaco-dispositivo incluyen stents liberadores de fármacos, inhaladores y dispositivos respiratorios, parches transdérmicos, sistemas de administración de insulina, sistemas de infusión de fármacos y balones recubiertos de fármacos. La administración dirigida, la eficacia mejorada, una mayor adherencia del paciente y un control preciso del tratamiento son algunos de los atributos destacados de estos productos.
Autoridades reglamentarias como la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA de US), la Agencia Europea de Medicamentos (EMA) y otras, han establecido directrices para combinaciones de fármacos y dispositivos. En los últimos años se han observado avances significativos en el panorama reglamentario, con un mayor énfasis en la armonización, las evaluaciones basadas en el riesgo y la vigilancia post-comercialización.
Consideraciones clave para las operaciones reglamentarias
Al gestionar las operaciones reglamentarias para combinaciones de medicamentos y dispositivos, algunas de las consideraciones que entran en juego se detallan a continuación:
Comprender la clasificación de productos y las vías reglamentarias
Comprender la clasificación de los productos combinados fármaco-dispositivo y seleccionar la vía regulatoria adecuada es crucial. Los fabricantes deben determinar si se trata de una combinación fármaco-dispositivo, una categoría de dispositivo recubierto con fármaco o una categoría de producto coenvasado. La selección de la vía correcta para el tipo de producto específico es vital para un acceso exitoso al mercado.
Abordar los requisitos científicos y técnicos
Incluye asegurar la compatibilidad entre los componentes del medicamento y del dispositivo, realizar estudios de estabilidad para evaluar la vida útil del producto, validar los procesos de fabricación e implementar evaluaciones de riesgo para identificar y mitigar posibles peligros.
Atención al paciente y pruebas de usabilidad
La atención al paciente y la ingeniería de usabilidad desempeñan un papel importante en el desarrollo de estos productos combinados. Considerar factores como la interfaz de usuario, la ergonomía, el manejo del dispositivo y la adherencia del paciente durante el desarrollo del producto ayuda a garantizar su uso seguro y eficaz por parte de pacientes y profesionales de la salud con errores mínimos.
Consideraciones post-comercialización
Las obligaciones post-comercialización son un aspecto crítico del cumplimiento reglamentario para las combinaciones de fármacos y dispositivos. Los fabricantes deben establecer procesos para la notificación de eventos adversos, la vigilancia post-comercialización y la notificación de vigilancia para supervisar la seguridad y el rendimiento de sus productos.
Mantenerse al día con las directrices normativas y las actualizaciones recientes.
Mantenerse al tanto de las últimas directrices y actualizaciones es crucial para garantizar el cumplimiento y alinear las estrategias reglamentarias con las expectativas actuales. El panorama reglamentario para las combinaciones de fármacos y Dispositivos Médicos está en constante evolución. Alinear las directrices de la FDA, el Reglamento de Dispositivos Médicos (MDR) de la UE y el Consejo Internacional de Armonización de los Requisitos Técnicos para Productos Farmacéuticos de Uso Humano (ICH) puede ayudar a los fabricantes a mantenerse conformes.
Mejores prácticas para optimizar las operaciones reglamentarias
Para optimizar las operaciones reglamentarias de las combinaciones de fármacos y dispositivos, las empresas farmacéuticas pueden seguir las mejores prácticas ilustradas en el gráfico circular a continuación:
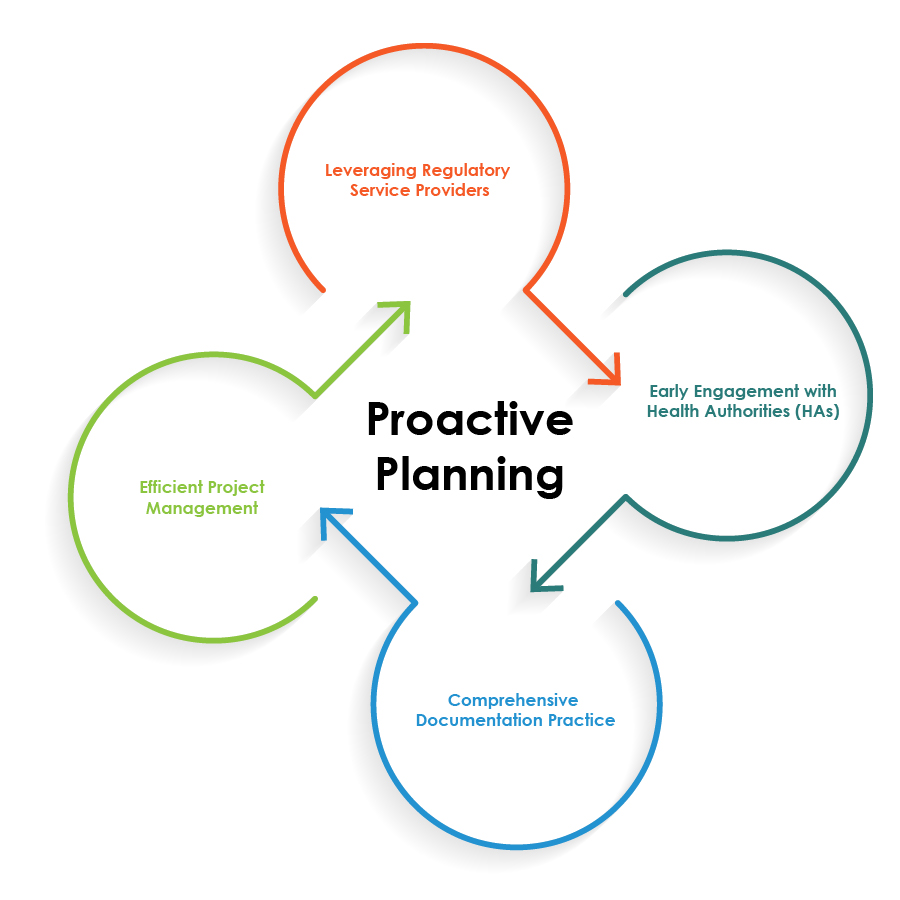
La planificación proactiva es la piedra angular para operaciones reglamentarias fluidas de productos combinados fármaco-dispositivo
Tendencias y desafíos futuros
Estar atento a las tendencias futuras y las deficiencias es crucial para las empresas farmacéuticas y los profesionales reglamentarios involucrados en las operaciones reglamentarias de estos productos. A continuación, se enumeran algunas tendencias y desafíos a tener en cuenta:
- Tecnologías emergentes: La nanotecnología, la impresión 3D y las aplicaciones relacionadas influyen en el desarrollo de combinaciones innovadoras de fármacos y dispositivos. Estas tendencias tecnológicas ofrecen administración dirigida de fármacos, medicina personalizada y monitorización mejorada del paciente. Sin embargo, también presentan desafíos reglamentarios únicos relacionados con la seguridad, la eficacia y el control de calidad.
- Ciberseguridad: Con la creciente conectividad de los Dispositivos Médicos, garantizar la seguridad de los datos y protegerse contra las ciberamenazas se vuelve fundamental. La integración de medidas sólidas de ciberseguridad y mantenerse al día con las mejores prácticas para la seguridad de los dispositivos son consideraciones críticas para las operaciones reglamentarias.
- Desafíos diversos: Estos incluyen las complejidades de la cadena de suministro global, como el abastecimiento de materias primas, la disponibilidad de componentes y los procesos de fabricación, que plantean desafíos para mantener el cumplimiento reglamentario y garantizar la calidad del producto. Las prácticas sólidas de gestión de la cadena de suministro, las evaluaciones de riesgos y la supervisión de proveedores son esenciales para abordar estos desafíos y mitigar los riesgos asociados.
Navegar el panorama reglamentario para productos combinados de fármacos y dispositivos requiere una comprensión exhaustiva del marco reglamentario, las directrices recientes y las mejores prácticas. Abordar las consideraciones clave, mantenerse al día con los cambios e implementar las mejores prácticas ayudará a las empresas farmacéuticas a optimizar sus operaciones reglamentarias. Colaborar con proveedores reglamentarios permite a las empresas aprovechar conocimientos y experiencias especializados y optimizar sus posibilidades de éxito reglamentario en este campo en evolución y exigente. Con nuestra probada experiencia en el cumplimiento de las normas reglamentarias globales, Freyr puede ayudar a lograr un recorrido del producto conforme. Para saber más, contáctenos.









