
La adopción de eCTD 4.0 representa un paso crucial hacia la modernización de las presentaciones reglamentarias en todo el mundo. Con beneficios como el seguimiento mejorado de documentos y eficiencias impulsadas por Metadata, no es de extrañar que las agencias globales estén adoptando este cambio.
¿Pero dónde se posiciona la EMA? A diferencia de la FDA, que ha delineado fases claras de implementación, la EMA está adoptando un enfoque más mesurado, comenzando con programas piloto y evaluaciones técnicas. En este blog, desglosamos los planes de la EMA para el eCTD 4.0, su impacto potencial en las presentaciones reglamentarias y cómo su empresa puede mantenerse a la vanguardia.
Más importante aún, ¿ha exigido la EMA el eCTD 4.0 ya? Profundicemos en ello.
¿Qué es eCTD 4.0 y en qué se diferencia de eCTD 3.2.2?
El Documento Técnico Común Electrónico (eCTD) es el formato aceptado internacionalmente para las presentaciones reglamentarias. Estandariza la forma en que las empresas farmacéuticas presentan las solicitudes de medicamentos y gestionan las actualizaciones del ciclo de vida en diferentes mercados.
La versión actual, eCTD 3.2.2, ha estado en uso durante años. Sin embargo, los organismos reglamentarios, incluida la EMA, han estado trabajando en la eCTD 4.0, que se basa en el estándar de Presentación de Productos Reglamentados (RPS) de Health Level 7 (HL7). Esta actualización mejora la eficiencia de las presentaciones y la gestión del ciclo de vida reglamentario.
Diferencias clave entre eCTD 3.2.2 y eCTD 4.0:
- Mejor gestión del ciclo de vida: Mejor seguimiento de las versiones de los documentos, reduciendo la duplicación.
- Granularidad más flexible: Permite la reutilización de documentos estructurados en diferentes presentaciones.
- Gestión mejorada de Metadata: Metadata más estructurada, lo que facilita las interacciones reglamentarias.
- Mayor interoperabilidad: Diseñado para funcionar mejor con los sistemas reglamentarios digitales en evolución a nivel mundial.
- Aunque estos cambios ofrecen numerosos beneficios, la transición a eCTD 4.0 requiere preparación, inversión y una comprensión de las expectativas reglamentarias.
Postura de la EMA sobre la adopción de eCTD 4.0
La gran pregunta en la mente de todos es: ¿Ha exigido la EMA el eCTD 4.0? La respuesta es que todavía no, pero la transición está en curso.
Estado Actual de eCTD 4.0 en la UE:
- Actualmente, eCTD 3.2.2 sigue siendo el estándar obligatorio para las presentaciones en la UE.
- La EMA ha estado evaluando activamente el eCTD 4.0, pero no ha hecho obligatorio su uso de forma oficial.
- La agencia está trabajando junto con otros organismos reguladores, como la FDA y la PMDA de Japón, para armonizar los estándares globales.
- No se han establecido plazos oficiales de transición, pero la EMA ha indicado que el eCTD 4.0 acabará siendo obligatorio.
Enfoque de la EMA: Implementación por fases con un programa piloto
A diferencia de la USFDA, que ha esbozado un plan de implementación por fases, la EMA está adoptando un enfoque estructurado. La agencia ha lanzado un Programa Piloto Técnico para probar la implementación de eCTD 4.0 con las partes interesadas de la industria.
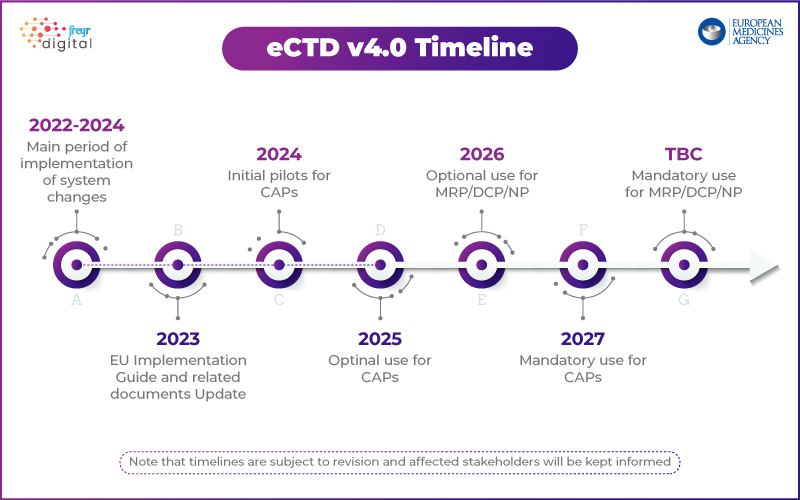
Aspectos destacados de la estrategia eCTD 4.0 de la EMA:
- Paso 1: Centrarse en la interoperabilidad técnica con herramientas reglamentarias.
- Fases futuras: Presentaciones de prueba, gestión del ciclo de vida y presentaciones agrupadas.
- Borrador del paquete de implementación disponible con vocabularios controlados y criterios de validación.
La EMA se compromete a garantizar una transición fluida, y las empresas de ciencias de la vida deben seguir las actualizaciones en la página oficial de eCTD de la EMA.
Desafíos y consideraciones para empresas de ciencias de la vida
Aunque eCTD 4.0 ofrece claros beneficios, su adopción no está exenta de desafíos. Estas son algunas consideraciones clave para las empresas farmacéuticas y biotecnológicas:
- Complejidades reglamentarias
- La transición gradual de la EMA significa que las empresas deben estar preparadas para dobles procesos de presentación (eCTD 3.2.2 y eCTD 4.0).
- Las diferentes regiones tendrán distintos plazos de adopción, lo que exigirá a las empresas mantenerse ágiles.
- Desafíos Técnicos
- La migración de datos de eCTD 3.2.2 a 4.0 requiere una planificación cuidadosa.
- Las reglas de validación cambiarán significativamente, exigiendo software y herramientas actualizados.
- Las empresas necesitan invertir en automatización y soluciones impulsadas por inteligencia artificial (IA) para asegurar el cumplimiento.
- Riesgos de cumplimiento
- El mapeo incorrecto de Metadata o el incumplimiento de los nuevos requisitos de granularidad de los documentos podría dar lugar al rechazo de la presentación.
- Los equipos reglamentarios necesitan una formación adecuada para comprender las nuevas reglas de validación.
- Impacto en los Flujos de Trabajo Existentes
- Las empresas necesitarán adaptar sus procesos internos para acomodar el eCTD 4.0.
- Será necesaria una mayor colaboración entre los equipos reglamentarios, de TI y de presentación.
¿La conclusión principal? Las empresas deben empezar a prepararse ahora, aunque la EMA aún no haya exigido el eCTD 4.0.
¿Cómo pueden las empresas prepararse para la transición a eCTD 4.0 de la EMA?
Aunque la EMA no ha establecido una fecha límite oficial, las empresas proactivas se beneficiarán de una preparación temprana. Así es como:
- Evaluar los procesos de presentación actuales
- Identificar las deficiencias en los flujos de trabajo eCTD 3.2.2 existentes.
- Evaluar cómo las nuevas reglas de gestión del ciclo de vida impactarán en las presentaciones en curso.
- Invierta en las herramientas eCTD 4.0 adecuadas
- Seleccione un software de presentación reglamentaria que sea compatible con eCTD 4.0.
- Asegurar que el software sea compatible con los estándares HL7 RPS y la automatización de Metadata.
- Capacitar a los equipos reglamentarios y de TI
- Realizar talleres y sesiones de formación sobre los cambios de eCTD 4.0.
- Proporcionar directrices para el etiquetado de Metadata y el seguimiento del ciclo de vida.
- Interactuar con la EMA y colegas de la industria
- Participe en los programas piloto y las consultas reglamentarias de la EMA.
- Manténgase actualizado sobre las últimas orientaciones de la EMA y las actualizaciones reglamentarias.
- Realizar pruebas y validación
- Realizar presentaciones de prueba internas utilizando estructuras de eCTD 4.0.
- Identificar posibles problemas en la granularidad de los documentos y la asignación de Metadata antes del mandato final de la EMA.
Al empezar ahora, las empresas pueden asegurar una transición fluida sin interrupciones en las presentaciones reglamentarias.
¿Qué sigue? Futuro del eCTD 4.0 en Europa
Si bien el cronograma completo de transición sigue sin estar claro, la estrategia a largo plazo de la EMA implica:
- Estandarizar las presentaciones en todos los mercados globales, mejorando la coherencia y la eficiencia.
- Reducir los plazos de aprobación mediante un mejor seguimiento del ciclo de vida de las presentaciones.
- Integración de la IA y la automatización en los flujos de trabajo reglamentarios para mejorar el cumplimiento.
En los próximos años, podemos esperar más claridad de la EMA, incluidos los plazos de transición oficiales y los nuevos criterios de validación.
Conclusión
Aunque la EMA aún no ha exigido el eCTD 4.0, es solo cuestión de tiempo que se convierta en el estándar para las presentaciones regulatorias en la UE. Las empresas que se preparen proactivamente obtendrán una ventaja competitiva, asegurando el cumplimiento y evitando obstáculos regulatorios de última hora.
Puntos clave
- eCTD 3.2.2 sigue siendo el estándar actual, pero eCTD 4.0 está en el horizonte.
- La EMA está adoptando un enfoque gradual, sin un mandato oficial todavía.
- Las empresas deberían empezar a prepararse ahora para asegurar una transición fluida.
- Invertir en nuevas tecnologías, formar equipos y probar las presentaciones será clave.
Llamada a la acción
Manténgase actualizado con los anuncios reglamentarios de la EMA y comience a evaluar su preparación para eCTD 4.0. Cuanto antes se prepare, más fácil será la transición cuando llegue el mandato.
¿Necesita ayuda para elegir un software compatible con eCTD 4.0 o para comprender cómo esta transición afecta a su negocio? No dude en contactarnos.









