
Para mejorar la accesibilidad de medicamentos innovadores para los pacientes en el Reino Unido después del Brexit, se lanzó en enero de 2021 una nueva vía de aprobación acelerada conocida como Vía Innovadora de Licencias y Acceso (ILAP). Su objetivo principal era proporcionar una hoja de ruta integrada para todas las partes interesadas que mejora el proceso de desarrollo de productos. La ILAP apoya además a los desarrolladores comerciales y no comerciales al facilitar el acceso de medicamentos innovadores a la población de pacientes, reduciendo el tiempo de comercialización. Las empresas farmacéuticas pueden explorar la ILAP como una vía una vez que los datos no clínicos estén consolidados. Es aplicable a Nuevas Entidades Químicas (NCE), medicamentos biológicos, nuevas indicaciones y medicamentos reposicionados.
El ILAP es una iniciativa desarrollada conjuntamente por la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) en asociación con el Centro de Terapéutica y Toxicología de Gales (AWTTC), el Instituto Nacional de Salud y Excelencia en la Atención (NICE) y el Consorcio Escocés de Medicamentos (SMC) como socios permanentes. Los socios colaboradores del ILAP incluyen el Servicio Nacional de Salud de Inglaterra (NHS), la Autoridad de Investigación Sanitaria (HRA) y el Instituto Nacional de Investigación Sanitaria (NIHR). Juntos, las partes interesadas aportan conocimientos reglamentarios, científicos, éticos y comerciales mejorados en la etapa temprana del desarrollo de medicamentos durante los ensayos clínicos.
En opinión de Freyr, el ILAP ofrece grandes oportunidades para los desarrolladores de tratamientos innovadores, especialmente para aquellos que abordan necesidades no cubiertas de los pacientes. Por una tarifa relativamente modesta (aproximadamente £8000), una empresa podría obtener asesoramiento en las primeras etapas, conseguir una designación para su producto y acordar un perfil de desarrollo objetivo. Esto tiene el potencial de ahorrar una cantidad significativa de tiempo del ciclo de vida general del desarrollo del producto. También hay beneficios al mirar más allá de la autorización de comercialización y hacer preparativos tempranos para las negociaciones sobre el reembolso.
El ILAP se compara favorablemente con esquemas similares ofrecidos dentro de la red europea de medicamentos (como el PRIME). Aunque diferente en concepto y ejecución, el ILAP tiene criterios de aceptación más amplios y una tasa de aceptación más alta. El ILAP también proporciona una vía para la integración con el Project Orbis de la Administración de Alimentos y Medicamentos de los Estados Unidos (USFDA) para productos oncológicos emergentes.
¿Cómo solicitar el ILAP?
Para acceder al ILAP, los solicitantes deben solicitar un Pasaporte de Innovación (IP). Obtener una designación de IP permite a los desarrolladores de medicamentos acceder a la vía basándose en la evidencia requerida para que un producto cumpla con los criterios de elegibilidad definidos por NICE, SMC, AWTTC y la MHRA.
Esta designación actúa como catalizador para productos innovadores desde la fase preclínica hasta la fase intermedia de desarrollo. La PI puede llevar a la definición de un documento de Perfil de Desarrollo Objetivo (TDP). El TDP es una hoja de ruta que facilita el acceso a los socios de ILAP en las primeras etapas del ciclo de vida del desarrollo de fármacos para acelerar y agilizar el acceso de los pacientes a tratamientos nuevos e innovadores. Los pacientes forman parte de todo este proceso. Varias herramientas proporcionadas por el ILAP apoyan a los solicitantes en todas las etapas del proceso de diseño, desarrollo y aprobación.
Criterios de designación de pasaporte innovador
La guía de la MHRA establece los criterios para una designación de IP. Esto es especialmente relevante para productos innovadores y también se compara favorablemente con esquemas equivalentes ofrecidos en Europa.
En el futuro, la aplicabilidad específica de la IP para Dispositivos Médicos y productos combinados, áreas en las que siempre hay una innovación significativa, puede resultar beneficiosa.
La designación de IP es evaluada por los socios permanentes y de apoyo según los siguientes criterios:
- Criterio 1: Detalles de la condición, el paciente o el área de salud pública
- Para afecciones graves o que ponen en peligro la vida
- En un caso donde la necesidad es crucial para los pacientes
- Criterio 2: El medicamento cumple una o más áreas específicas que incluyen
- Medicina innovadora
- Medicamento asociado a una nueva indicación
- Medicamento para enfermedades raras
- Medicamento en desarrollo con el objetivo de la salud pública del Reino Unido
- Criterio 3: El medicamento tiene el potencial de ofrecer
- Un breve informe sobre cómo el medicamento o la indicación propuestos beneficiarán a los pacientes.
- Se fomentan las opiniones de los pacientes o de las organizaciones de pacientes.
Al presentar la Solicitud de IP, se lleva a cabo una reunión entre los solicitantes y la MHRA para determinar si el producto cumple con los tres (03) criterios.
Según la última información de enero de 2022, la MHRA ha recibido setenta y una (71) solicitudes, de las cuales cuarenta y una (41) resultaron en la designación IP, veintidós (22) están en proceso y siete (07) solicitudes han sido denegadas.
El momento adecuado para entrar en el ILAP se menciona a continuación.
- En la etapa temprana a intermedia de desarrollo del producto.
- Cuando los datos relevantes estén disponibles
- Cuando los solicitantes sienten la necesidad de obtener aportaciones de las partes interesadas.
- Los solicitantes aspiran a adoptar nuevos enfoques innovadores
- No cuando el producto se encuentra en las etapas finales de desarrollo.
Panorama general del desarrollo de medicamentos
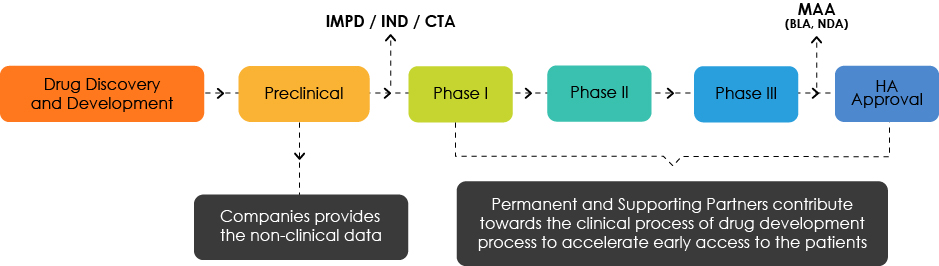
Comprender el perfil de desarrollo objetivo (TDP)
Los expertos de TDP analizan las características del producto y destacan las deficiencias desde un punto de vista reglamentario. Son responsables de orientar a los desarrolladores de medicamentos hacia una hoja de ruta que proporcione un acceso temprano de los pacientes a sus productos.
El TDP es un documento que se actualiza en tiempo real según los requisitos alineados con el desarrollo del producto. Por lo tanto, un producto experimenta múltiples modificaciones del TDP a medida que se generan nuevos datos.
La accesibilidad de los pacientes a medicamentos esenciales puede verse comprometida por los retrasos en el mercado. Para evitar tales escenarios, las vías aceleradas funcionan como un catalizador. El ILAP es un ejemplo de vía de autorización flexible que es bien aceptada en toda la industria y puede acelerar el cronograma de desarrollo de medicamentos innovadores. Los criterios detallados definidos por el Sistema de Salud del Reino Unido permiten a los solicitantes explorar su elegibilidad para solicitar la designación IP. Incentivar las necesidades clínicas y de los pacientes no satisfechas con vías aceleradas como el ILAP facilita la entrada al mercado y puede proporcionar alivio a las poblaciones de pacientes en riesgo. Para salvaguardar el interés de los pacientes, las Autoridades Sanitarias no comprometen la seguridad, eficacia o calidad del producto, al tiempo que garantizan un proceso de aprobación acelerado. Los servicios reglamentarios End-to-End de Freyr facilitan el proceso de documentación para apoyar la designación de Pasaporte Innovador en un tiempo acelerado, ayudando a que sus productos lleguen a los pacientes antes. Contacte con Freyr.










