
El mundo de las regulaciones farmacéuticas está a punto de recibir una importante actualización con la implementación de eCTD 4.0. Este formato estandarizado promete un camino más sencillo para las solicitudes de nuevos medicamentos presentadas a los organismos reglamentarios. Pero para las empresas que buscan una parte del mercado farmacéutico japonés de 141.5 mil millones de dólares, hay un giro crucial: ¡Japón está acelerando el cronograma de adopción!
A continuación, se presenta un análisis de estos puntos destacados:
- Adopción obligatoria: A diferencia de otras áreas que tienen fases voluntarias antes de la adopción obligatoria, Japón tiene como objetivo hacer obligatorio el uso de eCTD 4.0 para 2026.
- La Preparación es Clave: La preparación es clave debido a las limitaciones de tiempo y la ausencia de una ruta de migración directa del formato JP1.0 de la PMDA de Japón a eCTD 4.0; centrarse en un sistema mejor ayudará a las empresas farmacéuticas en Japón durante el proceso de transición. Estos pasos incluyen la actualización de software, la capacitación del personal y la preparación de PDFs para el nuevo formato.
- Recursos disponibles: La Agencia Japonesa de Productos Farmacéuticos y Dispositivos Médicos (PMDA) ha publicado recursos que pueden guiar a las empresas a través de este cambio, como la "Guía de Implementación del Documento Técnico Común Electrónico ICH eCTD 4.0", con explicaciones sobre los cambios realizados y las mejores prácticas disponibles.
Estas son algunas razones por las que no debería perderse este juego de números:
- Vía rápida hacia eCTD 4.0: A diferencia de otras regiones donde el proceso es por fases, Japón tiene como objetivo una adopción obligatoria de eCTD 4.0 tan pronto como en 2026. ¡Esto es tres años antes de la fecha límite establecida por la FDA de US para 2029! Con un cronograma tan ambicioso, significa que Japón ha tomado la delantera en cuanto a la incorporación global de eCTD.
- No hay Margen de Error: JP no pudo convertirse directamente a eCTD 4.0 a diferencia de sus versiones anteriores. Esto significa que las empresas farmacéuticas deben estar especialmente preparadas para esto para evitar retrasos en la presentación que podrían costarles millones en ingresos.
- Apoyo para una entrada exitosa: La Agencia Japonesa de Productos Farmacéuticos y Dispositivos Médicos (PMDA) comprende los desafíos. Han desarrollado recursos como guías de implementación diseñadas para guiar a las empresas a través de estas modificaciones con facilidad y asegurar una buena entrada en el mercado japonés. (https://www.pmda.go.jp/english/).
Si está desarrollando medicamentos para el enorme mercado japonés, ¡es hora de ponerse manos a la obra! Aquí tiene su lista de verificación previa al vuelo:
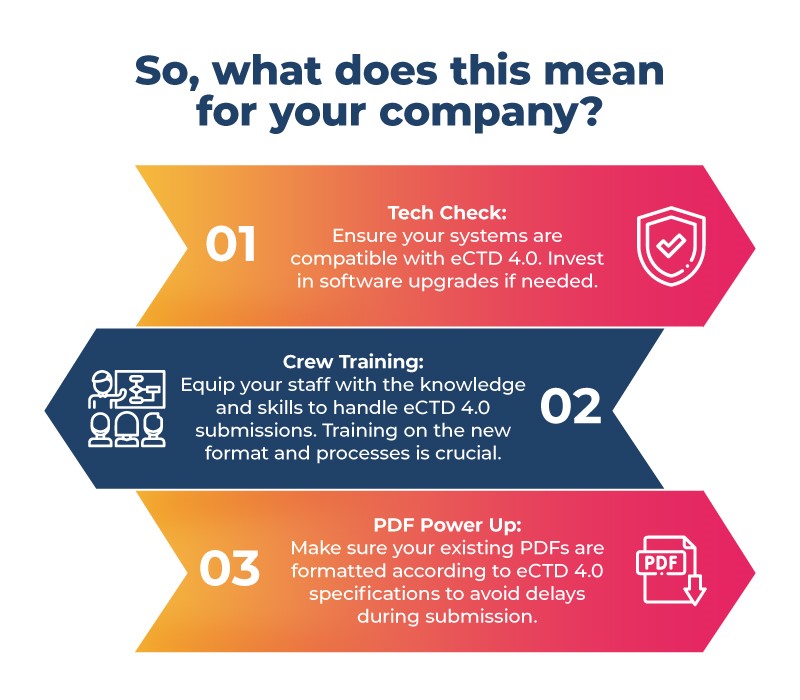
La transición a eCTD 4.0 promete una mayor eficiencia y estandarización global en todo el proceso de aprobación de medicamentos farmacéuticos. Su empresa puede anticipar este cambio en Japón para una transición fluida y aprovechar las innumerables oportunidades que ofrece esta nueva era. Recuerde que no prepararse es prepararse para fracasar, así que esté listo para prosperar con eCTD 4.0 en Japón.
Los beneficios y oportunidades obtenidos son atractivos para la industria farmacéutica. Sin embargo, presenta su propia cuota de dificultades en el camino que deben resolverse. Para navegar sin problemas a través de un entorno reglamentario en constante cambio, las empresas pueden buscar asociaciones con consultores confiables como Freyr. Adopte el futuro de las presentaciones reglamentarias en Japón con nuestro software eCTD inigualable, Freyr SUBMIT PRO, que cumple con los estándares 21 CFR Part 11 y tiene un modelo de implementación flexible. Contáctenos hoy para obtener más información y emprender un camino hacia una mayor eficiencia y éxito. Solicite una demostración hoy.









