
¡Hola, estimados profesionales reglamentarios! Como miembro de la industria de las ciencias de la vida, es probable que esté familiarizado con el formato de envío del Documento Técnico Común Electrónico (eCTD) que está revolucionando la industria reglamentaria de las ciencias de la vida. Su estructura estandarizada es un verdadero elemento transformador. Con este blog, nuestro objetivo es proporcionar información valiosa sobre las mejores prácticas para los envíos eCTD. ¡Así que, preparémonos para convertirnos juntos en expertos en envíos eCTD!
Presentaciones eCTD y mejores prácticas
Para garantizar una presentación eCTD exitosa, es esencial cumplir con los requisitos reglamentarios y seguir las mejores prácticas, como se muestra en la imagen siguiente:
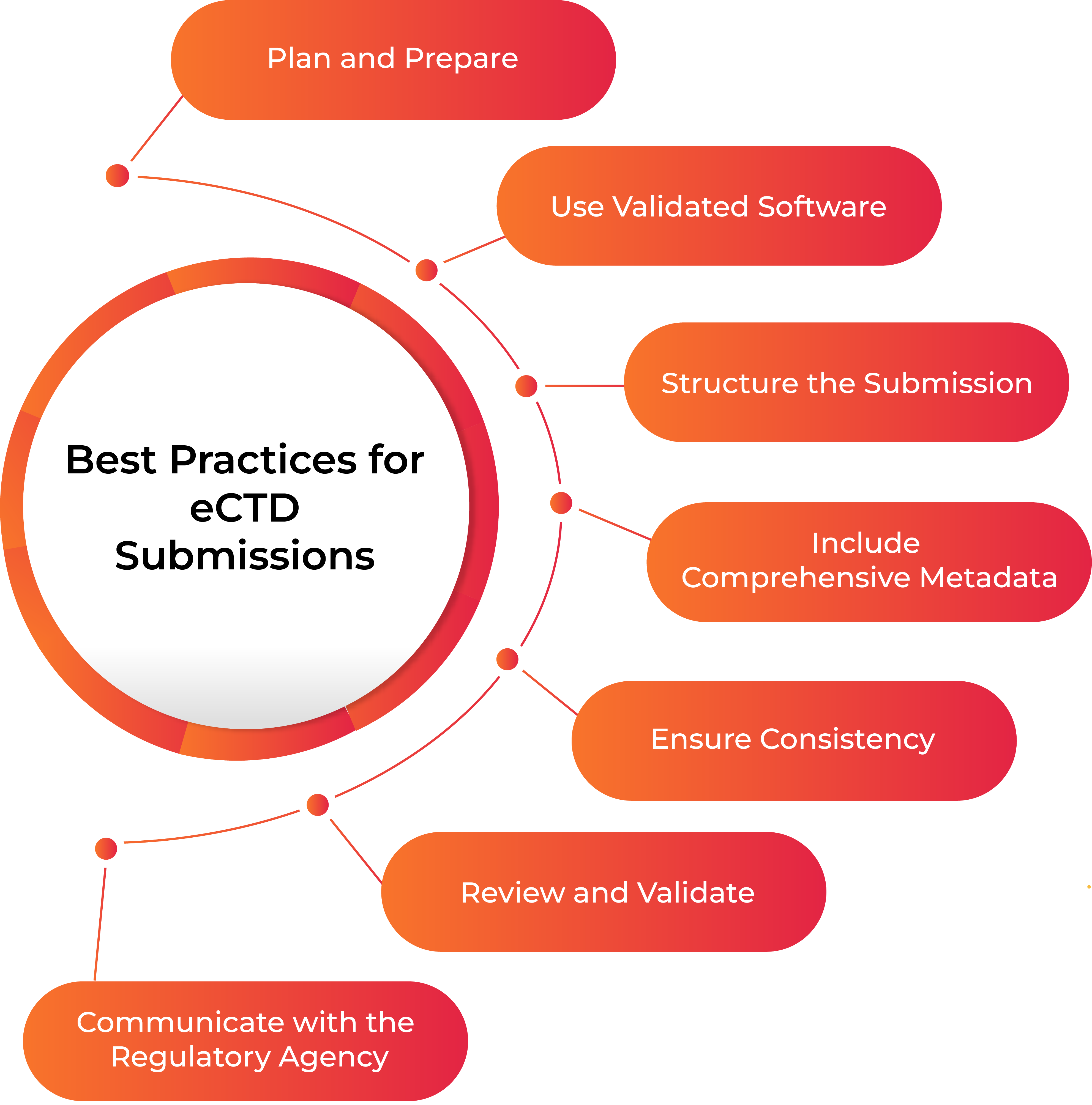
Planificar y Preparar
Desarrollar un plan detallado es el primer paso hacia una presentación eCTD exitosa. El plan debe incluir un cronograma, hitos y responsabilidades para cada miembro del equipo involucrado en el proceso de presentación. Se debe asignar tiempo suficiente para la revisión y aprobación del paquete de presentación. Todos los documentos requeridos deben prepararse y organizarse según las directrices reglamentarias aplicables.
Utilice Software Validado
El software de presentación eCTD debe ser validado para asegurar que cumple con los requisitos reglamentarios. El software debe ser capaz de generar presentaciones eCTD sin errores y bien estructuradas. Además, el software debe actualizarse con frecuencia para alinearse con los últimos requisitos reglamentarios.
Estructurar la presentación.
Una presentación eCTD bien estructurada facilita una revisión reglamentaria eficiente. La presentación debe estructurarse de acuerdo con las especificaciones eCTD del Consejo Internacional de Armonización (ICH) y las especificaciones regionales del Módulo 1. Cada presentación debe tener una estructura de carpetas claramente definida y consistente en todo el paquete de presentación.
Incluir Metadata Completa
La Metadata proporciona información adicional sobre los documentos en el paquete de presentación. Incluye el autor, el número de versión y la fecha de presentación. Una Metadata completa facilita la gestión de documentos y permite a las Agencias Reglamentarias rastrear los cambios y garantizar la integridad de los datos.
Asegurar la coherencia
La coherencia es esencial para una presentación eCTD exitosa. Todos los documentos deben ser coherentes en cuanto a contenido, formato y Metadata. La coherencia garantiza que la presentación sea fácil de navegar y minimiza la posibilidad de errores durante la revisión reglamentaria.
Revisar y Validar
Antes de presentar el paquete eCTD, es esencial revisar y validar la presentación para verificar su exhaustividad y precisión. Una revisión exhaustiva garantiza que todos los documentos requeridos están incluidos y que no hay errores ni discrepancias. La validación asegura que la presentación cumple con las especificaciones del eCTD y los requisitos reglamentarios.
Comuníquese con la Agencia Reglamentaria
Las agencias reglamentarias proporcionan directrices y comentarios sobre las presentaciones eCTD. Es importante aclarar las dudas o preocupaciones planteadas por las autoridades sanitarias antes de enviar el paquete. También es esencial responder con prontitud a las consultas que la agencia reglamentaria plantee durante el proceso de revisión.
En conclusión, seguir las mejores prácticas es fundamental para las presentaciones eCTD. Al hacerlo, puede asegurar un proceso de presentación fluido, optimizado y exitoso que cumpla con todos los requisitos normativos y acelere el proceso de revisión.
Integre Freyr SUBMIT PRO y cumpla con todos sus requisitos de presentación eCTD. La herramienta eCTD está totalmente equipada con funciones personalizadas y únicas que hacen que el proceso sea más fluido y eficiente.
¡Diga adiós a las presentaciones estresantes y hola a las presentaciones reglamentarias sin estrés con Freyr SUBMIT PRO!
Solicite una demostración hoy mismo!









