
El mercado farmacéutico de Malasia es un centro en expansión en el sudeste asiático que ofrece importantes oportunidades a las empresas internacionales. Gracias al aumento de la demanda de una asistencia sanitaria de calidad y a un marco normativo cada vez más estructurado, el mercado farmacéutico de Malasia se está convirtiendo en un destino atractivo tanto para los fabricantes de medicamentos genéricos como para los de medicamentos innovadores.
Panorama general del mercado de Malasia: un panorama prometedor en el mercado farmacéutico de Malasia
Tanto los medicamentos genéricos como las nuevas entidades químicas (NCE) tienen buenas perspectivas en el mercado farmacéutico de Malasia, un sector en rápido desarrollo en el sudeste asiático. El país ofrece un entorno dinámico para las empresas farmacéuticas debido al crecimiento de su población y al aumento de la demanda de atención sanitaria. El sector sanitario es un mercado lucrativo para los productos farmacéuticos, ya que está bien consolidado y cuenta con instalaciones médicas de primer nivel.
El mercado farmacéutico de Malasia se caracteriza por una creciente demanda de medicamentos novedosos, especialmente en áreas terapéuticas como la diabetes, las enfermedades cardiovasculares y la oncología. El entorno regulatorio se ha vuelto más organizado, con normas precisas para la aprobación de productos y la entrada en el mercado, mientras que el gobierno sigue centrándose en mejorar la sanidad pública y el acceso a los medicamentos.
Proceso de registro en Malasia:
El proceso de registro de productos farmacéuticos en Malasia está regulado por la Agencia Nacional de Regulación Farmacéutica ( NPRA), que se encarga de garantizar la seguridad, la eficacia y la calidad de los productos farmacéuticos.
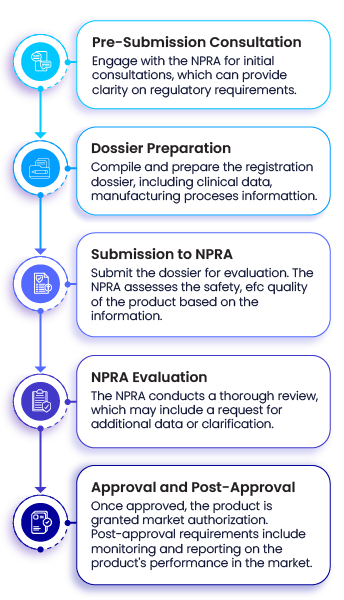
NPRA para el registro de productos farmacéuticos se ajustan a las directrices y recomendaciones en materia de calidad, seguridad y eficacia de la Organización Mundial de la Salud (WHO) o a otras normas aceptadas internacionalmente, como las de la Conferencia Internacional sobre Armonización (ICH). Las etapas clave del proceso de registro son las siguientes:
Requisitos reglamentarios básicos:
Para que un producto farmacéutico pueda registrarse en Malasia, debe cumplir varias condiciones reglamentarias importantes:
- Buenas prácticas de fabricación (BPF): Para garantizar que el producto cumple los requisitos de calidad, las instalaciones de fabricación deben estar acreditadas por las autoridades PIC/S .
- Datos clínicos: Para demostrar su seguridad y eficacia, los nuevos compuestos activos (NCE) necesitan datos de ensayos clínicos. En el caso de los medicamentos genéricos, debe demostrarse su bioequivalencia.
- Etiquetado y envasado: A la hora de etiquetar los productos, deben respetarse las leyes locales, especialmente en lo que se refiere al idioma y a la información de seguridad.
- Ficha técnica del producto: Es necesario incluir una descripción detallada de los ingredientes del producto, la posología y las instrucciones de uso.
- Representación local: Por lo general, un agente o representante local debe actuar como punto de contacto NPRA. El solicitante del registro del producto, conocido como «titular del registro del producto» (PRH), debe ser una empresa constituida localmente, una sociedad o una persona jurídica, con domicilio social y registrada en la Comisión de Sociedades de Malasia (SSM) (cuyo objeto social esté relacionado con productos sanitarios o farmacéuticos).
Caso práctico de Freyr: apoyo a una empresa farmacéutica con sede en Taiwán en su entrada en el mercado:
Perfil del cliente: Una empresa farmacéutica líder con sede en Taiwán solicitó a Freyr asistencia end-to-end para lanzar al mercado farmacéutico de Malasia tanto NCE genéricos como NCE . Su objetivo era garantizar una entrada oportuna en el mercado y, al mismo tiempo, superar las complejidades normativas.
Detalles del proyecto: El encargo de Freyr abarca una amplia gama de servicios normativos:
- Estrategia y enfoque normativo: Para el lanzamiento del producto en Malasia se desarrolló una estrategia que cumple con NPRA y se adapta a las necesidades del cliente.
- Revisión técnica y análisis de deficiencias: Se llevó a cabo un examen exhaustivo de los documentos de registro con el fin de detectar posibles deficiencias y garantizar que cumplieran con los requisitos NPRA.
- Recopilación y presentación: Me aseguré de que toda la documentación necesaria estuviera completa y cumpliera con las normas reglamentarias antes de recopilar y presentar el expediente de registro ante NPRA.
- Seguimiento con NPRA: Supervisé la correspondencia continua con NPRA resolver cualquier duda o solicitud adicional, agilizando así el procedimiento de aprobación.
Resultado: Con la ayuda de Freyr, el cliente logró completar con éxito el proceso de registro en Malasia. Los productos se aprobaron rápidamente, lo que permitió una entrada fluida en el mercado, subsanando cualquier deficiencia técnica y garantizando la presentación de la documentación adecuada. Este caso puso de relieve la solidez de Freyr en Asuntos Regulatorios su capacidad para orientarse con eficacia en el mercado farmacéutico de Malasia.
El cliente pudo centrarse en sus actividades principales gracias al end-to-end de Freyr, que garantizó que todo el proceso regulatorio —desde la preparación del expediente hasta la aprobación final— se desarrollara sin contratiempos.
¿Estás listo para entrar en el próspero mercado farmacéutico de Malasia?
El mercado farmacéutico de Malasia ofrece un enorme potencial de crecimiento. Sin embargo, para desenvolverse en el marco normativo se requiere una estrategia bien estructurada, una documentación precisa y un conocimiento profundo del mercado local.
Al asociarse con proveedores de servicios normativos con amplia experiencia, como Freyr, las empresas farmacéuticas pueden agilizar su entrada en el mercado farmacéutico de Malasia, subsanar las deficiencias técnicas y obtener autorizaciones más rápidamente, lo que les abre nuevas oportunidades en esta dinámica región.










