Los costos de cumplimiento para las empresas farmacéuticas pueden representar hasta el 25% de sus gastos operativos totales. Las empresas farmacéuticas con múltiples carteras de productos se enfrentan a desafíos únicos en la gestión del cumplimiento global, el seguimiento de las presentaciones de expedientes y la supervisión de las variaciones de etiquetado. La complejidad de los requisitos reglamentarios en las diferentes regiones, junto con el manejo manual de grandes volúmenes de datos, puede conducir al incumplimiento, retrasos en las aprobaciones de mercado e ineficiencias operativas.
Este blog explora los desafíos clave que enfrentan las empresas farmacéuticas al gestionar múltiples carteras de productos y demuestra cómo el software reglamentario, respaldado por estudios de caso reales, ofrece una solución estratégica a estos problemas.
Desafíos clave en la gestión de múltiples carteras de productos
- Requisitos de Cumplimiento Globales Complejos: Cada país tiene su propio organismo regulador, y sus requisitos pueden variar drásticamente. Por ejemplo, la US FDA, la EMA y la PMDA de Japón tienen diferentes formatos de presentación, plazos y estándares de cumplimiento. Las empresas farmacéuticas deben gestionar diversos expedientes en múltiples regiones, asegurando al mismo tiempo que no haya desviaciones de las regulaciones locales.
- Seguimiento de las variaciones de etiquetado entre regiones: Gestionar las variaciones de etiquetado para diferentes regiones y asegurar actualizaciones oportunas es uno de los aspectos más desafiantes de la gestión de cartera. Una mala gestión de los cambios en el etiquetado puede llevar a incumplimientos, retiradas de productos y grandes reveses financieros.
- Sobrecarga en la presentación de expedientes: Presentar y gestionar expedientes de múltiples líneas de productos, cada una en diferentes etapas de desarrollo, puede abrumar rápidamente a los equipos internos. Gestionar manualmente las actualizaciones del ciclo de vida del producto a menudo conduce a errores y retrasos en las aprobaciones.
- Mala gestión de recursos: Los equipos a menudo tienen dificultades para asignar los recursos adecuados de manera eficiente. Sin un sistema de gestión sólido, las empresas pueden sobrecargar al personal con tareas administrativas, limitando su capacidad para centrarse en actividades estratégicas clave.
- Silos de datos: La falta de centralización implica que los datos relacionados con las presentaciones, aprobaciones y actualizaciones de productos se almacenan en sistemas dispares, lo que provoca ineficiencias, falta de comunicación y dificultad para mantener una visión integral del ciclo de vida del producto.
La suite de productos tecnológicos de Freyr Digital apoya a las empresas farmacéuticas desde el concepto hasta la comercialización, como se muestra en la imagen a continuación.
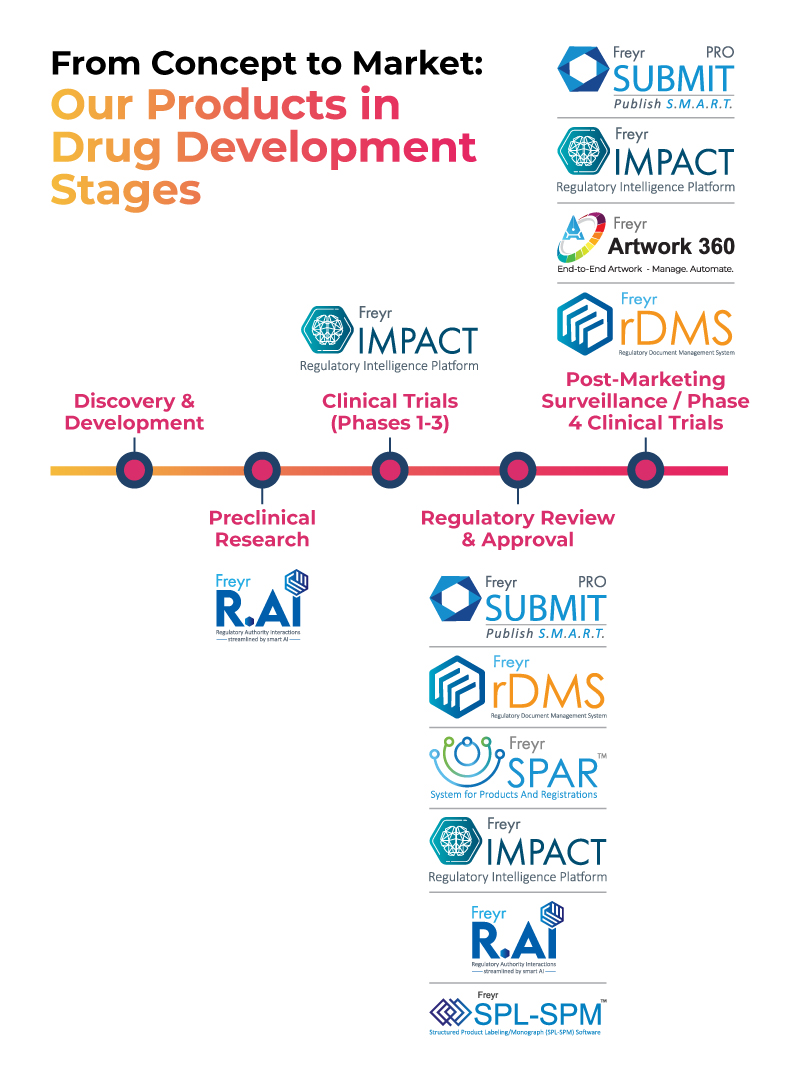
Casos de estudio: Cómo el software reglamentario proporciona una ventaja estratégica
Al adoptar software reglamentario, las empresas farmacéuticas pueden automatizar procesos, garantizar el cumplimiento y, en última instancia, obtener una ventaja estratégica sobre sus competidores. Los siguientes casos de estudio destacan ejemplos reales de cómo nuestras soluciones de software reglamentario han ayudado a las empresas farmacéuticas a superar estos desafíos.
Caso demostrado
Desafío del cliente
Una empresa farmacéutica genérica con sede en US tenía dificultades para gestionar de manera eficiente sus presentaciones reglamentarias End-to-End y la gestión de documentos. Se enfrentaron a desafíos con repositorios de documentos dispersos, lo que dificultaba el acceso sin interrupciones a los documentos reglamentarios tanto para las partes interesadas internas como externas. Además, el proceso de creación y gestión de Structured Product Labeling (SPL) era engorroso, lo que provocaba retrasos en los plazos de presentación y un aumento de los ciclos de revisión.
Solución de Freyr Digital
Freyr Digital intervino como proveedor de soluciones virtuales de Asuntos Regulatorios, implementando estos tres productos clave como soluciones para abordar los desafíos del cliente:
- Freyr rDMS: Un sistema centralizado de gestión documental que actúa como fuente única de verdad para todas las presentaciones y documentos reglamentarios, garantizando el acceso en tiempo real y el control de versiones tanto para los equipos internos como para los socios externos.
- Freyr SUBMIT PRO: Una potente herramienta para la publicación y presentación eCTD, que agiliza el proceso de presentación, reduce el tiempo de preparación y garantiza el cumplimiento de las normas reglamentarias en evolución.
- Freyr SPL-SPM: Una solución eficiente para gestionar todas las actividades relacionadas con SPL, mejorando significativamente los procesos de creación, gestión y presentación de documentos.
Resultados
Al implementar estas soluciones, Freyr Digital ayudó al cliente a lograr:
- Una reducción del 30% en el tiempo de preparación de la presentación
- Cumplimiento del 100% con todos los requisitos reglamentarios
- Una mejora del 40% en la eficiencia del procesamiento de documentos
- Una reducción del 25% en los ciclos de revisión
Conclusión: Adoptando la transformación digital para el éxito estratégico
Gestionar múltiples carteras de productos en mercados globales no es tarea fácil. Sin embargo, con el software reglamentario adecuado, las empresas farmacéuticas pueden optimizar los procesos, garantizar el cumplimiento y obtener una ventaja estratégica en la industria.
El conjunto de herramientas reglamentarias de Freyr Digital —que incluye Freyr SUBMIT PRO, Freyr rDMS y Freyr SPL-SPM— ha ayudado constantemente a las empresas farmacéuticas a reducir los tiempos de presentación, a mejorar el cumplimiento y a optimizar los recursos. Al automatizar los procesos manuales, al proporcionar una gestión de datos centralizada y al ofrecer información en tiempo real, nuestras soluciones permiten a las empresas farmacéuticas mantenerse a la vanguardia en un mercado competitivo. Contáctanos.









