
La publicidad de medicamentos dirigida directamente al consumidor (DTC) se ha convertido en un tema de discusión recurrente en los últimos años. Estos anuncios, que están dirigidos a los consumidores en lugar de a los profesionales de la salud, se les ha atribuido el aumento de la concienciación de los pacientes y la demanda de ciertos medicamentos. Sin embargo, también han sido criticados por poder conducir a un sobrediagnóstico y un sobretratamiento.
Participando en la actual carrera de tendencias dentro de las empresas farmacéuticas, se sabe que el gasto total en marketing es mayor que su presupuesto de investigación. A nivel mundial, se gastaron 1.42 billones de dólares en marketing. En los US, se gastaron 486.62 mil millones de dólares en 2021 para comercializar medicamentos a médicos; en Canadá, se gastaron 29,305.1 millones de dólares en 2022. Al desglosar estas cifras, el 56% correspondió a muestras gratuitas, el 25% a la "promoción detallada" (promoción directa de medicamentos) a médicos por parte de representantes de ventas farmacéuticas, el 12.5% a publicidad directa al usuario, el 4% a la promoción detallada en hospitales y el 2% a anuncios en revistas2. A veces, las prácticas de marketing negativas pueden afectar tanto a los pacientes como a la profesión sanitaria.
Tipos de actividades de promoción de medicamentos
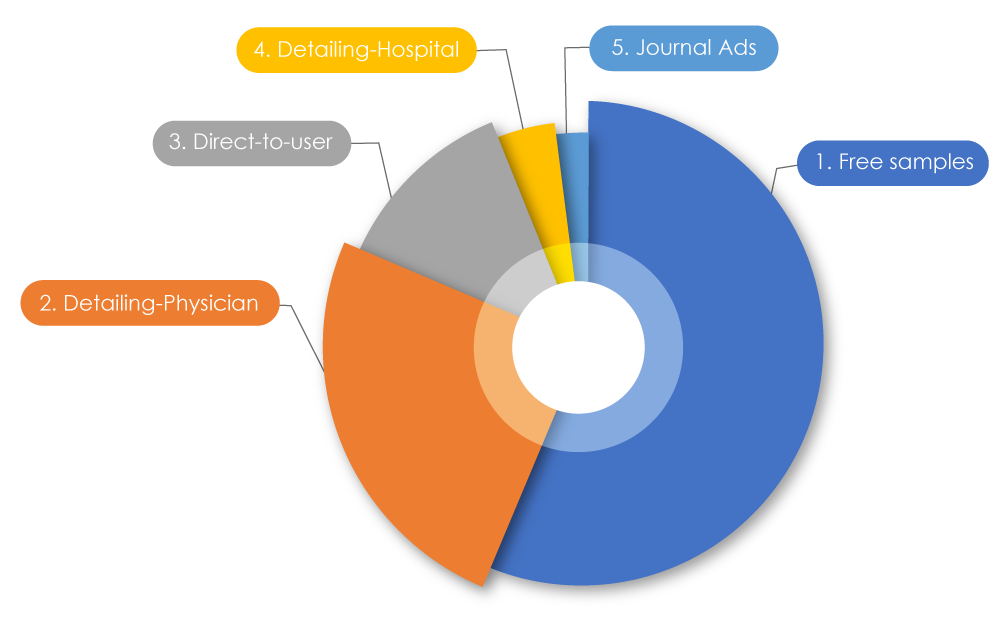
Fuente: Pharmaceutical marketing - Wikiwand
Publicidad farmacéutica dirigida al público en general
Se imponen restricciones a la publicidad de medicamentos de venta con receta al público en general, también conocida comúnmente como publicidad directa al consumidor (DTC). Para promocionar medicamentos de venta con receta al público, la comunicación debe cumplir ciertos requisitos fundamentales:
- La coherencia en la etiqueta de la publicidad y promoción de medicamentos de venta con receta se basa en el uso previsto para el cual el producto es aprobado por la FDA (el etiquetado del medicamento aprobado por la FDA). El etiquetado proporciona información sobre cómo usar el producto de manera segura y efectiva para la indicación aprobada. La publicidad y promoción que son inconsistentes con el etiquetado aprobado por la FDA se consideran promociones "fuera de etiqueta" ilegales.
- La promoción y publicidad de medicamentos con receta requieren un equilibrio justo entre los beneficios y riesgos del producto, asegurando que dicha información sea comparable en profundidad, detalle y contexto.
- Las reclamaciones deben estar respaldadas por pruebas suficientemente sólidas o experiencia clínica
- Veraz y no engañoso - Si la publicidad y promoción de medicamentos de prescripción son falsas o engañosas en algún aspecto, se considerará mal etiquetado según la Ley Federal de Alimentos, Medicamentos y Cosméticos (FDCA) y estará sujeto a aplicación de la ley.
- Uso de un lenguaje sencillo y accesible para el consumidor, evitando el lenguaje técnico, los términos científicos y la jerga médica en la publicidad y promoción dirigidas al consumidor. Debe cumplir con el etiquetado o la monografía aprobados del producto.
Información contenida en la publicidad farmacéutica dirigida al público en general
La publicidad y promoción de medicamentos recetados dirigidas al consumidor deben contener los siguientes elementos centrales, según lo exigen las regulaciones de la FDCA y la Administración de Alimentos y Medicamentos (FDA).
- Los nombres comerciales y establecidos deben ser según lo especificado en las reglamentaciones de la FDA
- Debe incluir la cantidad cuantitativa de ingredientes del medicamento anunciado.
- Debe incluir un “resumen breve” que divulgue cada efecto secundario, advertencia, precaución y contraindicación. Principalmente centrado en la información importante sobre riesgos en lugar de una lista exhaustiva de riesgos relacionados con el producto. La mayoría de los riesgos se presentan de una manera que es más probable que los consumidores entiendan.
- Los principales riesgos del producto deben presentarse de forma clara, visible y neutral como una “declaración principal”
- Las declaraciones de divulgación de eventos adversos para anuncios DTC deben incluir la siguiente declaración de MedWatch impresa en texto visible: "Se le anima a notificar los efectos secundarios negativos de los medicamentos recetados a la FDA. Visite www.fda.gov/medwatch o llame al +1-800-FDA-1088"
- El etiquetado y la publicidad de recordatorio están exentos de los requisitos generales. Es importante destacar que el etiquetado y la publicidad de recordatorio no están permitidos para un medicamento de venta con receta que tenga una advertencia de recuadro negro en su etiquetado aprobado por la FDA.
Para Publicidad de Medicamentos DTC, Contáctenos
Para la publicidad de medicamentos DTC
Restricciones sobre las interacciones entre pacientes u organizaciones de pacientes y la industria
Las interacciones entre empresas farmacéuticas y pacientes/organizaciones de pacientes están permitidas solo en algunos países, como los Estados Unidos, pero con limitaciones, como:
- Debe estar según la etiqueta/CFL
- Equilibrado
- Adecuadamente justificado y
- Que no sea falso o engañoso de otro modo
Además, las interacciones con los clientes no deben implicar el Estatuto Anti-Soborno al inducir a organizaciones de pacientes o a los propios pacientes a recomendar o utilizar el producto anunciado.
En el Reino Unido, la publicidad de DTC al público está permitida para productos farmacéuticos, pero excluye a los niños. La publicidad de medicamentos de venta con receta al público está prohibida. Los anuncios deben incluir el nombre del producto y el nombre del principio activo. No se permiten muestras de productos ni vales que permitan a los consumidores obtener el producto de forma gratuita o a un precio excesivamente bajo.
En Alemania, la publicidad dirigida al público está permitida para productos farmacéuticos exclusivamente para niños menores de 14 años. La publicidad de medicamentos de venta con receta al público está prohibida. Pero también existen normas especiales para la publicidad de productos medicinales fuera de los círculos profesionales. Estas normas especiales se establecen principalmente en la Ley de Publicidad de Medicamentos (Heilmittelwerbegesetz, "HWG") y fueron modificadas por la Ley Alemana de Productos Farmacéuticos (Arzneimittelgesetz – "AMG") para estar en línea con la Directiva 2001/83/EC4.
Debatiendo la posibilidad de la publicidad de medicamentos en la era digital
Los defensores de la publicidad de medicamentos DTC argumentan que empodera a los pacientes al proporcionarles información sobre las opciones de tratamiento. También señalan que puede conducir a un aumento de la demanda de medicamentos, lo que puede ser beneficioso para las empresas farmacéuticas.
Por otro lado, los críticos de la publicidad de medicamentos DTC argumentan que puede conducir a un sobrediagnóstico y un sobretratamiento. Afirman que estos anuncios a menudo exageran los beneficios de los medicamentos mientras minimizan sus riesgos, lo que lleva a los pacientes a pedir a sus médicos medicamentos que quizás no necesiten. Además, señalan que puede provocar un aumento de los costos de atención médica, ya que a los pacientes se les pueden recetar medicamentos de marca más caros en lugar de alternativas genéricas más baratas.
A pesar del debate en curso, la publicidad de medicamentos DTC (directa al consumidor) llegó para quedarse. La FDA ha emitido directrices para este subtipo de publicidad, que incluyen requisitos para la divulgación de riesgos y un equilibrio justo entre beneficios y riesgos. En conclusión, la publicidad de medicamentos DTC tiene el potencial de educar a los pacientes y aumentar la demanda de ciertos medicamentos. Sin embargo, también es importante considerar los posibles inconvenientes y ser consciente de las limitaciones de la información proporcionada en estos anuncios. Como siempre, es importante consultar con su proveedor de atención médica antes de tomar cualquier medicamento. ¡Contacte a los expertos de Freyr para un cumplimiento End-to-End!










