
En el panorama altamente reglamentado de la industria de las ciencias de la vida, cumplir con las Directrices Específicas de Productos (DEP) es fundamental para el desarrollo y la aprobación exitosos de medicamentos. Las DEP son documentos exhaustivos emitidos por las Autoridades Sanitarias (AS) mundiales para proporcionar orientación para las aprobaciones de productos farmacéuticos dentro de categorías terapéuticas específicas.
Este blog detalla el propósito, la pertinencia y la perspectiva de la Autoridad Sanitaria sobre la emisión de PSG. En este documento se explica la lógica y las expectativas establecidas en los PSG que permiten el éxito estratégico de las empresas de ciencias de la vida.
Comprender las directrices específicas de productos y sus tipos
Los PSG desempeñan un papel fundamental en la configuración de la vía reglamentaria para los productos farmacéuticos. Al proporcionar orientación específica, las HAs garantizan la coherencia y evaluaciones sólidas de las solicitudes de productos dentro de categorías terapéuticas específicas. Al adherirse a los PSG, las empresas farmacéuticas pueden navegar por el complejo panorama reglamentario, asegurando que sus productos cumplan con los estándares de seguridad y eficacia requeridos.
Los PSGs no se limitan al desarrollo de medicamentos genéricos. También cubren una amplia gama de productos farmacéuticos, como los siguientes:
- Para medicamentos innovadores: Las PSG ofrecen orientación específica sobre estudios preclínicos, diseño de ensayos clínicos, evaluación de seguridad, farmacocinética y criterios de valoración de eficacia. Guían a las empresas sobre el tipo y la cantidad de datos necesarios para demostrar la seguridad y eficacia de sus medicamentos innovadores.
- Para biosimilares: Las PSG (Guías de Desarrollo de Productos) describen los requisitos de datos, los métodos analíticos y las consideraciones de diseño de estudios clínicos para productos biosimilares. Al seguirlas, las empresas de biosimilares pueden demostrar la similitud de sus productos con el biológico de referencia, lo que facilita su aprobación y acceso al mercado.
- Para productos biológicos: Estas directrices abordan aspectos críticos, como la fabricación, la caracterización y los estudios de comparabilidad, asegurando que los productos biológicos cumplan con los estándares aprobados.
Desarrollo de directrices y procesos específicos de productos
El desarrollo de las PSG es un esfuerzo colaborativo que involucra a las Autoridades Sanitarias (HAs), expertos científicos y a las partes interesadas de la industria. Las siguientes son las etapas de desarrollo de las PSG:
Etapa 1 - Evaluación exhaustiva del área terapéutica: Las AA identifican lagunas en las directrices existentes e inician el desarrollo de las PSG para abordar esas lagunas. Luego se involucra a expertos científicos y partes interesadas de la industria para que aporten su experiencia, asegurando que los borradores de las directrices se basen en pruebas y sean prácticos de implementar.
Etapa 2 - Consulta Pública: Los borradores de las PSG ya están disponibles para revisión y comentarios públicos. Este enfoque abierto y transparente permite a las partes interesadas, incluidos los profesionales de la salud (HCP), los grupos de pacientes y los representantes de la industria, proporcionar aportes valiosos y mejorar la calidad general y la relevancia de las directrices.
Etapa 3: Fase de Revisión Interna: Mientras los borradores de las PSG están en consulta pública, el equipo de desarrollo de las PSG dentro de las AA lleva a cabo una rigurosa revisión interna, asegurando que las directrices cumplen con los requisitos reglamentarios necesarios y se alinean con el marco reglamentario más amplio.
Etapa 4 - Finalización: Una vez finalizadas, las PSG se publican y se ponen a disposición de la industria, proporcionando una guía clara y práctica para el desarrollo y la presentación de productos.
Componentes de los PSGs
Las empresas de ciencias de la vida deben tener una comprensión clara de los componentes de los PSG. El siguiente gráfico circular los ilustra en detalle:
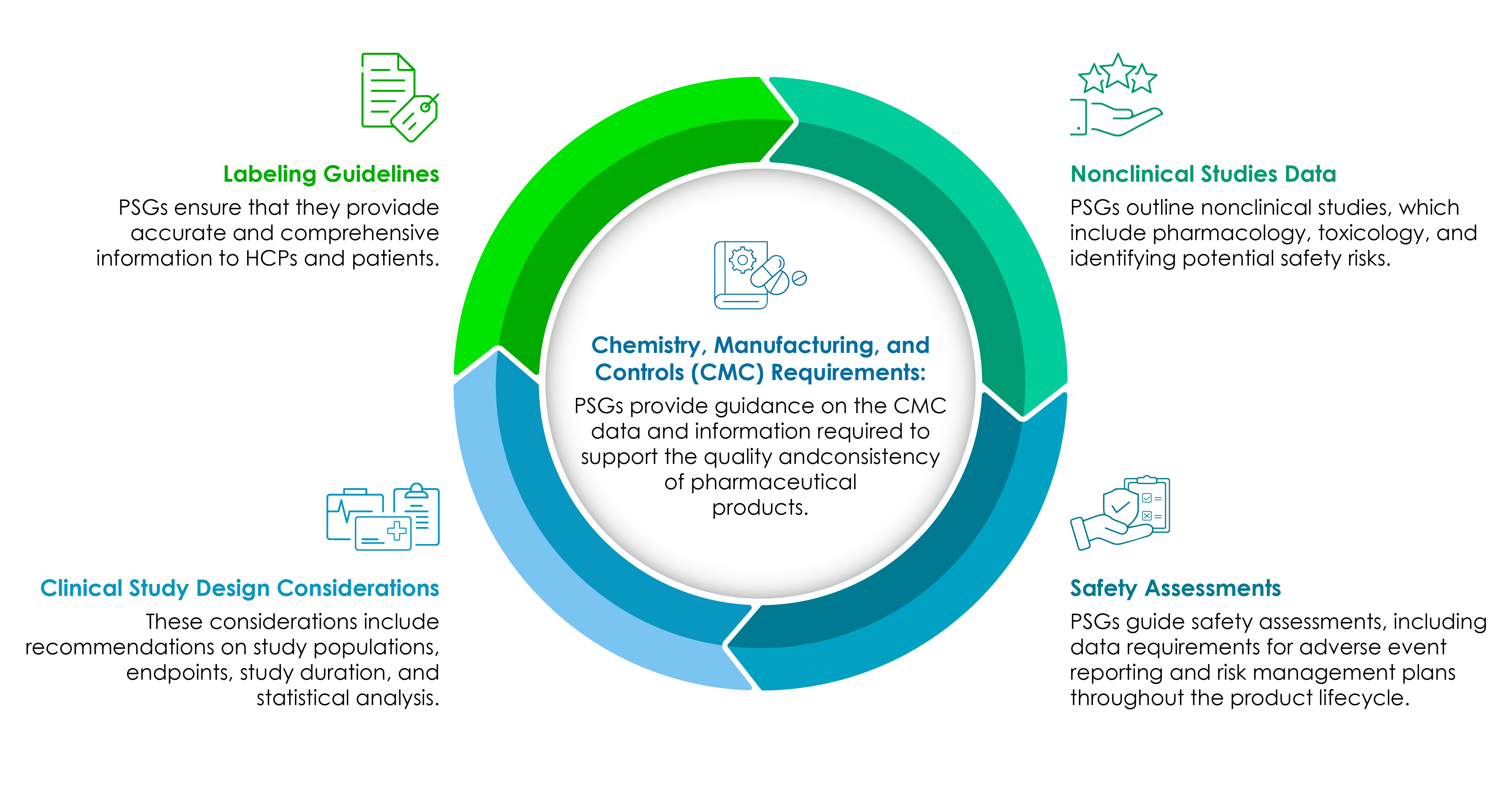
CMC sigue siendo el núcleo de cada desarrollo de productos farmacéuticos con enfoque reglamentario.
Cómo abordar los PSGs
Abordar los PSGs de manera conforme a la normativa se puede lograr mediante los siguientes puntos/estrategias enumerados:
- Interacción temprana con las autoridades sanitarias: Esta interacción fomenta un enfoque colaborativo y ayuda a abordar los posibles desafíos de forma proactiva.
- Experiencia científica: Aprovechar la experiencia de expertos garantiza que los diseños de los estudios, los métodos analíticos y las evaluaciones de seguridad se ajusten a los más altos estándares científicos.
- Consultores reglamentarios: Los consultores ofrecen orientación experta, asegurando el éxito de los planes de desarrollo y las presentaciones reglamentarias.
- Revisión exhaustiva de las PSG: Las empresas deben identificar las secciones específicas de las PSG aplicables a su producto y alinear sus planes de desarrollo en consecuencia.
- Monitoreo Continuo: Las PSG son documentos dinámicos que pueden sufrir actualizaciones o revisiones con frecuencia. Las empresas deben monitorear los cambios en las PSG para asegurar el cumplimiento reglamentario con los últimos requisitos de las PSG.
La orientación reglamentaria experta facilita la navegación por el PSG. ¡Consulte ahora!
Conclusión
Las Directrices específicas del producto (PSG) constituyen la base de las presentaciones reglamentarias para productos farmacéuticos dentro de categorías terapéuticas específicas. Comprender las perspectivas de la HA detrás de la emisión de las PSG es fundamental para las empresas de ciencias de la vida que buscan acelerar las aprobaciones, garantizar la calidad del producto y navegar por el panorama reglamentario global sin problemas.
Como proveedor líder de servicios reglamentarios, Freyr reconoce la importancia de adherirse a las mejores prácticas y aprovechar la experiencia que guiará a las empresas de ciencias de la vida para alinear sus estrategias de desarrollo de productos según los requisitos de PSG. Contáctenos hoy mismo para saber más sobre nuestros servicios y cómo podemos ayudarle a alcanzar sus objetivos.









