
Los productos combinados, que integran medicamentos, productos sanitarios y/o productos biológicos, han revolucionado la atención sanitaria al ofrecer soluciones terapéuticas innovadoras. Sin embargo, su naturaleza única presenta desafíos reglamentarios significativos. Esta guía completa explora el intrincado panorama de la regulación de productos combinados y proporciona estrategias para navegar con éxito por estas complejas vías.
Comprender los productos combinados y su marco reglamentario
Los productos combinados son productos médicos que combinan dos (2) o más componentes reglamentados —fármacos, dispositivos o productos biológicos— en una única entidad. Estos productos innovadores pueden adoptar diversas formas, como stents liberadores de fármacos, jeringas precargadas o parches transdérmicos. El marco reglamentario para los productos combinados se rige principalmente por la FDA en los Estados Unidos, con enfoques similares adoptados por organismos reglamentarios en todo el mundo.
La Oficina de Productos Combinados (OCP) de la FDA desempeña un papel crucial en la determinación del modo de acción principal (PMOA) de un producto combinado, lo que determina la vía reglamentaria y el centro principal de la FDA responsable de la revisión. El Centro de Evaluación e Investigación de Medicamentos (CDER), el Centro de Dispositivos y Salud Radiológica (CDRH) y el Centro de Evaluación e Investigación de Productos Biológicos (CBER) colaboran en el proceso de revisión, subrayando la necesidad de un enfoque integrado para garantizar la seguridad y eficacia de los productos combinados.
Determinación de la vía reglamentaria.
Uno de los pasos más importantes al desarrollar una estrategia reglamentaria para productos combinados es determinar la vía reglamentaria adecuada. Esta decisión se basa principalmente en el PMOA del producto. A continuación, se presentan consideraciones clave:
- Modo de Acción Principal (PMOA): Identificar el modo de acción único que proporciona la acción terapéutica más importante del producto combinado.
- Asignación del Centro Principal: Basándose en el PMOA, el producto se asignará a CDER, CDRH o CBER para una revisión principal.
- Tipo de presentación reglamentaria: Según el centro principal, la presentación puede adoptar la forma de una Solicitud de Nuevo Fármaco (NDA), una Solicitud de Licencia para Productos Biológicos (BLA) o una Aprobación Previa a la Comercialización (PMA).
- Solicitud de Designación (RFD): Si el PMOA no está claro, los patrocinadores pueden presentar una RFD a la OCP para una determinación formal.
- Pre-solicitud de designación (Pre-RFD): La OCP puede recibir una Pre-RFD para obtener comentarios informales y no vinculantes sobre cuestiones de clasificación y jurisdicción.
Comprender estos factores es crucial para desarrollar una estrategia reglamentaria eficaz adaptada a su producto combinado específico.
Cómo abordar los procesos de revisión previa a la comercialización
El proceso de revisión previa a la comercialización para productos combinados puede ser complejo, requiriendo una planificación y ejecución cuidadosas. Aquí hay estrategias clave para navegar este proceso de manera efectiva:
- Colaboración temprana con los organismos reguladores: Inicie conversaciones con la FDA al principio del proceso de desarrollo a través de reuniones previas a la presentación. Estas interacciones pueden proporcionar una orientación valiosa sobre los requisitos reglamentarios, los diseños de estudios y los posibles desafíos.
- Plan de desarrollo integral: Desarrolle un plan sólido que aborde los aspectos únicos de su producto combinado, incluyendo cómo interactúan las partes que lo componen y sus efectos combinados en la seguridad y la eficacia.
- Enfoque de Pruebas Integrado: Diseñar estudios preclínicos y clínicos que evalúen los componentes individuales y el producto combinado completo. Este enfoque debe evaluar las posibles interacciones y los efectos acumulativos.
- Consideraciones del Sistema de Calidad: Implemente un sistema de calidad que cumpla con las regulaciones de medicamentos (21 CFR 210/211) y Dispositivos Médicos (21 CFR 820) según corresponda a su producto.
- Ingeniería de Factores Humanos: Incorporar estudios de factores humanos para evaluar las interacciones del usuario con el producto combinado, garantizando un uso seguro y eficaz.
- Gestión de riesgos: Desarrollar un plan integral de gestión de riesgos que aborde los riesgos potenciales asociados con cada componente y su combinación.
Al adoptar estas estrategias, los patrocinadores pueden agilizar el proceso de revisión previa a la comercialización y aumentar la probabilidad de éxito reglamentario.
Abordar los desafíos post-comercialización
Las responsabilidades reglamentarias de los productos combinados se extienden más allá de la aprobación de comercialización. Una vigilancia poscomercialización eficaz y el cumplimiento son cruciales para el éxito a largo plazo. Considere las siguientes estrategias:
- Farmacovigilancia Integrada: Implementar un sistema de farmacovigilancia robusto que capture los eventos adversos relacionados con los componentes farmacéuticos y de dispositivo del producto combinado.
- Estudios post-comercialización: Planificar y llevar a cabo estudios post-comercialización para recopilar datos adicionales de seguridad y eficacia, especialmente para productos combinados novedosos.
- Mantenimiento del Sistema de Calidad: Actualice y mantenga continuamente su sistema de calidad para asegurar el cumplimiento con las regulaciones pertinentes para los componentes de medicamentos y dispositivos.
- Gestión de Cambios: Establecer un proceso sencillo para gestionar los cambios posteriores a la aprobación, considerando el impacto potencial en los aspectos del medicamento y del dispositivo del producto.
- Inteligencia Normativa: Manténgase informado sobre las regulaciones y los documentos guía en evolución relacionados con los productos combinados para asegurar el cumplimiento continuo.
Al abordar proactivamente estos desafíos poscomercialización, los fabricantes pueden mantener el cumplimiento reglamentario y la seguridad del producto durante todo su ciclo de vida.
Consideraciones Reglamentarias Mundiales
A medida que el mercado de productos combinados se expande globalmente, comprender los requisitos reglamentarios internacionales se vuelve cada vez más importante. Considere estas estrategias para el éxito reglamentario global:
- Armonización reglamentaria: Aprovechar los esfuerzos de armonización internacional, como los del Foro Internacional de Reguladores de Dispositivos Médicos (IMDRF), para agilizar las presentaciones reglamentarias globales.
- Requisitos Específicos del Mercado: Investigar y comprender los requisitos específicos para productos combinados en los mercados objetivo, ya que las regulaciones varían significativamente entre países.
- Presentaciones simultáneas: Considere las presentaciones simultáneas a múltiples agencias reglamentarias para acelerar el acceso al mercado global, cuando sea apropiado.
- Ensayos Clínicos Globales: Diseñar ensayos clínicos que cumplan con los requisitos de múltiples agencias reglamentarias para respaldar las solicitudes de comercialización global.
- Alianzas Internacionales: Colaborar con expertos o socios reglamentarios locales en mercados objetivo para navegar por las regulaciones específicas de cada país y las consideraciones culturales.
Al adoptar una perspectiva global en el desarrollo de estrategias reglamentarias, los fabricantes pueden ampliar su alcance en el mercado para productos combinados de manera más eficaz.
Conclusión
Navegar por las vías reglamentarias para productos combinados requiere una comprensión exhaustiva de los complejos marcos reglamentarios y una planificación estratégica.
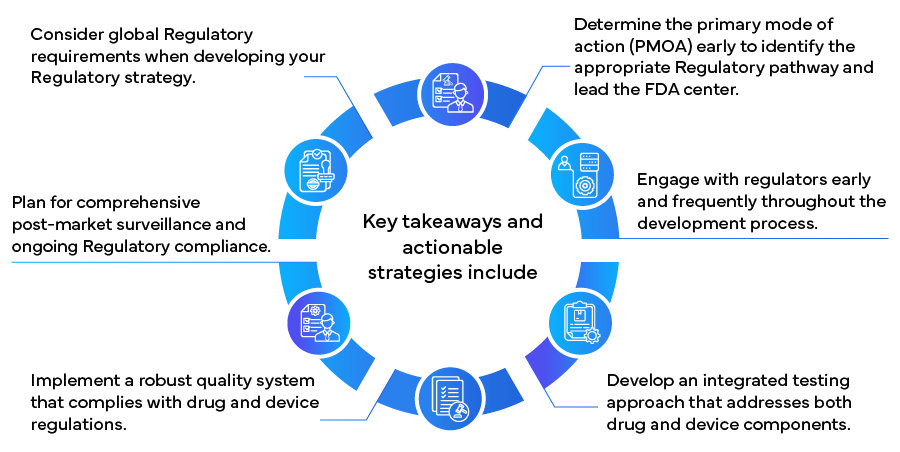
Al implementar estas estrategias, los fabricantes pueden navegar de manera más efectiva por el complejo panorama reglamentario de los productos combinados, lo que podría acelerar el tiempo de comercialización y garantizar el cumplimiento y el éxito a largo plazo. A medida que el campo de los productos combinados continúa evolucionando, mantenerse informado sobre los cambios reglamentarios y mantener la flexibilidad en los enfoques reglamentarios será crucial para el éxito continuo en este sector sanitario innovador y de rápido crecimiento.









