Mientras que los productos farmacéuticos innovadores o de marca conllevan costes adicionales asociados a la investigación y el desarrollo del producto, desde la etapa de identificación de la molécula hasta la autorización posterior a la comercialización, los productos farmacéuticos genéricos son relativamente rentables. Estas terapias no solo reducen el coste total del tratamiento, sino que también mejoran significativamente el acceso de los pacientes a productos farmacéuticos que salvan vidas. Dado que la dependencia de la importación de antibióticos genéricos y la terapia farmacológica para enfermedades raras afectó la disponibilidad de estos productos farmacéuticos a nivel mundial durante la pandemia, las agencias de salud están introduciendo nuevas directrices para apoyar a los fabricantes locales de fármacos.
Desde 1993, la organización comercial Medicines for Europe, antes conocida como European Generics Medicine Association (EGA), ha mantenido su objetivo de acercar terapias rentables a la población de pacientes europea. Durante la última década, han suministrado con éxito el 67% de todos los medicamentos a Europa, ampliando el acceso de los pacientes al 100% en siete (07) áreas terapéuticas clave. Dentro del ámbito de las autoridades sanitarias europeas, una “autonomía estratégica” posterior al Brexit puso en marcha la necesidad inmediata de remediar eficazmente la desventaja competitiva a la que se enfrentan los fabricantes europeos de genéricos y biosimilares. Con el advenimiento de la pandemia de COVID-19, las capacidades de la cadena de suministro global sucumbieron bajo la presión de la demanda de medicamentos. Medicamentos que salvan vidas y que aliviaban enfermedades crónicas desaparecieron de los estantes de las farmacias locales. Para superar los obstáculos en los productos farmacéuticos protegidos por patente y desarrollar la capacidad de fabricación local de medicamentos para mejorar el acceso de los pacientes, el Consejo de la UE adoptó un reglamento que establece una excepción para una molécula original al proporcionar un Certificado Complementario de Protección (SPC). Esta disposición facilita la fabricación de genéricos y biosimilares antes de la expiración de la patente con fines de almacenamiento o exportación. Sin embargo, la excepción será aplicable solo bajo las siguientes circunstancias.
- Los genéricos o biosimilares producidos son exclusivamente para exportación a otro país donde la patente de la molécula del fármaco no existe o ha expirado, o para fines de almacenamiento dentro del plazo restante de la patente de seis (06) meses.
- Según el requisito, el fabricante ha transmitido la información a la Autoridad Sanitaria local y al titular del SPC antes de los tres (03) meses.
- El fabricante ha informado a todas las partes interesadas relacionadas con la comercialización del producto.
- El fabricante ha asegurado que los requisitos de etiquetado establecen que el producto farmacéutico indica que es solo para fines de exportación.
De Hecho
Desde la concesión de la autorización de comercialización condicional para los productos de vacunas contra la COVID-19 en la UE, el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos ha autorizado cuatro (04) centros para la producción de vacunas en un año; dos (02) en Suiza y dos (02) en los EE. UU. Estas decisiones a favor de ampliar los centros de producción mejorarán las capacidades de fabricación de vacunas, haciéndolas más accesibles para la población europea.
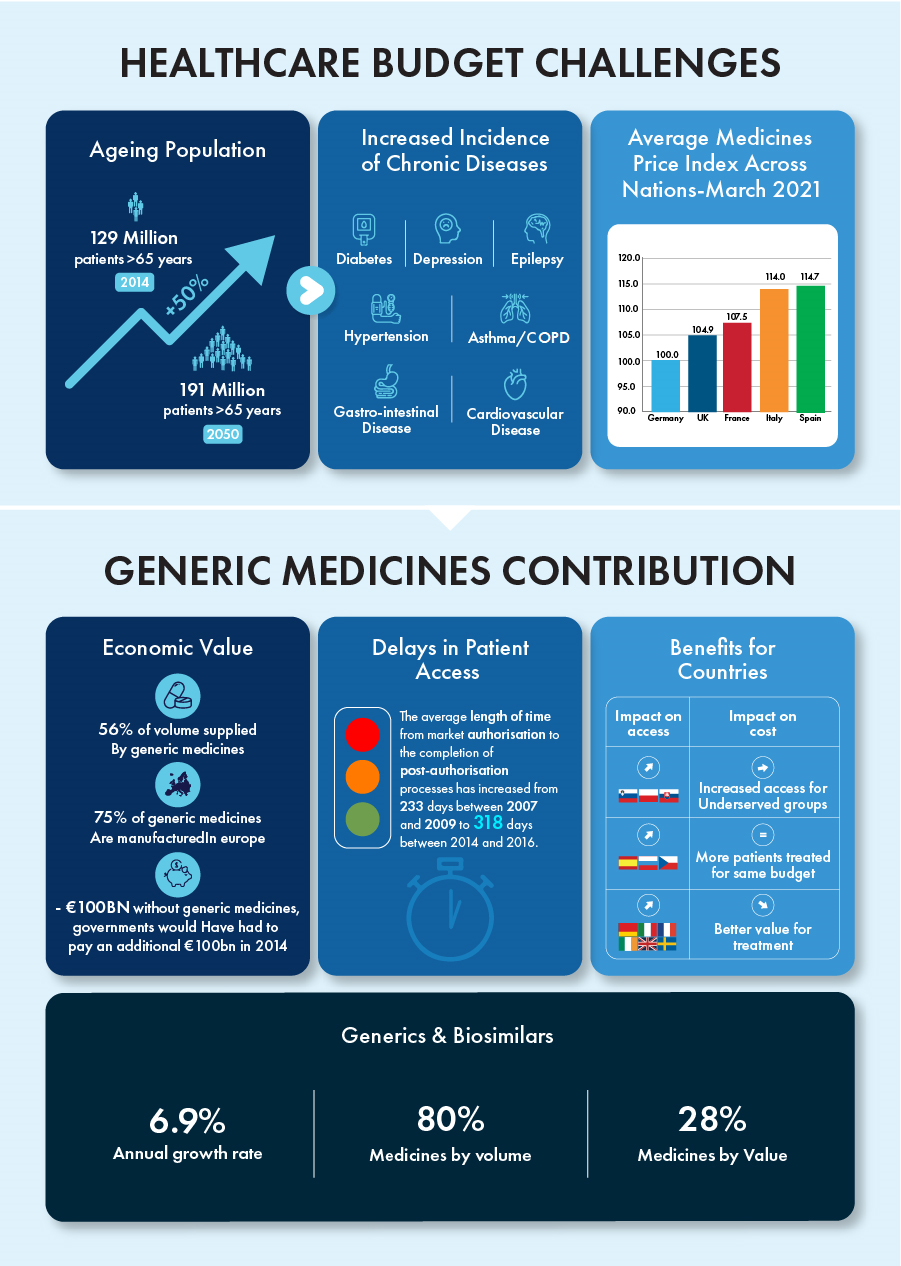
Los medicamentos genéricos y biosimilares han contribuido por sí solos a una tasa de crecimiento anual del 6,9 % mientras que representan el 80 % de todos los medicamentos por volumen y el 28 % por valor en la última década. El plazo de la patente para ciertos productos biológicos valorados en unos 90 000 millones de euros finalizará en 2023, creando un entorno competitivo para estos productos con un enorme potencial de crecimiento.
La implementación de una exención del Certificado Complementario de Protección (CCP) beneficiaría a la Unión Europea al:
- Añadiendo aproximadamente 90.5 mil millones de euros adicionales al año.
- Generando veinticinco mil (25.000) nuevas oportunidades de empleo con dos mil (2.000) empleos directos para la industria de API de la UE. La iniciativa ayudará a los Member States de la UE a ahorrar 3.100 millones de euros en gastos sanitarios.
- Acumulación de alternativas más baratas de medicamentos patentados innovadores para permitirles entrar en el mercado inmediatamente después del vencimiento de la Propiedad Intelectual (PI), mejorando el acceso de los pacientes.
Para un fabricante de medicamentos con sede en la Unión Europea, la implementación de la exención del SPC es una de las iniciativas más gratificantes a favor de los genéricos. Dado que la Autoridad Sanitaria de la UE regula los medicamentos para uso humano y veterinario a través de un procedimiento centralizado o descentralizado, navegar por los requisitos locales específicos puede resultar abrumador. Un experto, conocedor de los requisitos locales en cuanto a diversas presentaciones y documentos de licencia, puede ayudarle a centrar sus esfuerzos en los protocolos de producción esenciales en lugar de obsesionarse con complejos obstáculos reglamentarios. Reimagine el potencial de su negocio experimentando el cumplimiento y la calidad. Contacte con Freyr.









