
Los estudios de toxicología son fundamentales para el proceso de aprobación de productos farmacéuticos, garantizando que los nuevos medicamentos sean seguros para el uso humano. Estos estudios evalúan los posibles efectos adversos de los nuevos compuestos y determinan los niveles de dosificación seguros. Sin evaluaciones toxicológicas exhaustivas, los riesgos asociados con los nuevos productos farmacéuticos podrían superar sus beneficios, lo que llevaría a graves consecuencias para los pacientes y a contratiempos para las empresas farmacéuticas.
A pesar de su importancia crítica, los estudios de toxicología pueden asociarse con desafíos. Las evaluaciones de toxicología inadecuadas o defectuosas pueden provocar importantes contratiempos en el desarrollo de fármacos, incluidos retrasos clínicos, requisitos de pruebas adicionales o la denegación total de la aprobación por parte de las autoridades reglamentarias. Estos problemas no solo retrasan la disponibilidad de medicamentos que pueden salvar vidas, sino que también aumentan los costos de desarrollo y reducen la probabilidad de que un fármaco llegue al mercado.
Aspectos clave de los estudios de toxicología
Los estudios de toxicología abarcan varios tipos, cada uno de los cuales aborda preocupaciones de seguridad específicas relevantes para los productos farmacéuticos. Aquí, exploramos los principales tipos de estudios de toxicología y sus funciones en el proceso de aprobación de productos farmacéuticos.
Toxicología preclínica
La toxicología preclínica implica estudios iniciales realizados in vitro e in vivo para evaluar los niveles de toxicidad antes de los ensayos en humanos/clínicos. Estos estudios ayudan a identificar posibles efectos adversos y a determinar rangos de dosis seguros.
Estudios de Toxicidad Crónica
Los estudios de toxicidad crónica evalúan los efectos de la exposición prolongada a un fármaco, lo cual es crucial para tratamientos destinados a enfermedades crónicas. Estos estudios a largo plazo ayudan a identificar cualquier efecto adverso tardío que podría no ser evidente en estudios a corto plazo.
Toxicología reproductiva y del desarrollo.
Estos estudios examinan los posibles efectos de un fármaco en la reproducción y el desarrollo fetal. Son esenciales para asegurar que los productos farmacéuticos no afecten negativamente la fertilidad ni causen problemas de desarrollo en la descendencia.
Pruebas de genotoxicidad
Las pruebas de genotoxicidad determinan si un compuesto puede causar mutaciones genéticas, lo que podría conducir al cáncer. Estas evaluaciones son vitales para identificar posibles riesgos carcinogénicos asociados con nuevos medicamentos.
| Tipo de estudio de toxicología | Propósito |
|---|---|
| Toxicidad Aguda | Determina los efectos inmediatos de un medicamento |
| Toxicidad subcrónica | Evalúa los efectos de la exposición repetida durante un período corto. |
| Toxicidad Crónica | Evaluar los efectos a largo plazo de la exposición prolongada |
| Toxicología reproductiva. | Examina el impacto de los medicamentos en la fertilidad y el desarrollo fetal |
El papel de los expertos reglamentarios
Los expertos reglamentarios desempeñan un papel fundamental para garantizar el éxito de los estudios de toxicología. Aportan su experiencia en el diseño e interpretación de estos estudios, garantizando el cumplimiento de los estándares reglamentarios globales. Los socios reglamentarios ayudan en la preparación de informes completos para su presentación y en la gestión eficaz de las consultas reglamentarias. Su participación puede agilizar el proceso de aprobación y aumentar la probabilidad de éxito de un fármaco.
Beneficios de colaborar con socios reglamentarios
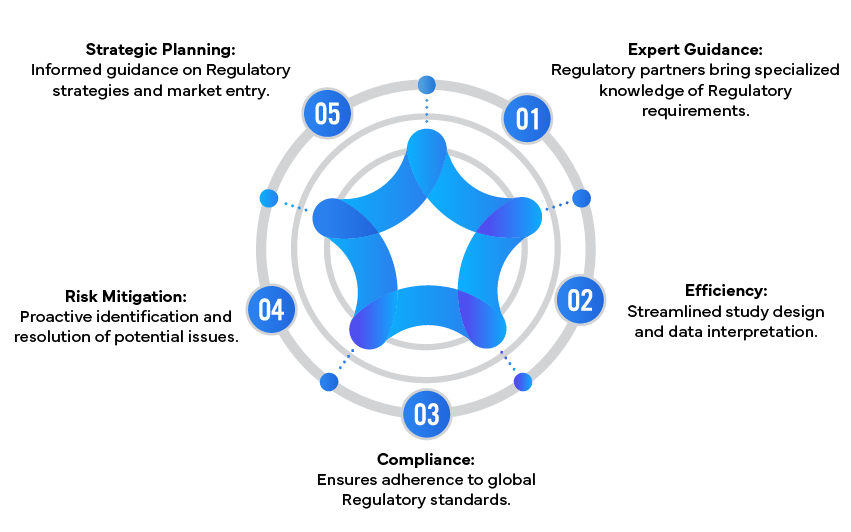
Conclusión
Los estudios de toxicología son fundamentales para establecer el perfil de seguridad de los nuevos productos farmacéuticos. Al abordar diversas preocupaciones de seguridad a través de diferentes tipos de evaluaciones toxicológicas, estos estudios garantizan que los nuevos productos farmacéuticos sean seguros para el uso humano. Colaborar con expertos reglamentarios experimentados puede agilizar aún más el proceso de aprobación, asegurando el cumplimiento de estrictas normas de seguridad y aumentando la probabilidad de éxito de un producto farmacéutico en el mercado. Al adoptar un enfoque integral y proactivo de la toxicología, las empresas farmacéuticas pueden gestionar las complejidades del desarrollo de productos farmacéuticos de manera más eficaz, lo que en última instancia se traduce en tratamientos más seguros y efectivos para los pacientes.










