
Las Autorizaciones de Uso de Emergencia (EUA) son importantes para que los productos medicinales que salvan vidas estén disponibles para los pacientes más rápidamente. Han sido útiles para hacer frente a pandemias como la COVID-19. Una iniciativa de la Administración de Alimentos y Medicamentos de los US (USFDA) comenzó en el año 2004, y la EUA entró en vigor cuando la Sección 564 de la Ley Federal de Alimentos, Medicamentos y Cosméticos fue modificada por la Ley Project BioShield. Este programa es un paso dado por la FDA para proteger la salud pública asegurando la seguridad, eficacia y calidad de los productos médicos, al mismo tiempo que aborda las emergencias médicas y las amenazas emergentes para la salud pública.
Entendámoslo mejor a continuación.
Decodificando la EUA
La vía de la EUA es un medio para facilitar la accesibilidad de contramedidas médicas en tiempos de emergencias declaradas. El Comisionado de la FDA puede autorizar lo siguiente en tales situaciones:
- El uso autorizado de productos médicos no aprobados.
- El uso no autorizado de productos médicos aprobados.
Los productos cubiertos por la EUA incluyen vacunas, fluidos intravenosos, medicamentos, dispositivos, pruebas, etc., y pueden utilizarse para diagnosticar, tratar o prevenir afecciones que ponen en peligro la vida. Se concede la EUA a los productos si se cumplen los siguientes criterios:
- Prueba de una condición/enfermedad que ponga en peligro la vida.
- Los datos científicos proporcionan pruebas suficientes de que el producto es eficaz para el uso previsto.
- Los beneficios del producto superan los riesgos (es decir, evidencia de seguridad).
- Falta de productos alternativos.
Se aconseja a los patrocinadores que comprendan los requisitos de la FDA con antelación para que sigan el mejor proceso reglamentario y aseguren una presentación de EUA sin errores. A continuación, se presenta la información obligatoria que debe compartir el patrocinador en la solicitud.
Datos a presentar por el patrocinador a la FDA para una aprobación de EUA
- Descripción del producto y su uso previsto.
- El estado de aprobación del producto ante la FDA.
- Información de seguridad y eficacia, como datos clínicos y no clínicos, etc.
- Informe de análisis de riesgo-beneficio.
- Datos de Química, Fabricación y Controles (CMC).
- Información sobre la dosificación, contraindicaciones, advertencias y eventos adversos para la distribución del producto médico en cuestión.
¿Cómo son emitidas las EUA por la FDA?
A continuación se presenta una interpretación esquemática del ciclo de vida de la EUA en resumen:
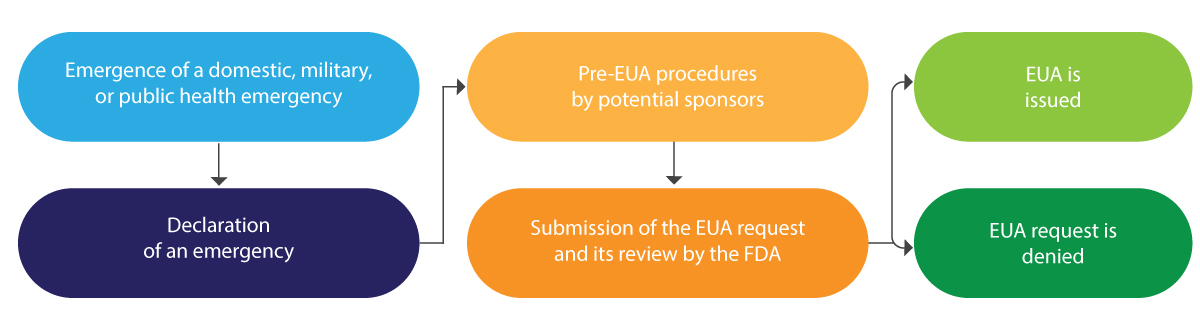
La EUA se emite normalmente por un período limitado y, al finalizar dicha emergencia, es terminada por la FDA.
EUA y COVID-19
El Secretario de Salud y Ciencias Humanas (HHS) declaró el COVID-19 como pandemia el 31 de enero de 2020. Desde entonces, la FDA ha sido fundamental en la aprobación de algunas vacunas y kits de prueba caseros bajo la vía de EUA para hacer frente al brote global en curso.
Con la aparición de nuevas variantes de la COVID-19, toda la industria farmacéutica está trabajando arduamente para frenar la propagación y reducir las tasas de mortalidad. Existe la necesidad de productos medicinales novedosos y aprobaciones más rápidas por parte de las Autoridades Reglamentarias globales para que se reduzca su tiempo de comercialización. La vía de Autorización de Uso de Emergencia (EUA) para registrar nuevos productos medicinales/fármacos es el camino a seguir, según los expertos. Varias otras Autoridades Sanitarias como la Agencia Europea de Medicamentos (EMA), la Central Drugs Standard Control Organization (CDSCO), la Saudi Food and Drug Authority (SFDA), etc., también han implementado la vía EUA para aprobaciones más rápidas.
Si usted es un fabricante de medicamentos y busca una EUA para su producto que salva vidas, necesitará un proveedor experto en soluciones reglamentarias. Contacte con Freyr para un tiempo de comercialización más rápido y una vía de cumplimiento.










