SmPC o Resumen de las Características del Producto es un documento legal que forma parte de la autorización de comercialización de cada medicamento. El documento sirve como base de información sobre el uso de medicamentos para los profesionales de la salud. La información incluida en el SmPC se actualiza regularmente a medida que surge la información más reciente. El SmPC contiene más información que un prospecto. La información del SmPC se puede encontrar a través de las siguientes fuentes:
- Sitios web de Autoridades Sanitarias; como la Agencia Europea de Medicamentos (EMA)
- Diccionarios de medicamentos
¿De qué consta un SmPC?
- Información relacionada con el uso del medicamento.
- Información cualitativa y cuantitativa sobre los beneficios y riesgos de los medicamentos
- Información sobre la dosificación
- Método de administración
- Información farmacológica
- Información de atención individual
Estructura de un SmPC
La estructura del SmPC está definida por la legislación farmacéutica europea. La información incluida en el SmPC debe ser específica del producto y puede remitirse a otras secciones para evitar redundancias. Debe documentarse en un lenguaje claro y no debe dar lugar a ambigüedades. El SmPC se divide en 6 secciones principales:
- Nombre del producto
- Composición.
- Forma farmacéutica
- Datos clínicos – Incluye indicaciones terapéuticas, recomendaciones de dosificación e información de seguridad
- Propiedades farmacológicas – Tiene en cuenta las indicaciones terapéuticas de los elementos clínicos y sus posibles reacciones adversas a medicamentos
- Datos farmacéuticos – Incluye información reglamentaria relacionada con el medicamento
Según la EMA, la estructura de un SmPC se puede representar como:
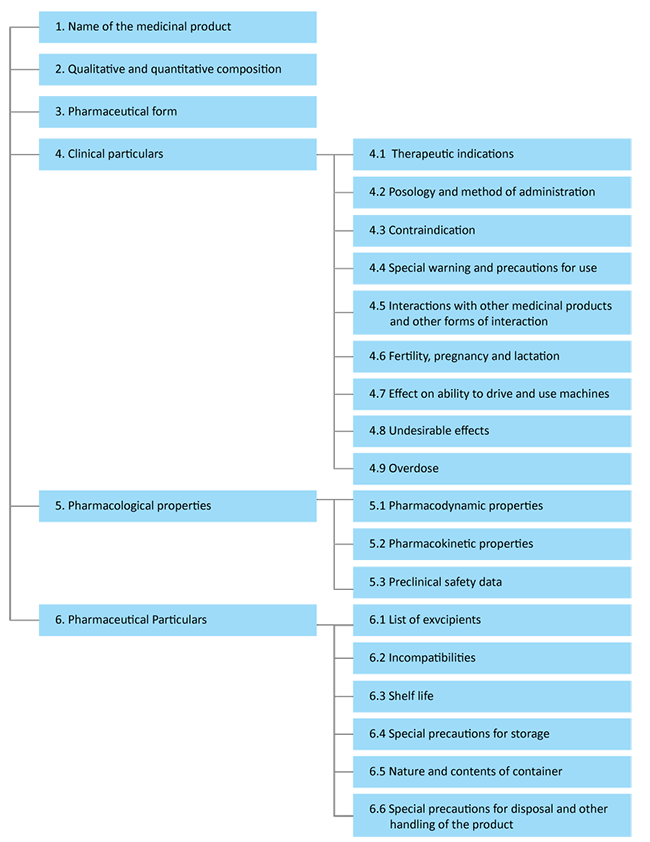
Referencia: EMA
¿Qué Información se Excluye de un SmPC?
- Información disponible en los informes de evaluación pública (detalles del desarrollo científico)
- Información de indicación no aprobada
- Cuestiones que carecen de datos
- Asesoramiento general sobre afecciones farmacológicas
Mantener una SmPC es importante para el ciclo de vida de cualquier medicamento, ya que forma parte de su autorización de comercialización. Por lo tanto, se recomienda encarecidamente la redacción de una SmPC conforme a la normativa. ¿Busca asistencia reglamentaria experta para desarrollar una SmPC? Contacte con Freyr en sales@freyrsolutions.com.