
L'intercambiabilità con un prodotto biologico di riferimento rappresenta un passaggio cruciale nel processo di approvazione dei biosimilari. Essa garantisce che un biosimilare possa sostituire il prodotto di riferimento senza rischi significativi di efficacia ridotta o maggiori preoccupazioni per la sicurezza. Questo blog si propone di analizzare l'ultimo aggiornamento della FDA sulle considerazioni per ottenere l'intercambiabilità e le migliori pratiche del settore per raggiungere l'eccellenza normativa.
Definire l'intercambiabilità
Il raggiungimento dell'intercambiabilità è un processo complesso e rigoroso che richiede il rispetto di stringenti requisiti normativi. La sfida consiste nel dimostrare che il biosimilare non solo corrisponde al prodotto di riferimento in termini di sicurezza ed efficacia, ma fornisce anche gli stessi risultati clinici in qualsiasi paziente. Il mancato rispetto di questi requisiti può comportare ritardi o rifiuti nell'approvazione, influenzando l'accesso al mercato e l'assistenza ai pazienti.
Requisiti normativi per l'intercambiabilità
La FDA delinea criteri specifici per dimostrare l'intercambiabilità nei suoi documenti guida. Questi criteri includono:
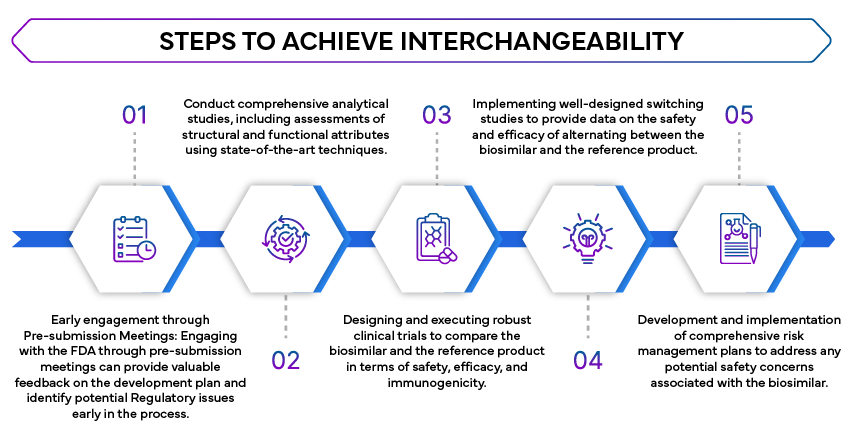
- Studi Analitici Comparativi: Sono richiesti studi analitici approfonditi per dimostrare che il biosimilare è altamente simile al prodotto di riferimento. Questi studi valutano la struttura molecolare, la funzione e la composizione del biosimilare.
- Studi Clinici: Sono necessari studi clinici per confermare che il biosimilare non presenta differenze clinicamente significative rispetto al prodotto di riferimento in termini di sicurezza, purezza e potenza. Ciò spesso comporta studi comparativi di farmacocinetica (PK) e farmacodinamica (PD).
- Studi di switching: La FDA richiede studi di switching per valutare l'impatto dell'alternanza tra il biosimilare e il prodotto di riferimento. Questi studi sono cruciali per garantire che il passaggio non influisca sull'efficacia o sulla sicurezza del trattamento.
- Strategie di valutazione e mitigazione del rischio (REMS): Se applicabili, le REMS devono essere affrontate per garantire che il biosimilare possa essere utilizzato in modo intercambiabile senza ulteriori preoccupazioni per la sicurezza.
Passi per raggiungere strategicamente l'intercambiabilità
Ruolo di un Partner Normativo
Le partnership regolatorie possono migliorare significativamente la probabilità di raggiungere l'intercambiabilità. Ecco come un partner regolatorio può aiutare:
- Guida di esperti: Fornisce consulenza esperta sui requisiti normativi e sulle strategie per soddisfare le linee guida della FDA.
- Supporto alla documentazione: Assiste nella preparazione di documenti di presentazione di alta qualità conformi agli standard normativi.
- Progettazione di Studi Clinici: Supporta la progettazione e l'esecuzione di studi clinici e di transizione solidi.
- Interazioni con le HA: Facilita una comunicazione efficace con le HA, garantendo un feedback tempestivo e costruttivo.
- Gestione del Rischio: Sviluppare strategie complete di gestione del rischio per mitigare potenziali preoccupazioni relative alla sicurezza.
Vantaggi di avere un partner normativo
| Vantaggi | Descrizione | |
| 1. | Competenza nei requisiti normativi | Profonda conoscenza dei panorami e dei requisiti normativi globali. |
| 2. | Documentazione semplificata | Garantisce la preparazione di documentazione accurata e conforme. |
| 3. | Processo di presentazione efficiente | Riduce tempo e costi grazie a una gestione efficiente delle sottomissioni. |
| 4. | Maggiore conformità | Riduce al minimo il rischio di ritardi e rifiuti attraverso una conformità rigorosa. |
| 5. | Gestione efficace del rischio | Identificazione e mitigazione proattiva dei rischi potenziali. |
Riepilogo
Il raggiungimento dell'intercambiabilità con un prodotto di riferimento è un processo impegnativo ma essenziale per l'approvazione di successo dei biosimilari. Richiede una comprensione approfondita dei requisiti normativi, una pianificazione meticolosa e dati clinici solidi. Collaborare con un fornitore di servizi normativi esperto può aumentare notevolmente le possibilità di successo, garantendo che il biosimilare soddisfi i rigorosi criteri stabiliti dalle autorità di regolamentazione. Sfruttando la guida di esperti, una documentazione accurata e una gestione strategica del rischio, gli sponsor possono navigare il complesso percorso verso l'intercambiabilità in modo più efficace.










