
L'adozione dell'eCTD 4.0 rappresenta un passo cruciale verso la modernizzazione delle presentazioni regolatorie a livello mondiale. Con vantaggi come il tracciamento migliorato dei documenti e le efficienze basate sui Metadata, non sorprende che le agenzie globali stiano adottando questo cambiamento.
Ma qual è la posizione di EMA? A differenza della FDA, che ha delineato chiare fasi di implementazione, EMA sta adottando un approccio più misurato, iniziando con programmi pilota e valutazioni tecniche. In questo blog, analizziamo i piani di EMA per eCTD 4.0, il suo potenziale impatto sulle presentazioni normative e come la vostra azienda può rimanere all'avanguardia.
Ancora più importante, l'EMA ha già reso obbligatorio l'eCTD 4.0? Approfondiamo.
Cos'è l'eCTD 4.0 e in cosa si differenzia dall'eCTD 3.2.2?
Il Documento Tecnico Comune Elettronico (eCTD) è il formato accettato a livello internazionale per le presentazioni normative. Standardizza il modo in cui le aziende farmaceutiche presentano le domande di farmaci e gestiscono gli aggiornamenti del ciclo di vita nei diversi mercati.
La versione attuale, eCTD 3.2.2, è in uso da anni. Tuttavia, gli organismi di regolamentazione, inclusa EMA, hanno lavorato per l'eCTD 4.0, che è basato sullo standard Health Level 7 (HL7) Regulated Product Submission (RPS). Questo aggiornamento migliora l'efficienza delle sottomissioni e la gestione del ciclo di vita normativo.
Differenze chiave tra eCTD 3.2.2 ed eCTD 4.0:
- Migliore gestione del ciclo di vita: Migliore tracciabilità delle versioni dei documenti, riducendo la duplicazione.
- Granularità più flessibile: consente il riutilizzo di documenti strutturati in diverse presentazioni.
- Gestione Migliorata dei Metadata: Metadata più strutturati, che rendono le interazioni normative più fluide.
- Maggiore interoperabilità: Progettato per funzionare meglio con i sistemi normativi digitali in evoluzione a livello globale.
- Mentre questi cambiamenti offrono numerosi vantaggi, la transizione all'eCTD 4.0 richiede preparazione, investimenti e una comprensione delle aspettative normative.
La posizione dell'EMA sull'adozione di eCTD 4.0
La grande domanda nella mente di tutti è: EMA ha reso obbligatorio l'eCTD 4.0? La risposta è non ancora, ma la transizione è in corso.
Stato Attuale dell'eCTD 4.0 nell'UE:
- Ad oggi, eCTD 3.2.2 rimane lo standard obbligatorio per le presentazioni nell'UE.
- EMA ha attivamente valutato eCTD 4.0 ma non ne ha ancora ufficialmente imposto l'uso.
- L'agenzia sta collaborando con altri organismi regolatori, come la FDA e la PMDA giapponese, per allineare gli standard globali.
- Non sono state fissate scadenze ufficiali per la transizione, ma EMA ha indicato che l'eCTD 4.0 diventerà obbligatorio a tempo debito.
L'approccio dell'EMA: Implementazione graduale con un programma pilota
A differenza della USFDA, che ha delineato un piano di implementazione graduale, l'EMA sta adottando un approccio strutturato. L'agenzia ha lanciato un Programma Pilota Tecnico per testare l'implementazione di eCTD 4.0 con le parti interessate del settore.
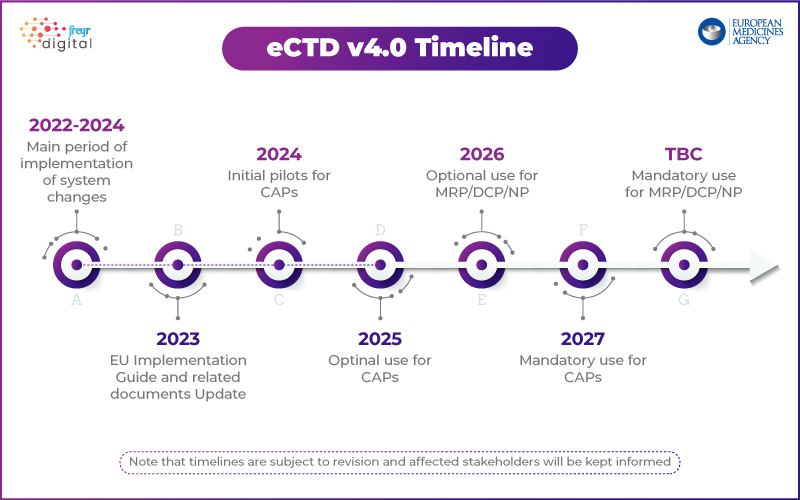
Punti salienti della strategia eCTD 4.0 dell'EMA:
- Fase 1: Concentrarsi sull'interoperabilità tecnica con gli strumenti normativi.
- Fasi Future: Sottomissioni simulate, gestione del ciclo di vita e sottomissioni raggruppate.
- Bozza del pacchetto di implementazione disponibile con vocabolari controllati e criteri di convalida.
EMA si impegna a garantire una transizione fluida e le aziende delle scienze della vita dovrebbero seguire gli aggiornamenti sulla pagina ufficiale EMA eCTD.
Sfide e Considerazioni per le Aziende delle Scienze della Vita
Sebbene eCTD 4.0 offra chiari vantaggi, la sua adozione non è priva di sfide. Ecco alcune considerazioni chiave per le aziende farmaceutiche e biotecnologiche:
- Complessità normative
- La transizione graduale dell'EMA significa che le aziende devono essere preparate per processi di presentazione doppi (eCTD 3.2.2 ed eCTD 4.0).
- Diverse regioni avranno tempistiche di adozione differenti, il che richiederà alle aziende di rimanere agili.
- Sfide tecniche
- La migrazione dei dati dall'eCTD 3.2.2 al 4.0 richiede un'attenta pianificazione.
- Le regole di validazione cambieranno in modo significativo, richiedendo software e strumenti aggiornati.
- Le aziende devono investire in soluzioni di automazione e basate sull'IA per garantire la conformità.
- Rischi di conformità
- Mappatura errata dei metadata o il mancato rispetto dei nuovi requisiti di granularità dei documenti potrebbe portare al rifiuto della presentazione.
- I team normativi necessitano di una formazione adeguata per comprendere le nuove regole di convalida.
- Impatto sui flussi di lavoro esistenti
- Le aziende dovranno adattare i processi interni per accogliere eCTD 4.0.
- Sarà necessaria una maggiore collaborazione tra i team normativi, IT e di presentazione.
Il messaggio chiave? Le aziende devono iniziare a prepararsi ora, anche se l'EMA non ha ancora reso obbligatorio l'eCTD 4.0.
Come le aziende possono prepararsi alla transizione eCTD 4.0 dell'EMA
Anche se l'EMA non ha fissato una scadenza ufficiale, le aziende proattive trarranno vantaggio da una preparazione tempestiva. Ecco come:
- Valutare i processi di presentazione attuali
- Identificare le lacune nei flussi di lavoro eCTD 3.2.2 esistenti.
- Valutare come le nuove norme di gestione del ciclo di vita influenzeranno le domande in corso.
- Investire negli strumenti eCTD 4.0 giusti
- Selezionate un software per la presentazione normativa conforme a eCTD 4.0.
- Assicurarsi che il software supporti gli standard HL7 RPS e l'automazione dei Metadata.
- Formare i team normativi e IT
- Condurre workshop e sessioni di formazione sulle modifiche dell'eCTD 4.0.
- Fornire linee guida per l'etichettatura dei Metadata e il tracciamento del ciclo di vita.
- Collaborare con l'EMA e i colleghi del settore
- Partecipare ai programmi pilota dell'EMA e alle consultazioni normative.
- Rimanete aggiornati sulle ultime linee guida e sugli aggiornamenti normativi dell'EMA.
- Condurre test e convalida
- Eseguire presentazioni di prova interne utilizzando strutture eCTD 4.0.
- Identificare potenziali problemi nella granularità dei documenti e nella mappatura dei Metadata prima del mandato finale dell'EMA.
Iniziando ora, le aziende possono garantire una transizione agevole senza interruzioni nelle pratiche normative.
Cosa c'è dopo? Il futuro dell'eCTD 4.0 in Europa
Sebbene la tempistica completa della transizione rimanga incerta, la strategia a lungo termine dell'EMA prevede:
- Standardizzare le sottomissioni nei mercati globali, migliorando la coerenza e l'efficienza.
- Ridurre i tempi di approvazione grazie a un migliore tracciamento del ciclo di vita delle sottomissioni.
- Integrare l'IA e l'automazione nei flussi di lavoro normativi per migliorare la conformità.
Nei prossimi anni, possiamo aspettarci maggiore chiarezza dall'EMA, incluse le tempistiche ufficiali di transizione e i nuovi criteri di convalida.
Conclusione
Sebbene l'EMA non abbia ancora reso obbligatorio l'eCTD 4.0, è solo questione di tempo prima che diventi lo standard per le presentazioni regolatorie nell'UE. Le aziende che si preparano proattivamente otterranno un vantaggio competitivo, garantendo la conformità ed evitando ostacoli normativi dell'ultimo minuto.
Punti chiave
- eCTD 3.2.2 rimane lo standard attuale, ma eCTD 4.0 è all'orizzonte.
- EMA sta adottando un approccio graduale, senza un mandato ufficiale ancora.
- Le aziende dovrebbero iniziare a prepararsi ora per garantire una transizione agevole.
- Investire in nuove tecnologie, formare i team e testare le sottomissioni sarà fondamentale.
Invito all'azione
Rimanete aggiornati sugli annunci normativi dell'EMA e iniziate a valutare la vostra prontezza per l'eCTD 4.0. Prima vi preparate, più facile sarà la transizione quando arriverà il mandato.
Desiderate assistenza nella scelta di un software conforme a eCTD 4.0 o per capire come questa transizione influisce sulla vostra attività? Non esitate a contattarci.









