
La United States Food and Drug Administration (US FDA) ha pubblicato una guida a dicembre 2022, una revisione della guida intitolata 'Failure to Response to an ANDA Complete Response Letter (CRL) Within the Regulatory Timeframe Guidance for Industry', di luglio 2022. È destinata a guidare i richiedenti di Abbreviated New Drug Applications (ANDAs) presentate ai sensi della sezione 505(j) del Federal Food, Drug, and Cosmetic Act (FD&C Act) (21 U.S.C. 355(j)). Una risposta completa e pertinente a una CRL è cruciale per l'approvazione del farmaco generico. Il documento di guida offre raccomandazioni riguardo alle ripercussioni del ricevimento di una CRL e alle azioni che la FDA può intraprendere se alla CRL non viene data risposta entro il periodo di tempo specificato.
La FDA deve garantire che i farmaci generici approvati soddisfino gli standard di sicurezza, qualità, efficacia e accessibilità economica. Se l'ANDA non soddisfa i requisiti normativi della FDA, viene inviata una CRL al richiedente, che include le carenze identificate durante la sua valutazione.
Di seguito è riportata una descrizione figurativa di ciò che un richiedente può fare entro un anno dalla ricezione del CRL:
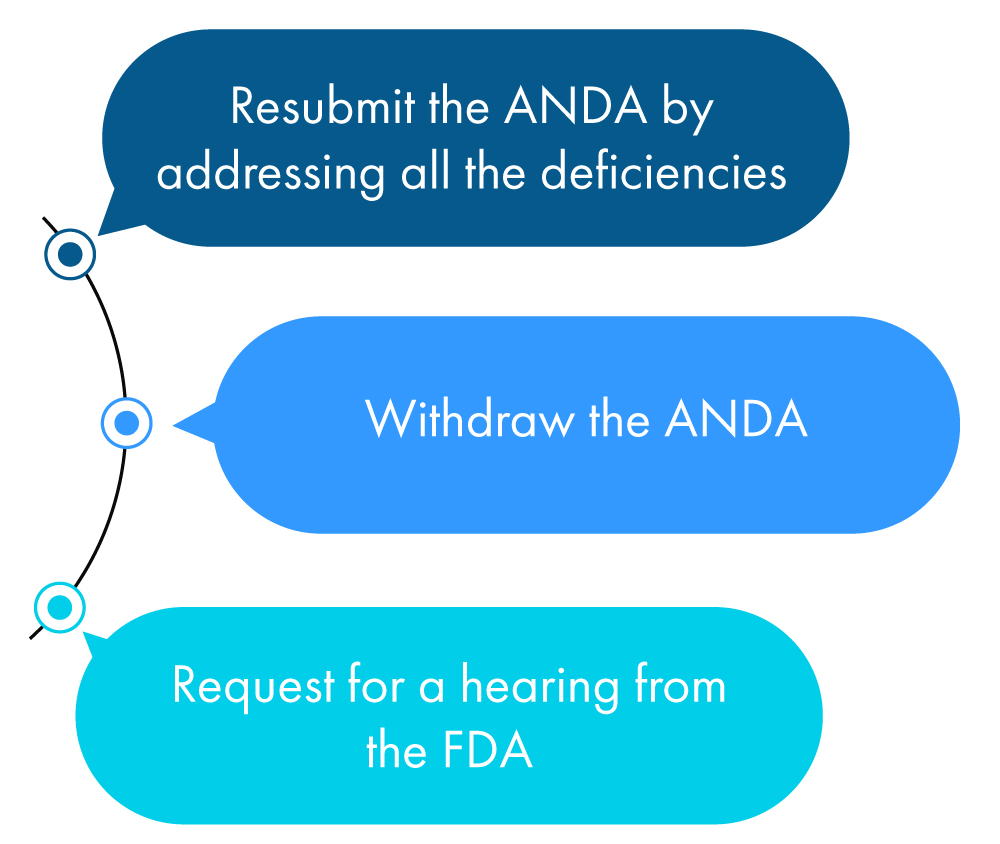
Se il richiedente non intraprende nessuna delle azioni sopra indicate, la FDA lo considera come una richiesta di ritiro dell'ANDA, a meno che il richiedente non abbia richiesto una proroga per verificare tutte le discrepanze menzionate nella CRL.
Cosa succede dopo un anno dall'emissione della CRL?
La FDA invia una notifica scritta che il richiedente ha trenta giorni dalla notifica per quanto segue:
- Fornire le ragioni per cui l'ANDA non dovrebbe essere ritirata
- Richiesta di proroga del termine per affrontare tutte le carenze menzionate nel CRL
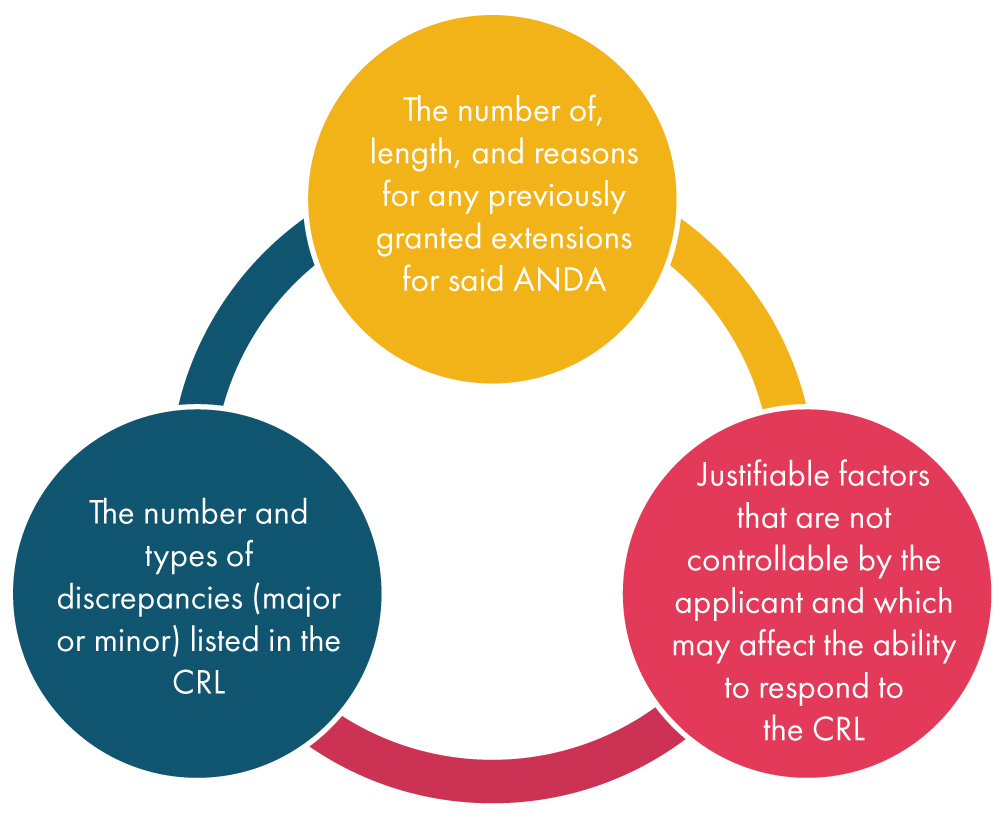
Una volta che la FDA riceve una richiesta di proroga dal richiedente, considera vari fattori come menzionato di seguito e successivamente decide sulla richiesta:
Cos'è un Emendamento?
Il richiedente deve presentare una richiesta di proroga per rispondere a un CRL tramite un emendamento. La FDA classifica un emendamento come maggiore o minore in base all'effetto che ha sul processo di approvazione.
Raccomandazioni essenziali della FDA di cui i richiedenti dovrebbero essere a conoscenza:
- La FDA riclassificherà un emendamento minore come maggiore se l'emendamento viene presentato dopo un anno dalla CRL, a meno che l'ANDA non sia per un prodotto presente nell'elenco dei farmaci in carenza ai sensi della sezione 506E del FD&C Act (21 U.S.C. 356e), o sia oggetto di una risposta a un'emergenza di salute pubblica dichiarata dal Segretario del Dipartimento della Salute e dei Servizi Umani degli US ai sensi della sezione 319 del Public Health Service Act (42 U.S.C. 247d), o si preveda che sia soggetto agli stessi criteri applicabili a tale dichiarazione, al momento della presentazione.
- Se il richiedente non riesce a risolvere le discrepanze nella CRL entro il periodo di proroga concesso dalla FDA, quest'ultima può considerare il ritiro dell'ANDA.
- Se il richiedente necessita di un periodo di proroga superiore a trenta giorni, può richiedere un'ulteriore proroga. L'integrazione dovrà quindi includere nuove informazioni che consentiranno alla FDA di determinare se la proroga può essere concessa o meno.
Ricevere una CRL dalla FDA può essere piuttosto scoraggiante per i richiedenti ANDA. Dall'affrontare le discrepanze al citare le ragioni/informazioni corrette per una proroga, tutti i requisiti pertinenti devono essere soddisfatti per garantire un'approvazione più rapida del farmaco. Freyr è un esperto regolatorio comprovato con una vasta conoscenza nella risposta alle CRL e nella garanzia di conformità ai requisiti FDA. Contattaci ora per un supporto strategico End-to-End nelle presentazioni ANDA.










