
Il settore delle normative farmaceutiche sta per subire un'importante evoluzione con l'introduzione dell'eCTD 4.0. Questo formato standardizzato promette di semplificare il processo di presentazione delle domande per i nuovi farmaci alle autorità regolatorie. Tuttavia, per le aziende che puntano a una quota del mercato farmaceutico giapponese, stimato in 141,5 miliardi di dollari, c'è un elemento cruciale: il Giappone sta accelerando i tempi di adozione!
Di seguito è riportata un'analisi di questi punti salienti:
- Adozione obbligatoria: Contrariamente ad altri settori che prevedono fasi volontarie prima dell'adozione obbligatoria, il Giappone mira a rendere l'uso dell'eCTD 4.0 obbligatorio entro il 2026.
- La preparazione è fondamentale: La preparazione è fondamentale a causa dei vincoli di tempo e dell'assenza di un percorso di migrazione diretto dal formato PMDA giapponese JP1.0 all'eCTD 4.0; concentrarsi su un sistema migliore aiuterà le aziende farmaceutiche in Giappone durante il processo di transizione. Questi passaggi includono l'aggiornamento del software, la formazione del personale e la preparazione dei PDF per il nuovo formato.
- Risorse disponibili: La Pharmaceuticals and Medical Devices Agency (PMDA) del Giappone ha pubblicato risorse che possono guidare le aziende attraverso questo cambiamento, come la "ICH Electronic Common Technical Document eCTD 4.0 Implementation Guide" con spiegazioni sulle modifiche apportate e sulle migliori pratiche disponibili.
Ecco alcuni motivi per cui non dovresti perdere questa opportunità legata ai numeri:
- Corsia preferenziale per eCTD 4.0: A differenza di altre regioni in cui il processo è graduale, il Giappone mira a un'adozione obbligatoria dell'eCTD 4.0 già nel 2026. Questo è tre anni prima della scadenza fissata dalla US FDA per il 2029! Con una tempistica così aggressiva, significa che il Giappone ha assunto la leadership in termini di incorporazione globale dell'eCTD.
- Nessun Margine di Errore: JP non poteva essere convertito direttamente in eCTD 4.0 a differenza delle sue versioni precedenti. Ciò significa che le aziende farmaceutiche devono essere particolarmente preparate per questo al fine di prevenire ritardi nella presentazione che potrebbero costare loro milioni di entrate.
- Un aiuto per un ingresso agevole: L'Agenzia per i Prodotti Farmaceutici e i Dispositivi Medici (PMDA) del Giappone comprende le sfide. Ha messo a disposizione risorse come guide all'implementazione, progettate per guidare le aziende attraverso queste modifiche con facilità e per un buon ingresso nel mercato giapponese. (https://www.pmda.go.jp/english/).
Se stai sviluppando farmaci per l'enorme mercato giapponese, è ora di darsi da fare! Ecco la tua lista di controllo pre-volo:
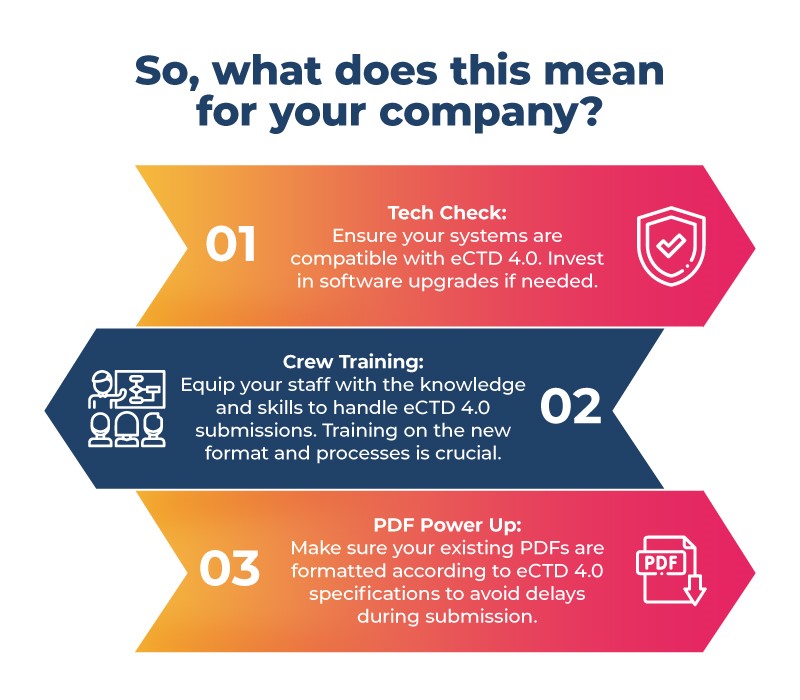
La transizione all'eCTD 4.0 promette maggiore efficienza e standardizzazione globale in tutto il processo di approvazione dei farmaci. La vostra azienda può anticipare questa mossa in Giappone per una transizione fluida e cogliere le innumerevoli opportunità offerte da questa nuova era. Ricordate che non prepararsi significa prepararsi al fallimento, quindi siate pronti ad avere successo con l'eCTD 4.0 in Giappone.
I benefici e le opportunità acquisite sono attraenti per l'industria farmaceutica. Tuttavia, essa presenta anche la sua parte di difficoltà lungo il percorso che devono essere risolte. Per navigare senza intoppi in un ambiente normativo in continua evoluzione, le aziende possono cercare partnership con consulenti affidabili come Freyr. Abbraccia il futuro delle sottomissioni normative in Giappone con il nostro software eCTD senza pari, Freyr SUBMIT PRO, conforme agli standard 21 CFR Part 11 e con un modello di implementazione flessibile. Contattaci oggi per saperne di più e intraprendere un percorso verso maggiore efficienza e successo. Richiedi una demo oggi.









