
Nel panorama normativo dell'assistenza sanitaria, i prodotti combinati rappresentano una frontiera dell'innovazione, fondendo i benefici di farmaci, dispositivi e prodotti biologici in soluzioni terapeutiche uniche e potenti. Tuttavia, una grande innovazione comporta una grande responsabilità, in particolare quando si tratta di garantire la sicurezza della nostra popolazione più vulnerabile: i bambini. Concentrandosi sugli imperativi critici dell'imballaggio a prova di bambino, questo blog descrive come le aziende del settore delle scienze della vita possono navigare in questo complesso terreno normativo.
La convergenza delle tecnologie farmaceutiche e dei dispositivi medici nei prodotti combinati presenta sfide uniche nella progettazione dell'imballaggio e nella conformità normativa. Gli approcci tradizionali all'imballaggio a prova di bambino potrebbero non essere sufficienti per questi prodotti complessi, portando a potenziali rischi per la sicurezza e ostacoli normativi.
I recenti richiami di prodotti medicinali da parte di importanti aziende farmaceutiche a causa di un imballaggio non adeguato a prova di bambino sottolineano l'importanza di questo problema e la necessità di un approccio più sfumato alla sicurezza e alla conformità normativa.
Considerazioni da fare:
- Comprensione dei quadri normativi:
I prodotti combinati rientrano nella giurisdizione di più organismi di regolamentazione, principalmente la FDA negli US. La modalità d'azione principale (PMOA) determina quale centro all'interno della FDA assume la guida nella regolamentazione – che sia il Center for Drug Evaluation and Research (CDER), il Center for Devices and Radiological Health (CDRH) o il Center for Biologics Evaluation and Research (CBER). Per gli imballaggi a prova di bambino, la conformità al Poison Prevention Packaging Act (PPPA) è fondamentale. - Considerazioni di Progettazione:
Lo sviluppo di imballaggi a prova di bambino per prodotti combinati richiede un delicato equilibrio tra sicurezza, usabilità e funzionalità. I design innovativi degli imballaggi non devono solo impedire l'accesso ai bambini, ma anche garantire la facilità d'uso per gli adulti, in particolare gli anziani o le persone con disabilità.
Ciò spesso rende necessarie nuove approcci come:- Meccanismi a doppia azione (ad es., tappi a pressione e rotazione)
- Tecnologie di distrazione visiva
- Sistemi di apertura attivati dall'umidità
- Blister perforati con schemi di strappo specifici
- Test e Validazione:
È fondamentale eseguire test rigorosi per garantire la conformità agli standard degli imballaggi a prova di bambino. Ciò include tipicamente:- Test del protocollo con bambini di età compresa tra 42 e 51 mesi
- Test adatto agli anziani per garantire l'accessibilità
- Test di stabilità per garantire l'integrità dell'imballaggio per tutto il ciclo di vita del prodotto
- Presentazioni normative:
La preparazione di una presentazione normativa completa per un prodotto combinato con confezione a prova di bambino comporta:- Specifiche dettagliate dell'imballaggio e motivazioni di progettazione
- Risultati dei test di resistenza all'apertura da parte dei bambini e di facilità d'uso per gli anziani
- Dati di stabilità che dimostrano l'efficacia dell'imballaggio nel tempo
- Analisi del rischio e strategie di mitigazione
Tabella: Standard normativi chiave per gli imballaggi a prova di bambino nei prodotti combinati
| Standard | Giurisdizione | Focus |
|---|---|---|
| 16 CFR 1700.20 | Stati Uniti | Protocolli di test per imballaggi richiudibili e non richiudibili |
| ISO 8317 | Internazionale | Requisiti per imballaggi richiudibili a prova di bambino |
| EN 14375 | Europa | Imballaggi non richiudibili per prodotti farmaceutici |
| BS EN 862:2005 | Europa | Imballaggi non richiudibili per prodotti non farmaceutici |
Ruolo dei Partner Normativi:
Orientarsi nel complesso panorama delle normative sui prodotti combinati, in particolare per quanto riguarda gli imballaggi a prova di bambino, può essere scoraggiante per le aziende del settore delle scienze della vita. È qui che i partner normativi svolgono un ruolo cruciale:
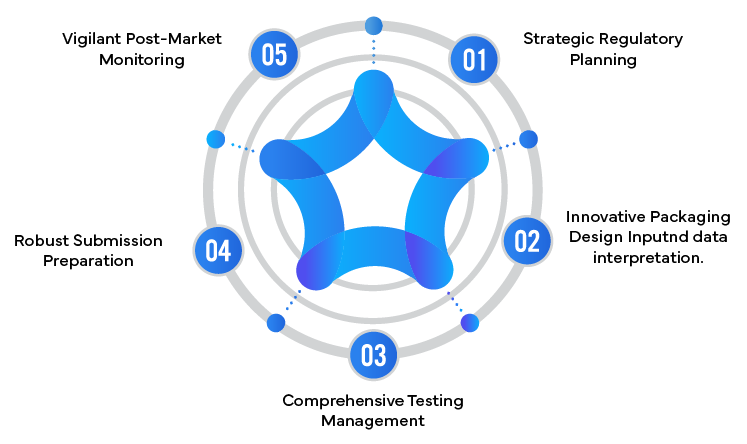
- Sviluppo della strategia normativa: Elaborazione di una strategia completa che affronta le sfide uniche dei prodotti combinati e i requisiti di imballaggio a prova di bambino.
- Input di Progettazione: Fornire approfondimenti sulla progettazione dell'imballaggio che soddisfa sia i requisiti normativi che le esigenze dell'utente.
- Coordinamento dei Test: Gestire e interpretare protocolli di test complessi per garantire la conformità agli standard di sicurezza a prova di bambino.
- Preparazione delle presentazioni: Compilazione di solide presentazioni normative che comunicano efficacemente la sicurezza e l'efficacia del prodotto.
- Sorveglianza post-commercializzazione: Implementazione di sistemi per monitorare le prestazioni e la sicurezza dei prodotti combinati in contesti reali.
5 modi in cui i partner normativi migliorano la sicurezza dei prodotti combinati
Riepilogo:
Mentre i prodotti combinati continuano a spingere i confini dell'innovazione medica, garantire la loro sicurezza attraverso un imballaggio efficace a prova di bambino rimane fondamentale. Navigare nel complesso panorama normativo richiede una comprensione approfondita delle normative sui prodotti farmaceutici e sui dispositivi medici, unita ad approcci innovativi alla progettazione dell'imballaggio.
Collaborando con esperti normativi, le aziende del settore delle scienze della vita possono non solo garantire la conformità normativa, ma anche promuovere l'innovazione nelle soluzioni di imballaggio che proteggono i bambini e migliorano l'usabilità per tutti i pazienti. In questo campo in evoluzione, la chiave del successo risiede nel bilanciare sicurezza, innovazione e acume normativo – una sfida che, se affrontata, promette di aprire nuove frontiere nella cura dei pazienti e nella progettazione dei prodotti.










