I costi di conformità per le aziende farmaceutiche possono rappresentare fino al 25% delle loro spese operative totali. Le aziende farmaceutiche con portafogli di prodotti diversificati affrontano sfide uniche nella gestione della conformità globale, nel monitoraggio delle presentazioni dei dossier e nella supervisione delle variazioni di etichettatura. La complessità dei requisiti normativi nelle diverse regioni, unita alla gestione manuale di grandi quantità di dati, può portare a non conformità, ritardi nelle approvazioni di mercato e inefficienze operative.
Questo blog esplora le principali sfide che le aziende farmaceutiche incontrano nella gestione di più portafogli di prodotti e dimostra come un software normativo, supportato da casi di studio reali, offra una soluzione strategica a questi problemi.
Principali sfide nella gestione di più portafogli di prodotti.
- Requisiti complessi di conformità globale: Ogni paese ha il proprio organismo di regolamentazione e i loro requisiti possono variare drasticamente. Ad esempio, la US FDA, l'EMA e la PMDA giapponese hanno diversi formati di presentazione, tempistiche e standard di conformità. Le aziende farmaceutiche devono gestire dossier diversi in più regioni, garantendo al contempo nessuna deviazione dalle normative locali.
- Tracciamento delle variazioni delle etichette tra le regioni: La gestione delle variazioni delle etichette per diverse regioni e la garanzia di aggiornamenti tempestivi è uno degli aspetti più impegnativi della gestione del portafoglio. Una gestione errata delle modifiche delle etichette può portare a non conformità, richiami di prodotti e gravi battute d'arresto finanziarie.
- Sovraccarico di sottomissioni di dossier: La sottomissione e la gestione di dossier per più linee di prodotti, ciascuna in diverse fasi di sviluppo, può rapidamente sovraccaricare i team interni. La gestione manuale degli aggiornamenti del ciclo di vita del prodotto porta spesso a errori e ritardi nelle approvazioni.
- Cattiva gestione delle risorse: I team spesso faticano ad allocare le risorse giuste in modo efficiente. Senza un sistema di gestione solido, le aziende possono sovraccaricare il personale con compiti amministrativi, limitando la loro capacità di concentrarsi sulle attività strategiche principali.
- Silos di dati: La mancanza di centralizzazione significa che i dati relativi a presentazioni, approvazioni e aggiornamenti dei prodotti sono archiviati in sistemi disparati, portando a inefficienze, problemi di comunicazione e difficoltà nel mantenere una visione olistica del ciclo di vita del prodotto.
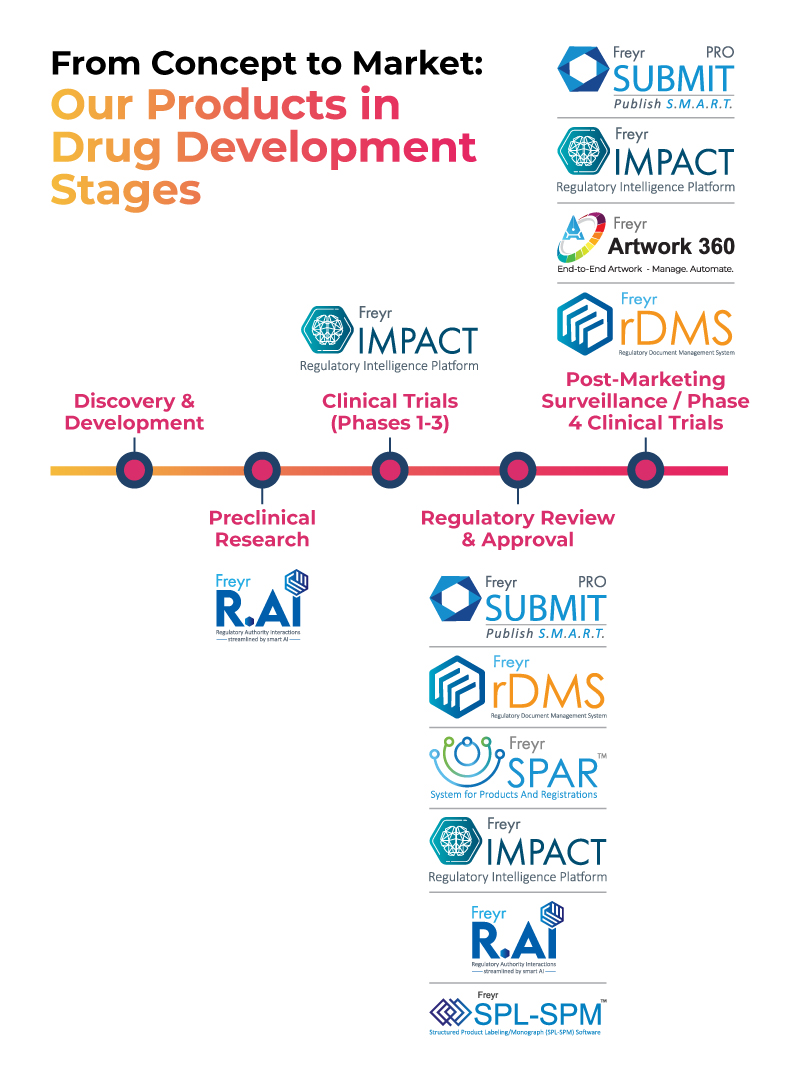
La suite di prodotti tecnologici di Freyr Digitale supporta le aziende farmaceutiche dal concetto al mercato, come mostrato nell'immagine sottostante.
Casi di studio: Come i software normativi offrono un vantaggio strategico
Adottando software normativi, le aziende farmaceutiche possono automatizzare i processi, garantire la conformità e in ultima analisi ottenere un vantaggio strategico rispetto ai concorrenti. I seguenti casi di studio evidenziano esempi reali di come le nostre soluzioni software normative abbiano aiutato le aziende farmaceutiche ad affrontare queste sfide.
Caso comprovato
Sfida del Cliente
Un'azienda farmaceutica generica statunitense aveva difficoltà a gestire in modo efficiente le sue presentazioni normative End-to-End e la gestione dei documenti. Hanno riscontrato problemi con repository di documenti frammentati, rendendo difficile fornire un accesso agevole ai documenti normativi sia per gli stakeholder interni che esterni. Inoltre, il processo di creazione e gestione dello Structured Product Labeling (SPL) era macchinoso, causando ritardi nelle tempistiche di presentazione e cicli di revisione più lunghi.
La soluzione di Freyr Digitale
Freyr Digitale è intervenuta come fornitore di soluzioni virtuali per gli affari normativi, implementando questi tre prodotti chiave come soluzioni per affrontare le sfide del cliente:
- Freyr rDMS: Un sistema centralizzato di gestione dei documenti per fungere da unica fonte di verità per tutte le presentazioni e i documenti normativi, garantendo accesso in tempo reale e controllo delle versioni sia per i team interni che per i partner esterni.
- Freyr SUBMIT PRO: Uno strumento potente per la pubblicazione e la presentazione eCTD, che semplifica il processo di presentazione, riduce i tempi di preparazione e garantisce la conformità agli standard normativi in evoluzione.
- Freyr SPL-SPM: Una soluzione efficiente per la gestione di tutte le attività relative a SPL, migliorando significativamente i processi di creazione, gestione e presentazione dei documenti.
Risultati
Implementando queste soluzioni, Freyr Digitale ha aiutato il cliente a raggiungere:
- Una riduzione del 30% nel tempo di preparazione delle sottomissioni
- Conformità al 100% a tutti i requisiti normativi
- Un miglioramento del 40% nell'efficienza di elaborazione dei documenti
- Una riduzione del 25% nei cicli di revisione
Conclusione: Abbracciare la Trasformazione Digitale per il Successo Strategico
La gestione di più portafogli di prodotti nei mercati globali non è un'impresa da poco. Tuttavia, con il software normativo giusto, le aziende farmaceutiche possono ottimizzare i processi, garantire la conformità e ottenere un vantaggio strategico nel settore.
La suite di strumenti normativi di Freyr Digitale-inclusi Freyr SUBMIT PRO, Freyr rDMS e Freyr SPL-SPM -ha costantemente aiutato le aziende farmaceutiche a ridurre i tempi di sottomissione, migliorare la conformità e ottimizzare le risorse. Automatizzando i processi manuali, fornendo una gestione centralizzata dei dati e offrendo approfondimenti in tempo reale, le nostre soluzioni consentono alle aziende farmaceutiche di rimanere competitive sul mercato. Contattaci.









