
Con la US Food and Drug Administration (USFDA) che implementerà la norma finale per i regolamenti del sistema di gestione della qualità (QMSR) nel 2024, i produttori di dispositivi medici devono adottare gli emendamenti per commercializzare e distribuire i loro dispositivi nel mercato degli STATI UNITI D'AMERICA.
Questa regola aggiorna i Regolamenti del Sistema Qualità (QSR) della USFDA allineandosi alla ISO 13485:2016, che è lo standard internazionale per il QMS dei dispositivi medici. I produttori di dispositivi medici hanno un periodo di transizione di due anni per conformarsi, il che rende necessario per le organizzazioni adattare i nuovi requisiti per evitare la non conformità al momento dell'ispezione.
Cos'è il QMSR?
Il QMSR della FDA è un approccio semplificato ai requisiti del QMS, che rappresenta un aggiornamento della precedente struttura QSR. Questo allineamento è cruciale perché semplifica la conformità globale per i produttori, specialmente quelli che operano a livello globale. Questa armonizzazione consentirà alle aziende di soddisfare i requisiti normativi sia negli US che in altri mercati in modo molto più unificato.
Il QMSR impone miglioramenti nella gestione del rischio, nella progettazione del dispositivo e nella sorveglianza post-commercializzazione. Questo ruolo può aggiungere maggiore complessità, ma offre anche ai produttori la possibilità di standardizzare le proprie procedure di qualità, il che a sua volta aumenta la sicurezza del dispositivo e migliora la documentazione, elementi vitali durante le ispezioni USFDA.
Principali modifiche nel QMSR
- Armonizzazione con ISO 13485: Questo è il passo più critico che consente ai produttori di dispositivi medici di accettare standard riconosciuti a livello internazionale. La USFDA ha riconosciuto che molte aziende di dispositivi medici sono già conformi a ISO 13485, il che riduce gli sforzi duplicati.
- La gestione del rischio enfatizza la gestione del rischio durante l'intero ciclo di vita del dispositivo medico. I produttori di dispositivi medici devono dimostrare una gestione del rischio, un controllo del rischio e una gestione del rischio efficaci.
- Progettazione e controlli del dispositivo: Nell'ambito del QMSR, i controlli di progettazione sono stati estesi per garantire che i produttori di dispositivi medici tengano pienamente conto delle esigenze degli utenti, della sicurezza del dispositivo e dei criteri di prestazione, che è un'area di interesse durante l'ispezione USFDA.
- Sorveglianza post-commercializzazione: Le aziende devono migliorare il sistema di monitoraggio post-commercializzazione. Ciò richiederà ai produttori di raccogliere informazioni sulla sicurezza e l'efficacia del dispositivo, il che aiuta a individuare e identificare rapidamente i problemi.
- Documentazione e tenuta dei registri: Questa è la regola finale che enfatizza la documentazione. Una tenuta dei registri accurata / adeguata è fondamentale durante l'ispezione.
Fasi per prepararsi all'ispezione della US Food and Drug Administration:
Con l'ispezione che durerà fino al 2026, le aziende hanno due anni per i loro sistemi di qualità, il che si allinea con il QMSR. Tuttavia, aspettare l'ultimo minuto può essere rischioso.
Passi per l'ispezione USFDA nell'ambito del quadro QMSR per le industrie in cui l'attuale QMS si basa sul QSR:
- Effettuare un'analisi delle lacune: Questo è il primo passo in cui l'attuale sistema qualità si discosta dai nuovi requisiti QMSR. Un'analisi approfondita delle lacune aiuterà a identificare le aree che necessitano di aggiornamenti, come la gestione del rischio, la sorveglianza post-commercializzazione e i controlli di progettazione.
- Aggiornare la procedura di gestione del rischio: Assicurarsi che le attività di gestione del rischio siano integrate nell'intero ciclo di vita del prodotto, dalla progettazione alla sorveglianza post-commercializzazione.
- Rivedere il controllo del design: i produttori dovrebbero assicurarsi che il processo di progettazione sia robusto e ben documentato. Convalidare che il processo di progettazione sia robusto, ben documentato e pienamente integrato nel vostro sistema di gestione della qualità.
- Migliorare la sorveglianza post-commercializzazione: implementare sistemi per monitorare le prestazioni del dispositivo dopo l'immissione sul mercato. Ciò può comportare l'istituzione di meccanismi di feedback dei clienti, la raccolta di dati clinici e il loro attento monitoraggio.
- Formazione e documentazione: Formare il personale sui nuovi requisiti, specialmente coloro che sono coinvolti nella gestione della qualità e nella conformità normativa. Ciò garantisce che l'intero processo di documentazione sia allineato alle aspettative del QMSR.
- Certificazione di terze parti: Se la vostra azienda non è certificata ISO 13485, ora potrebbe essere il momento di prenderla in considerazione. Ottenere la certificazione ISO 13485 può darvi un vantaggio nel soddisfare i requisiti della USFDA per aumentare la credibilità nei mercati globali.
Orientarsi nel periodo di transizione di due anni
Per utilizzare efficacemente il periodo di transizione e garantire la conformità al Regolamento sul Sistema di Gestione della Qualità (QMSR) della USFDA, i produttori dovrebbero adottare un approccio proattivo. Ecco una tabella di marcia suggerita:
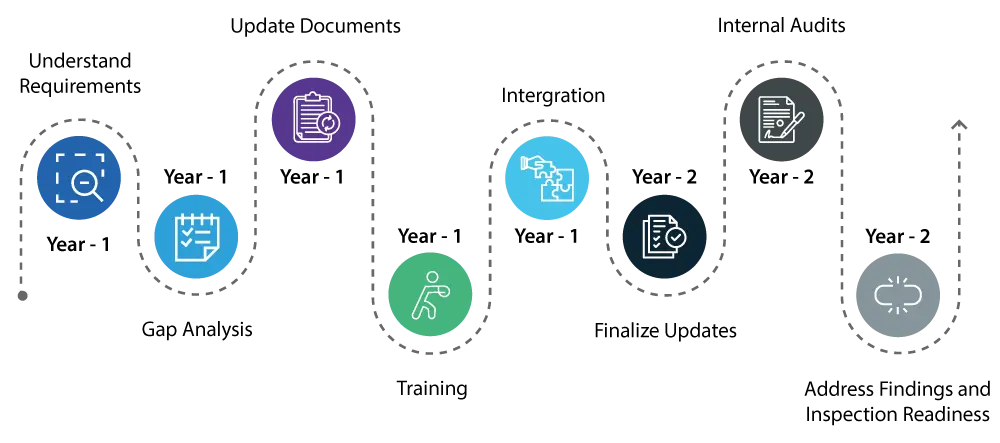
Anno 1:
- Comprendere il requisito: Iniziare comprendendo a fondo i cambiamenti introdotti dal QMSR. Ciò comporta una revisione dettagliata dei nuovi requisiti e di come differiscono dal Regolamento del Sistema Qualità (QS) esistente.
- Identificare le lacune: Effettuare un'analisi completa delle lacune per individuare le aree all'interno del vostro attuale sistema qualità che richiedono aggiornamenti per soddisfare i nuovi standard QMSR.
- Aggiornamento / rimedio della documentazione: Avviare gli aggiornamenti necessari al sistema qualità, concentrandosi su aree come la gestione del rischio e i controlli di progettazione, che sono componenti critici del QMSR.
- Formazione :Iniziate a formare il vostro personale sulle nuove normative per garantire che tutti i soggetti coinvolti siano a conoscenza dei cambiamenti e comprendano i loro ruoli nel mantenimento della conformità.
- Integrazione: Iniziate a integrare i nuovi requisiti QMSR nelle vostre operazioni quotidiane per rendere la transizione più agevole.
Anno 2:
- Proseguire con l'implementazione delle modifiche al sistema qualità, assicurando che tutti gli aggiornamenti siano pienamente integrati e operativi.
- Effettuare audit interni approfonditi per verificare che gli aggiornamenti siano efficaci e che il sistema qualità sia pienamente allineato ai requisiti QMSR.
- Affrontare tempestivamente qualsiasi risultato delle verifiche interne per garantire che tutti gli aspetti del sistema qualità siano conformi.
- Entro la fine del secondo anno, il vostro sistema qualità dovrebbe essere pienamente conforme al QMSR, e dovreste essere preparati per le ispezioni USFDA con la certezza che non ci saranno problemi importanti.
Seguendo questa roadmap, i produttori non solo possono soddisfare i requisiti della USFDA ma anche stabilire un sistema di qualità robusto che sia efficiente, standardizzato e riconosciuto a livello globale. Questo approccio proattivo aiuterà a garantire una transizione agevole alle nuove normative e a mantenere i più alti standard di qualità e sicurezza per i dispositivi medici.
Conclusione: Adottare misure proattive
Prepararsi alle ispezioni della USFDA secondo la nuova regola QMSR non significa solo evitare sanzioni, ma migliorare la sicurezza e l'efficacia dei dispositivi. Armonizzandosi con la ISO 13485, la USFDA sta stabilendo aspettative più elevate, ma offre anche un percorso verso una conformità globale più snella. I produttori che iniziano ad adattarsi precocemente dovrebbero concentrarsi su aree chiave come la gestione del rischio e la sorveglianza post-commercializzazione, e assicurarsi che i loro sistemi di qualità siano aggiornati e robusti, il che non solo soddisferà le aspettative normative ma migliorerà anche il loro vantaggio competitivo sul mercato.

