
La pubblicità farmaceutica, inclusa la pubblicità diretta al consumatore, è regolamentata dall'Office of Prescription Drug Promotion (OPDP) della United States Food and Drug Administration (US FDA), dall'Advertising and Promotional Labeling Branch (APLB) presso il Center for Drug Evaluation and Research (CDER) e dal Center for Biologics Evaluation and Research (CBER), rispettivamente. Le informazioni presentate all'OPDP e all'APLB devono essere accurate, etiche e non fuorvianti. Ulteriori informazioni sui benefici e sui rischi del prodotto devono essere incluse nella presentazione. Gli Uffici esaminano anche i materiali promozionali presentati all'Agenzia.
Nell'aprile 2022, la US FDA ha pubblicato linee guida sulle presentazioni per l'etichettatura promozionale e il materiale pubblicitario. Le linee guida aiutano a comprendere la presentazione elettronica nel Modulo 1 dell'eCTD, utilizzando la versione 3.3 o superiore del file backbone regionale US. Nel documento è elencata una menzione dei tipi di materiali promozionali non soggetti alla presentazione elettronica obbligatoria ai sensi della sezione 745A. Le copie cartacee di tutti i tipi di presentazione promozionale saranno accettate fino a ventiquattro mesi dopo la pubblicazione delle linee guida.
Eccezione
Il documento afferma che le presentazioni ai sensi della sezione 505(b), (i) o (j) del Federal Food, Drug, and Cosmetic Act (FD&C Act) e le presentazioni ai sensi della sezione 47 351(a) o (k) del Public Health Service (PHS) Act devono essere presentate in formato elettronico come definito dalla FDA. Questo documento non è soggetto alle usuali restrizioni dei regolamenti sulle buone pratiche di guida della FDA in quanto non è legalmente stabilito per responsabilità esecutive. Pertanto, la parte di questa guida che stabilisce il requisito per le presentazioni elettroniche ai sensi della sezione 745A(a) del FD&C Act ha un effetto vincolante, come indicato dall'uso delle parole "deve", "dovrà" o "richiesto".
La FDA esamina il materiale promozionale redatto entro quarantacinque giorni dalla presentazione volontaria da parte degli sponsor. Per qualsiasi domanda relativa al prodotto sollevata da professionisti sanitari, consumatori, sponsor di farmaci o studi legali, l'OPDP concede agli sponsor di rispondere entro trenta giorni di calendario.
Definizione di Materiale Promozionale
L'espressione 'materiale promozionale' si riferisce a etichette e materiali pubblicitari promozionali, indipendentemente dal formato, dal modo o dal mezzo attraverso cui vengono comunicati. La FDA generalmente supervisiona due tipi di etichettatura per i farmaci:
- Etichettatura richiesta dalla FDA
- Etichettatura promozionale
Secondo la sezione 201(m) della FDA, l'etichettatura è definita come “tutte le etichette, oltre a quelle scritte, stampate o grafiche impresse su qualsiasi contenitore, involucro, o su qualsiasi articolo o che accompagnano tale articolo.” Il linguaggio utilizzato in 'che accompagnano tale articolo' è considerato un'interpretazione o una spiegazione del materiale promozionale, come dichiarato dalla Corte Suprema degli US.
Criteri per la presentazione di materiale promozionale per la revisione
- Inclusione di numeri NDA, ANDA o BLA appropriati
- Nei casi in cui i richiedenti necessitano di revisione immediata, indirizzare le presentazioni al Project Manager OPDP
- Dal modulo FDA 2253, assegnare il tipo di materiale più specifico per rappresentare il materiale promozionale
- Diversi tipi di materiali devono essere presentati separatamente
- Non mescolare altre presentazioni con materiale promozionale
- Il materiale promozionale destinato ai professionisti sanitari deve essere presentato separatamente da quello destinato ai consumatori
Le metriche seguenti chiariscono il numero di moduli 2253 presentati e i materiali inclusi in tali presentazioni.
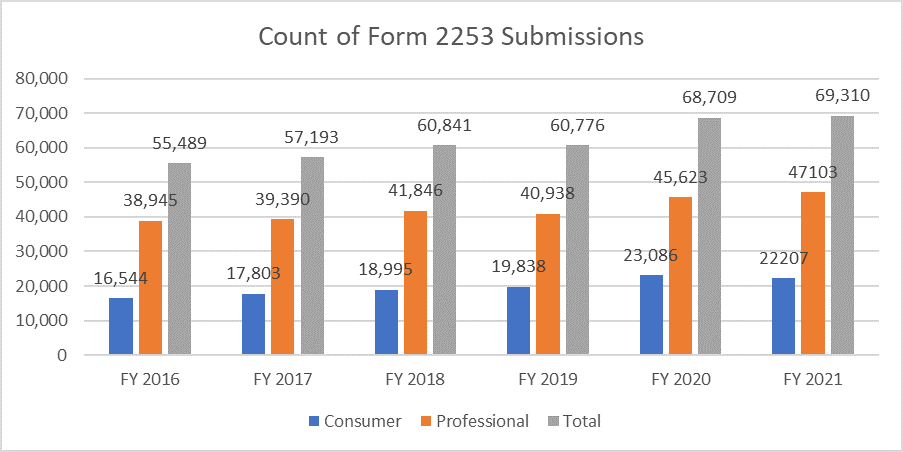
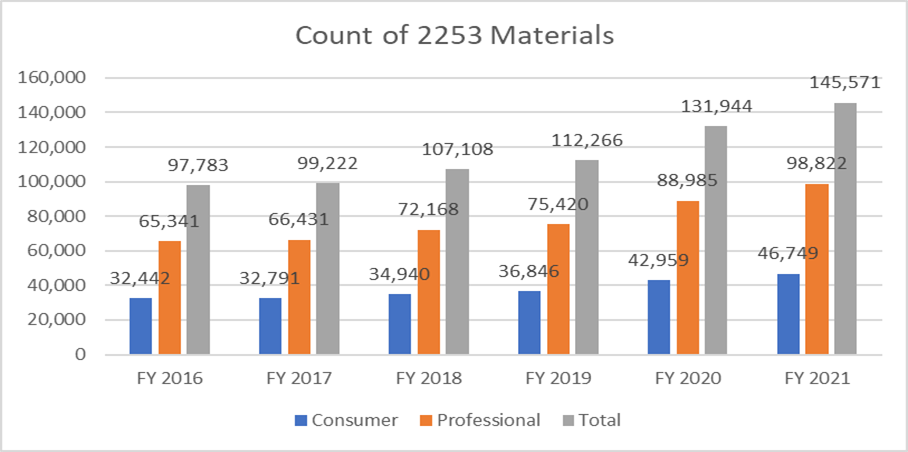
È di massima importanza che gli sponsor redigano il loro materiale promozionale secondo le linee guida fornite dalla FDA per evitare cicli di revisione multipli, dato il costo del processo. Disporre di risorse in grado di facilitare senza intoppi il processo di presentazione del materiale promozionale può consentire agli sponsor di raggiungere i loro obiettivi aziendali e di rimanere al passo con i requisiti normativi. Un partner normativo comprovato come Freyr può garantire una revisione completa del materiale promozionale e non promozionale prima della presentazione, sia in formato elettronico che non elettronico. Contatta Freyr oggi stesso per redigere materiale promozionale chiaro, conciso e conforme fin dalla prima volta.










