
La maggior parte delle organizzazioni del settore delle scienze della vita trova difficile ottimizzare il proprio processo di presentazione delle domande normative a causa dei frequenti cambiamenti nelle linee guida per la presentazione. Secondo un'analisi recente condotta dalla United States Food and Drug Administration (USFDA), il 32% delle presentazioni con dati di studio presentava problemi critici di conformità dei dati. Il processo richiede una profonda comprensione della collaborazione tra le parti interessate interne ed esterne. All'interno dell'organizzazione, i dipartimenti di produzione, ricerca e sviluppo, ricerca clinica/non clinica, QA/QC, marketing e vendite devono lavorare in armonia per accelerare il processo di approvazione dallo sviluppo iniziale fino a quando il farmaco arriva sul mercato. Il dipartimento Affari Regolatori e le Autorità Sanitarie (HA) sono in costante corrispondenza per garantire e valutare la sicurezza e l'efficacia dei farmaci per uso umano. Vediamo quali misure preliminari le organizzazioni farmaceutiche devono adottare per raggiungere l'eccellenza nelle presentazioni normative:
Allocare e impiegare risorse per ottimizzare, standardizzare e accelerare il lavoro di presentazione disorganizzato
Uno specialista delle sottomissioni partecipa su base contrattuale e può comprendere più di un tipo di sottomissione, pur essendo associato a programmi di sviluppo nel corso degli anni, assistendo nella creazione di narrazioni convincenti per il dossier. In questo modo, le organizzazioni possono più facilmente:
- Eliminare gli errori bilanciando la collaborazione tra gli stakeholder interni ed esterni
- Ridurre il ciclo di revisione dell'Autorità Competente (AC) per il processo di creazione e approvazione dei documenti.
- Preparare presentazioni complete e conformi per stare al passo con i mutevoli requisiti normativi per i diversi mercati
- Prendere atto delle istanze interessate da un'Autorità di Regolamentazione
- Essere a conoscenza dello stato di redazione, revisione e approvazione delle sottomissioni
- Miglioramento del protocollo di presentazione attuale
Semplificare la metodologia di presentazione dei dossier
La redazione di un dossier è fondamentale per la preparazione delle richieste. Si osserva che le domande di licenza per prodotti biologici (BLA) e le domande di autorizzazione per nuovi farmaci (NDA) sono composte da moltissime pagine, rendendo difficile per le autorità di regolamentazione comprendere la narrazione del dossier. Una rappresentazione strutturata di un'idea generale può aumentare la capacità del team di preparare le richieste e facilitare l'esame da parte delle agenzie.
L'uso di moduli per snellire le presentazioni consente agli esperti di analizzare cosa deve essere incluso in ogni sezione o modulo del dossier. Tale pratica facilita:
- Avvio anticipato della redazione, accelerando la preparazione delle richieste da parte dell'organizzazione.
- Utilizzo di dati pertinenti necessari per la redazione delle presentazioni.
- Utilizzo di risorse adeguate senza la necessità di redigere documenti estesi da zero per ogni presentazione.
Lavorare in collaborazione con le Autorità Regolatorie
Ogni organizzazione deve condurre riunioni regolari con le Autorità Sanitarie (AS) come prassi durante la fase iniziale dello sviluppo del prodotto. Ciò garantisce una revisione e un feedback tempestivi, con una risoluzione accelerata dei commenti da parte dell'AS e, di conseguenza, del processo di approvazione. Ciò non solo crea un buon rapporto tra le organizzazioni e l'AS, ma aiuta anche a ottenere chiarezza in una fase iniziale della pianificazione della presentazione.
Semplificare contenuti e dati nel sistema di gestione documentale (DMS)
Un solido archivio di contenuti è previsto per gestire tutti i dati tra le diverse aree funzionali, inclusa la documentazione e le informazioni create in precedenza. Un archivio di contenuti e dati strutturati fornisce un accesso senza interruzioni ai documenti da varie aree funzionali senza alcuno sforzo aggiuntivo o la necessità di duplicare. I documenti archiviati nel DMS diventano l'unica fonte di riferimento per tutti gli stakeholder interni (scienze cliniche, CMC, non cliniche, farmacocinetica, farmacodinamica, scrittura medica e operazioni cliniche). Tali contenuti e dati possono essere utilizzati per creare contenuti locali basati sui requisiti regionali. Ottimizzazione delle Presentazioni Normative tramite la Gestione Strutturata di Contenuti e Dati
Adottare tecnologia e automazione per ridurre il lavoro ripetitivo e gli errori
Le organizzazioni possono sfruttare la tecnologia utilizzando la sua funzione di aggiornamento automatico e controllo qualità delle Tabelle, Elenchi e Figure (TLF) presenti nel testo rispetto ai dati di origine, per accelerare il processo di documentazione. In questo modo, ogni volta che vengono apportate modifiche alle tabelle di origine esistenti, le TLF nel testo vengono aggiornate di conseguenza. Ciò contribuisce a ridurre le ore di lavoro complessive, a risparmiare tempo sul percorso critico e a migliorare l'accuratezza dei dati.
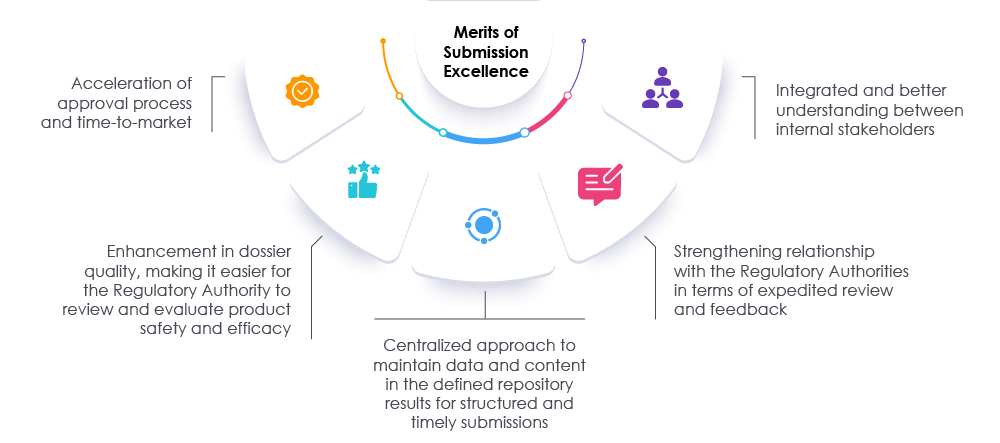
L'adozione di misure appropriate, insieme a revisioni tempestive dei dossier e dei dati, può aiutare sia le autorità di regolamentazione che le organizzazioni ad accelerare il processo di presentazione. Questo approccio riduce il tempo di immissione sul mercato per soddisfare le esigenze sia dei pazienti che del settore. Un partner normativo collaudato può assistere le organizzazioni nel ripensare, rivalutare e modificare gli approcci attuali per la preparazione delle presentazioni. I nostri esperti di Freyr possono facilitare un percorso verso l'eccellenza nelle presentazioni normative aumentando la visibilità all'interno dell'organizzazione e promuovendo la conformità generale, consentendo all'organizzazione di avere successo nel mercato odierno delle scienze della vita. Consultare Freyr.










