
La gestione delle modifiche post-approvazione è un aspetto essenziale, ma spesso trascurato, della gestione del ciclo di vita dei prodotti farmaceutici. Una volta che un prodotto farmaceutico è stato approvato, deve continuare a soddisfare gli standard normativi per garantirne la sicurezza, l'efficacia e la qualità. Ciò comporta l'introduzione di modifiche necessarie al prodotto, al suo processo di fabbricazione o al suo confezionamento.
Questi cambiamenti spesso vanno dal miglioramento dell'efficienza produttiva, all'affrontare problemi di sicurezza o al rispetto dei requisiti regolatori più recenti e/o nuovi. Tuttavia, la gestione di questi cambiamenti presenta diverse sfide nascoste che possono influenzare il ciclo di vita del prodotto e la sua presenza sul mercato. In un tale contesto, è necessaria la presenza di un partner regolatorio per supervisionare tale gestione del processo di cambiamento e condurre senza intoppi le operazioni regolatorie.
Ostacoli per un'azienda farmaceutica
Gestire le modifiche post-approvazione comporta complessità che variano significativamente tra le diverse regioni, creando ostacoli alla conformità. Inoltre, garantire l'integrità dei dati, coordinare molteplici parti interessate e gestire un'ampia documentazione può essere scoraggiante. La mancata gestione efficace di questi aspetti può comportare la non conformità normativa, il ritiro dei prodotti e gravi danni alla reputazione e alle operazioni.
Poche sfide nella gestione delle modifiche post-approvazione
- Complessità Regolatoria
- Diverse autorità sanitarie (HA) in tutto il mondo hanno requisiti unici per le modifiche post-approvazione, il che rende necessaria una profonda comprensione delle linee guida e delle tempistiche specifiche di ciascuna regione. Comprendere queste differenze è fondamentale per presentazioni tempestive e di successo.
- I ritardi nella comprensione di queste normative possono portare a notevoli battute d'arresto nel ciclo di vita del prodotto.
- Integrità dei dati
- Garantire l'accuratezza e l'integrità dei dati presentati per le modifiche post-approvazione è fondamentale. Dati inaccurati o incompleti possono portare a rifiuti normativi e ritardi significativi.
- Mantenere elevati standard di qualità dei dati implica rigorosi processi di convalida e frequenti audit per prevenire discrepanze.
- Coordinamento delle Parti Interessate
- La gestione efficace delle modifiche post-approvazione implica il coordinamento tra i team interni (come R&S, produzione e garanzia di qualità) e i partner esterni (come le organizzazioni di produzione a contratto).
- L'utilizzo di strumenti di gestione dei progetti e riunioni interfunzionali regolari può migliorare la collaborazione e garantire che tutte le parti siano allineate.
- Documentazione
- Una documentazione dettagliata e precisa è fondamentale per dimostrare la conformità e facilitare processi di revisione fluidi.
- Al contrario, pratiche di documentazione scadenti possono portare a richieste normative, richieste di dati aggiuntivi e ritardi nella presentazione.
- Gestione del Rischio
- La gestione proattiva del rischio aiuta ad anticipare le sfide e a implementare soluzioni per garantire che il processo di presentazione proceda senza intoppi.
- Un piano efficace di gestione del rischio riduce al minimo la probabilità di ostacoli normativi e garantisce la conformità continua.
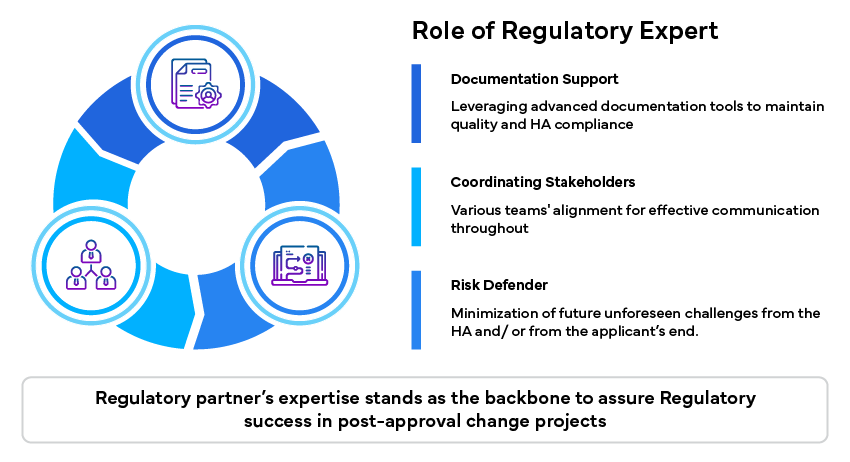
Ruolo dell'Esperto Normativo
Esperti normativi svolgono un ruolo significativo nel superare queste sfide fornendo competenze e supporto specializzati:
Riepilogo
Una gestione efficace delle modifiche post-approvazione è essenziale per mantenere la qualità, la sicurezza e l'efficacia dei prodotti farmaceutici. Navigare le complessità normative è necessario per ottenere le approvazioni di gestione delle modifiche dalle Autorità Sanitarie. Gli esperti normativi forniscono un supporto inestimabile nel superare queste sfide offrendo la loro esperienza, facilitando il coordinamento e mitigando i rischi. Sfruttando le loro capacità, i richiedenti possono garantire una gestione efficace delle modifiche post-approvazione e mantenere la presenza dei loro prodotti sul mercato.










