
Il Programma di Audit Unico per i Dispositivi Medici (MDSAP) consente a un'Organizzazione di Audit (AO) riconosciuta di condurre un singolo audit del Sistema di Gestione della Qualità (QMS) di un produttore di dispositivi medici. Fornisce i requisiti normativi pertinenti per cinque paesi, ovvero Brasile (ANVISA), STATI UNITI D'AMERICA (FDA), Giappone (PMDA), Canada (Health Canada) e Australia (TGA). Oltre alle autorità di regolamentazione partecipanti, diversi altri partner internazionali (gli osservatori ufficiali e i membri affiliati) sono coinvolti nell'MDSAP.
La certificazione MDSAP è obbligatoria per Health Canada per i dispositivi di Classe II, III e IV ma è volontaria per gli altri quattro paesi. Ha promosso la trasparenza e l'allineamento normativo tra le autorità partecipanti e ha minimizzato la necessità di audit multipli, risparmiando così tempo e risorse dei produttori di dispositivi medici. Per darti una migliore prospettiva sul programma MDSAP, abbiamo cercato di rispondere alle quindici domande più frequenti.
- Perché è stato sviluppato il programma MDSAP quando esiste una certificazione ISO 13485 accettata a livello globale?
L'MDSAP è stato sviluppato per ridurre l'onere degli audit normativi per i produttori di dispositivi medici e per promuovere un maggiore allineamento degli approcci normativi e dei requisiti tecnici basati su standard internazionali e migliori pratiche. Si concentra sul portare coerenza, prevedibilità e trasparenza ai programmi normativi standardizzando le procedure e le pratiche dei regolatori e delle organizzazioni di audit di terze parti.
L'audit si basa sui requisiti QMS ai sensi della ISO 13485 e sui requisiti normativi del paese partecipante dove i dispositivi medici saranno commercializzati.
- Quali sono i criteri di idoneità per sottoporsi a un audit MDSAP?
Qualsiasi fabbricante di dispositivi medici che intenda commercializzare il proprio dispositivo nei paesi partecipanti può sottoporsi a un audit MDSAP. Tuttavia, ogni Autorità Regolatoria può stabilire criteri di esclusione per determinate condizioni, se necessario.
Ad esempio, in Giappone, le eccezioni per l'idoneità sono:
- Un sito di produzione registrato (RMS) che fabbrica dispositivi medici realizzati con tessuti umani/animali.
- Un RMS che produce IVD radioattivi, e
- Uno stabilimento di un Titolare dell'Autorizzazione all'Immissione in Commercio (MAH)
- L'audit MDSAP include i prodotti combinati?
Dispositivi medici che includono farmaci (sostanze medicinali) o prodotti biologici (ad esempio, materiali di origine animale resi non vitali, o tessuti, cellule, o sostanze di origine microbica o ricombinante, sangue umano o estratti di sangue umano o prodotti ematici, ecc.) sono considerati prodotti combinati e possono essere inclusi nell'ambito di un audit MDSAP.
Tuttavia, a causa delle differenze nel modo in cui questi prodotti sono regolamentati nelle giurisdizioni delle Autorità Regolatorie partecipanti, i rapporti di audit MDSAP e i documenti di certificazione potrebbero non essere considerati un'alternativa ai requisiti di ispezione e valutazione in alcune giurisdizioni.
Australia- I prodotti combinati sono soggetti a un esame a distanza della TGA nell'ambito della Valutazione di Conformità australiana. Ma un audit MDSAP efficace può ridurre le ispezioni per questi dispositivi.
Brasile, Giappone- I prodotti combinati considerati dispositivi medici sono inclusi nel MDSAP, poiché non ci sono requisiti specifici riguardo al Sistema di Gestione della Qualità.
Canada- Il modello MDSAP copre i requisiti QMS per i prodotti combinati considerati dispositivi medici.
US- Gli audit MDSAP non sono considerati alternative alle ispezioni FDA per i prodotti combinati.
- È possibile selezionare il paese oggetto dell'audit MDSAP?
Sì, l'audit viene eseguito in base all'ambito dichiarato nella domanda di servizi di certificazione. I produttori di dispositivi medici devono essere conformi alle normative solo nelle giurisdizioni in cui i loro prodotti devono essere commercializzati.
- Sono un produttore di dispositivi medici dagli US, e intendo commercializzare il mio dispositivo solo in Giappone. Sto per sottopormi a un audit MDSAP. Devo conformarmi anche ai requisiti di altri paesi?
No, i produttori di dispositivi medici sono tenuti a essere conformi ai requisiti e ai regolamenti ISO 13485 solo nelle giurisdizioni in cui i loro prodotti devono essere commercializzati.
- La mia Organizzazione di Audit (AO) e l'Organismo Notificato Europeo sono gli stessi. Posso essere sottoposto a audit per entrambi contemporaneamente?
Se il vostro AO e l'Organismo Notificato Europeo sono gli stessi, la valutazione della conformità può essere eseguita dopo aver condotto l'audit MDSAP, non contemporaneamente. Gli Organismi Notificati Europei sono osservatori per MDSAP e la valutazione della conformità è condotta secondo il EU MDR 2017/ 745. Per MDSAP, la valutazione viene eseguita secondo i requisiti della ISO 13485 e i requisiti normativi dei paesi partecipanti inclusi nell'ambito.
- Qual è la differenza tra le valutazioni di Fase I e II?
Il processo di audit iniziale MDSAP prevede due fasi. L'audit iniziale, chiamato anche audit di Certificazione Iniziale, consiste negli audit di Fase I e Fase II.
L'audit di Fase I include la revisione della documentazione e la valutazione della preparazione del fabbricante di dispositivi medici a sottoporsi a un audit di Fase II.
L'audit di Fase II viene eseguito per verificare se tutti i requisiti applicabili della ISO 13485 e altri requisiti normativi dell'autorità di regolamentazione in questione sono stati implementati.
- Quanti auditor posso aspettarmi per un audit MDSAP?
La Determinazione del Tempo di Audit specifica come determinare la durata dell'audit in loco in giorni-uomo. L'AO decide quanti auditor comporranno il team di audit. Ad esempio, un audit di sei giorni-uomo può essere completato in tre giorni da un team di due auditor.
- Come viene pianificato l'audit MDSAP?
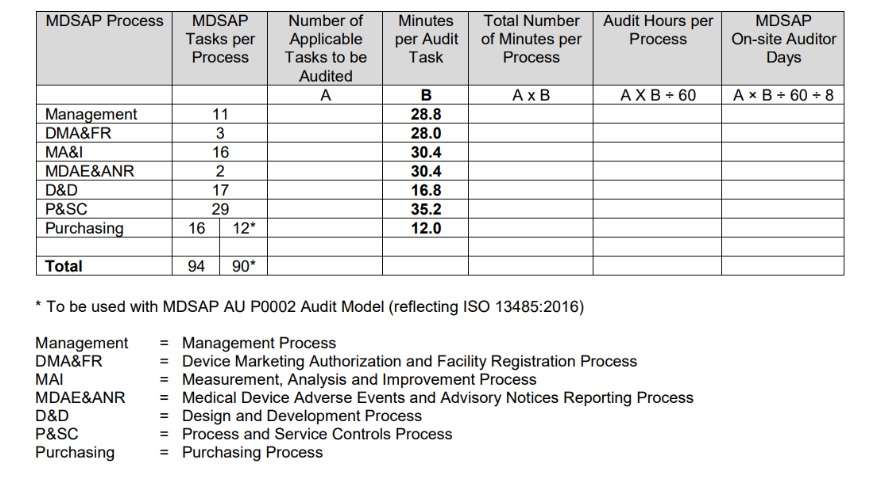
La Procedura di Determinazione del Tempo di Audit, emessa dalla FDA, riassume il processo per determinare la durata del calcolo dell'audit nella seguente tabella.
Il calcolo della durata dell'audit si basa principalmente sul numero di attività di audit applicabili associate al tipo di audit da condurre e alle attività specifiche dell'organizzazione da sottoporre ad audit.
Per informazioni dettagliate in merito, è possibile fare riferimento a MDSAP P0008007
- Esiste una guida o una checklist a cui posso accedere per garantire la conformità con un audit MDSAP?
Sì, è possibile accedere al documento MDSAP Audit Approach. È una guida ben organizzata, pubblicata dalla USFDA, che fa riferimento a sezioni specifiche della ISO 13485:2016 e alle normative pertinenti emesse dalla TGA australiana, dall'ANVISA brasiliana, da Health Canada, dal MHLW/PMDA giapponese e dalla US FDA.
- Qual è il ruolo di un osservatore in un audit MDSAP?
Un osservatore MDSAP è un'Autorità Regolatoria a cui è consentito partecipare a riunioni, valutazioni e altre attività, ma che non utilizza i risultati MDSAP. Gli osservatori sono rappresentati nel Consiglio delle Autorità Regolatorie MDSAP (RAC) da un dirigente di alto livello.
- Quali sono i prossimi passi da intraprendere se ho ricevuto un punteggio di 4 o superiore?
Il sistema di valutazione viene assegnato alle non conformità osservate durante l'audit da parte dell'AO. Un punteggio di 4 o 5 indica un rischio elevato che richieda un intervento. È necessario fornire un piano di rimedio per ogni non conformità registrata entro 15 giorni di calendario dalla data di emissione del rapporto di non conformità. Il piano di rimedio deve includere i risultati dell'indagine sulla non conformità, le sue cause e le azioni correttive pianificate per prevenire qualsiasi ricorrenza. La prova dell'implementazione del piano/azione di rimedio deve essere fornita entro trenta giorni di calendario dalla data di fine dell'audit.
- C'è una differenza nel processo di approccio all'audit da parte di un revisore interno rispetto a un AO?
MDSAP segue un approccio basato sui processi. L'Organismo di Audit (AO) tende a esaminare i collegamenti e le interconnessioni, mentre un revisore interno potrebbe concentrarsi su un singolo aspetto funzionale alla volta. Pertanto, l'AO potrebbe riscontrare una non conformità in un'area funzionale e cercare risposte in un'area funzionale diversa. Tuttavia, seguire l'approccio basato sui processi potrebbe essere problematico durante un audit interno.
- Posso fare ricorso all'AO se posso dimostrare che una non conformità registrata non è valida?
AO dispone di un processo di ricorso o di contestazione, che potete utilizzare se potete dimostrare che una non conformità registrata non è valida. Tuttavia, i gradi assegnati alle non conformità non possono essere modificati a causa di azioni correttive. Possono essere modificati solo sulla base di prove che dimostrino che non erano validi.
- Per quanto tempo è valido il certificato MDSAP?
I produttori di dispositivi medici certificati nell'ambito del programma MDSAP saranno sottoposti a audit annuale, secondo un ciclo di certificazione triennale. L'audit iniziale è un audit completo del sistema di gestione della qualità (QMS) del produttore di dispositivi medici. È seguito da audit di sorveglianza condotti annualmente per due anni consecutivi. Il ciclo ricomincia con un audit di ricertificazione nel terzo anno.
Per saperne di più sui nostri servizi MDSAP, contattate Freyr oggi stesso per fissare una chiamata con i nostri esperti.









