L'SmPC, o Riassunto delle Caratteristiche del Prodotto, è un documento legale che fa parte dell'autorizzazione all'immissione in commercio di ogni medicinale. Il documento funge da base informativa sull'uso dei medicinali per i professionisti sanitari. Le informazioni incluse nell'SmPC vengono aggiornate regolarmente in base all'emergere delle informazioni più recenti. L'SmPC contiene più informazioni di un Foglio Illustrativo. Le informazioni dell'SmPC possono essere reperite tramite le seguenti fonti:
- Siti web delle Autorità Sanitarie; come l'Agenzia Europea dei Medicinali (EMA)
- Dizionari medici
Di cosa è composto un SmPC?
- Informazioni relative all'uso del medicinale
- Informazioni qualitative e quantitative sui benefici e i rischi dei medicinali
- Informazioni sul dosaggio
- Metodo di somministrazione
- Informazioni farmacologiche
- Informazioni per la cura individuale
Struttura di un SmPC.
La struttura dello SmPC è definita dalla legislazione farmaceutica europea. Le informazioni incluse nello SmPC dovrebbero essere specifiche del prodotto e possono essere referenziate per evitare ridondanze. Dovrebbe essere documentato in un linguaggio chiaro e non dovrebbe portare ad alcuna ambiguità. Lo SmPC è diviso in 6 sezioni principali:
- Nome del prodotto
- Composizione
- Forma farmaceutica
- Dettagli clinici – Include indicazioni terapeutiche, raccomandazioni per i dosaggi e informazioni sulla sicurezza
- Proprietà farmacologiche – Tiene conto delle indicazioni terapeutiche degli elementi clinici e delle loro potenziali reazioni avverse al farmaco
- Dati farmaceutici – Include informazioni normative relative al farmaco
Secondo l'EMA, la struttura di un SmPC può essere rappresentata come segue:
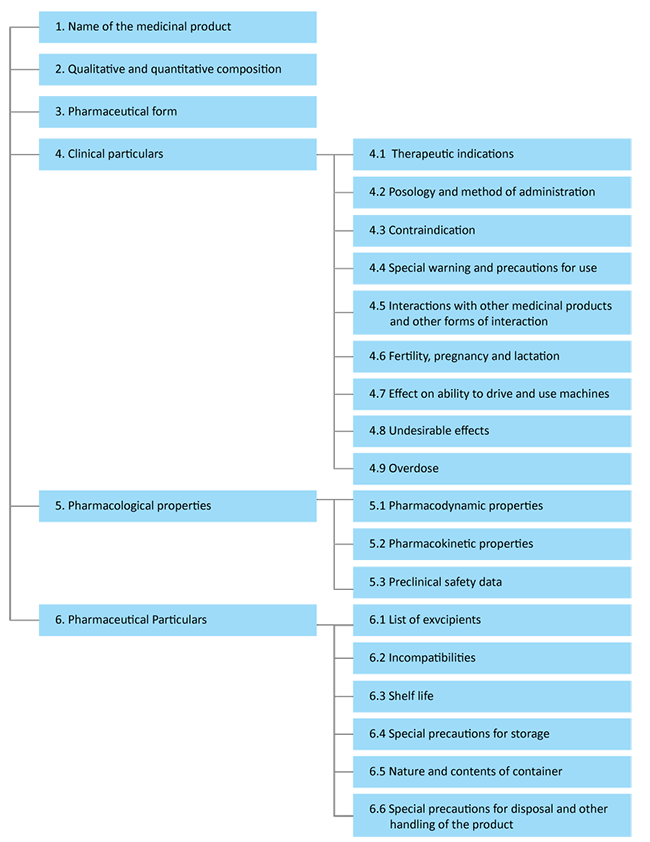
Riferimento: EMA
Quali informazioni sono escluse da un SmPC?
- Informazioni disponibili nei rapporti di valutazione pubblici (dettagli sullo sviluppo scientifico)
- Informazioni sull'indicazione non approvata
- Problemi per i quali mancano dati
- Consulenza generale sulle condizioni farmacologiche
Mantenere un SmPC è importante per il ciclo di vita di qualsiasi medicinale, in quanto fa parte della sua autorizzazione all'immissione in commercio. Pertanto, la redazione di un SmPC conforme è fortemente raccomandata. Stai cercando assistenza normativa esperta per sviluppare un SmPC? Contatta Freyr all'indirizzo sales@freyrsolutions.com.