L'obiettivo principale della US FDA è quello di esaminare costantemente e colmare il divario tra i processi normativi per l'importazione e la vendita ininterrotte di dispositivi medici nuovi e di alta qualità nel mercato US. La US FDA nel 1998 ha rilasciato un programma chiamato “Il Nuovo Paradigma 510(k): Approcci Alternativi per Dimostrare l'Equivalenza Sostanziale nelle Notifiche Premarket.” Esso intende stabilire un percorso efficiente per la presentazione 510(k) della FDA che contenga determinate modifiche all'applicazione 510(k) già approvata. Questa nuova notifica 510(k) offre tre tipi di presentazioni, vale a dire, 510(k) speciale, 510(k) abbreviato e 510(k) tradizionale. La US FDA, nel 2019, ha pubblicato un documento guida speciale 510(k) che descrive un percorso opzionale per i produttori che apportano determinate modifiche ben definite al loro dispositivo legalmente commercializzato.
Perché una 510(k) Speciale?
Quando un produttore desidera l'approvazione per le modifiche apportate a un dispositivo già commercializzato, ovvero il dispositivo esistente, può richiedere un 510(k) speciale. I principali fattori da considerare per determinare se una modifica a un dispositivo esistente possa essere appropriata per un 510(k) speciale sono i seguenti:
- La modifica riguarda il dispositivo precedente legalmente commercializzato dal richiedente.
- I dati sulle prestazioni non sono richiesti, oppure sono disponibili metodi ben consolidati, se ritenuto necessario per valutare la modifica.
- Tutti i dati sulle prestazioni a supporto di una determinazione di equivalenza sostanziale possono essere esaminati in formato riassuntivo o di analisi del rischio.
Documenti richiesti per il 510(k) speciale
- Lettera di accompagnamento
- Il nome del dispositivo legalmente commercializzato (esistente) del fabbricante e il numero 510(k).
- Una descrizione dettagliata delle modifiche apportate al dispositivo che hanno portato alla presentazione di un nuovo 510(k)
- Un confronto tra il dispositivo modificato e il dispositivo autorizzato, in formato tabellare
- Altre modifiche all'etichettatura o al design
- Un riepilogo conciso delle attività di controllo della progettazione
- Sulla base dell'analisi dei rischi, un'identificazione delle attività di verifica e/o convalida richieste per conformarsi a 21 CFR 820.30.
- Modulo delle indicazioni per l'uso
- Una dichiarazione che il proponente ha rispettato e non è attualmente in violazione dei requisiti della procedura di controllo della progettazione come specificato nel 21 CFR 820.30 e che i registri sono disponibili per la revisione su richiesta.
Tempistica di Revisione Speciale 510(k) da parte della FDA US
Secondo le linee guida della FDA “Refuse to Accept Policy for 510(k)s”, i tempi di revisione per le presentazioni speciali 510(k) sono entro trenta giorni dalla loro ricezione.
Quando richiedere lo Special 510(k)?
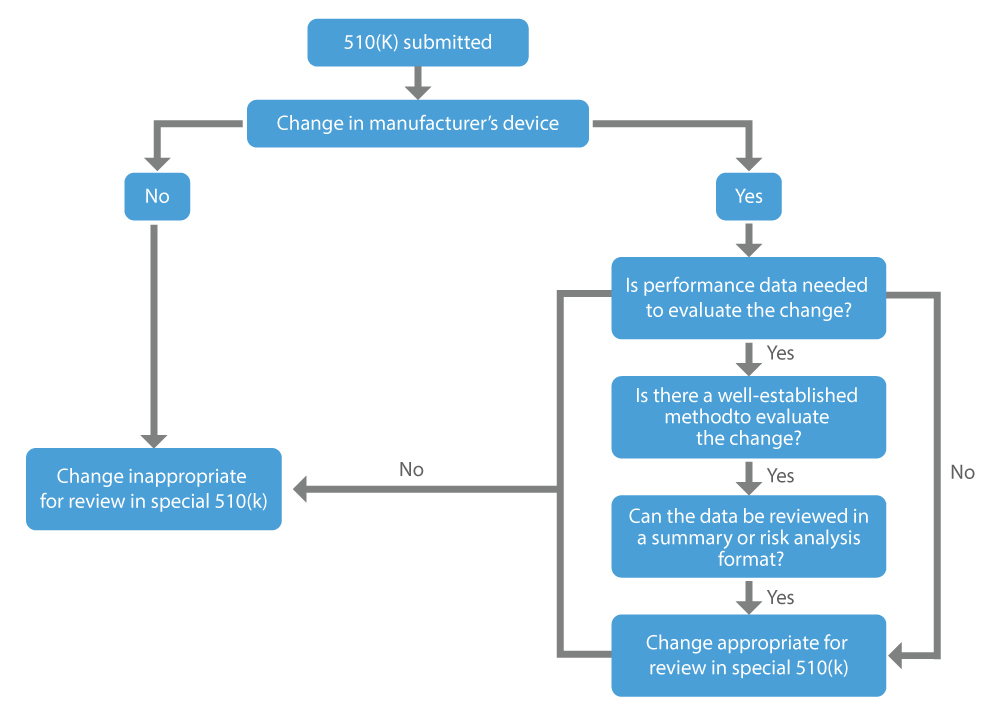
La FDA degli US si impegna costantemente per fornire dispositivi medici sicuri ed efficaci per promuovere la salute umana. Il programma Speciale 510(k) è efficiente e coerente con la procedura di revisione meno onerosa che aiuta i produttori stranieri a vendere i loro dispositivi all'interno degli STATI UNITI D'AMERICA e consente ai pazienti di accedere tempestivamente a nuovi dispositivi medici.
Per qualsiasi ulteriore chiarimento sul processo speciale 510(k) della FDA, contattate Freyr, un comprovato esperto normativo. Rimanete informati. Rimanete conformi.