
Gdy zagraniczny podmiot zajmuje się produkcją wyrobu medycznego importowanego do Stanów Zjednoczonych (US), obowiązkowe jest wyznaczenie agenta US dla tego podmiotu. Agent US służy jako punkt kontaktowy dla wszelkich komunikatów US Food and Drug Administration (US FDA) dotyczących zarejestrowanego zagranicznego obiektu. Ponieważ ta komunikacja może być pilna, niezbędne jest, aby agent US posiadał kompleksowe zrozumienie przepisów US FDA i był w stanie doradzać zagranicznemu podmiotowi w zakresie zgodności z wymaganiami US FDA dotyczącymi wyrobów medycznych. Co więcej, posiadanie niezależnego agenta US pomaga zapobiegać potencjalnym konfliktom interesów, które mogą powstać, gdy partner biznesowy zostanie wyznaczony jako agent US. W tym blogu zagłębimy się w szczegóły rejestracji zagranicznego podmiotu w US FDA.
Co to jest Rejestracja Zakładu?
Roczna rejestracja w US FDA jest obowiązkowa dla producentów kontraktowych, pierwszych importerów, firm przepakowujących/ponownie etykietujących, twórców specyfikacji itp. zakładów zajmujących się produkcją i dystrybucją wyrobów medycznych przeznaczonych na rynek US, procedura ta jest określana jako Rejestracja Zakładu (Tytuł 21 CFR Część 807).
Kto musi ubiegać się o rejestrację zakładu?
Właściciele obiektów zajmujących się produkcją i dystrybucją wyrobów medycznych przeznaczonych do użytku w US muszą dokonać corocznej rejestracji w US FDA. Rodzaje właścicieli, którzy mogą ubiegać się o rejestrację zakładu, to:
- Właściciele krajowych zakładów
- Właściciele zagranicznych zakładów
- Producenci kontraktowi
- Pierwsi importerzy
- Firmy przepakowujące/przeetykietowujące
- Twórcy Specyfikacji
Jakie są etapy procesu rejestracji zakładu?
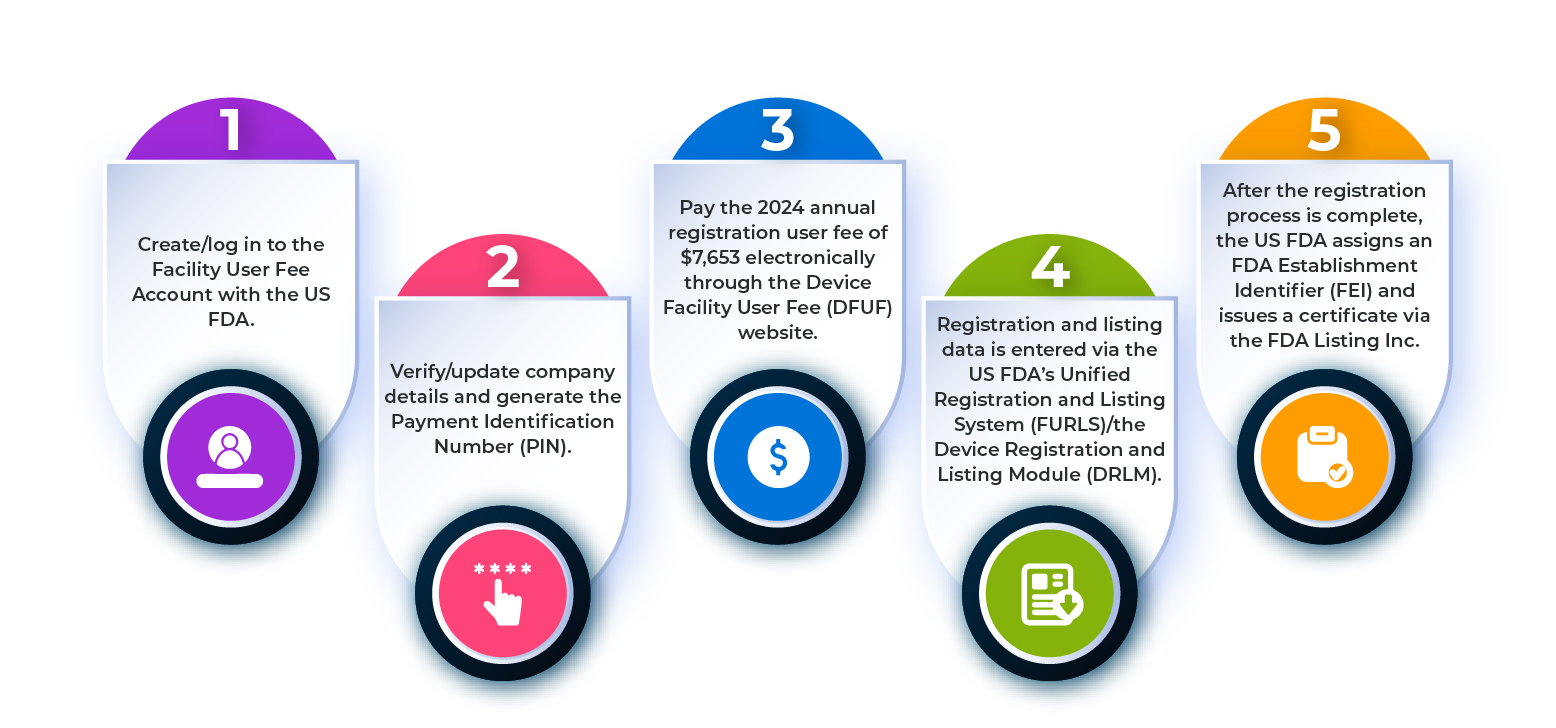
Aby zarejestrować placówkę wyrobów medycznych w US FDA, należy postępować zgodnie z krokami przedstawionymi na poniższym schemacie.
Rysunek 1: Etapy procesu rejestracji zakładu
Jakie są wymagania dotyczące rejestracji i wykazu zagranicznych placówek?
Zrozumienie znaczenia wyboru niezależnego, doświadczonego agenta US pomoże zagranicznemu podmiotowi priorytetowo traktować unikanie konfliktu interesów, co jest kluczowe dla tych podmiotów, gdy poruszają się w złożonym świecie zgodności z US FDA. Zagraniczne podmioty muszą pogłębić swoją wiedzę na temat warunków wstępnych do osiągnięcia zgodności, budować silne partnerstwa z agentami US i przygotować grunt pod płynny proces rejestracji. Poniższa tabela przedstawia wymagania dotyczące rejestracji i wpisu na listę w oparciu o działalność zagranicznego podmiotu. Wskazuje również, które działania wiążą się z opłatą za rejestrację podmiotu.
Tabela 1: Wymagania dotyczące rejestracji i wpisu do wykazu w oparciu o działalność zagranicznego podmiotu
| Działalność | Zarejestruj się | Lista | Opłać opłatę | |
| Producent na zlecenie (w tym firmy pakujące na zlecenie) | TAK 807.40 (a) | TAK 807.40 (a) | Tak | |
| Firma sterylizująca na zlecenie | TAK 807.40 (a) | TAK 807.40 (a) | Tak | |
| Producenci wyrobów na zamówienie | TAK 807.20 (a) (2) | TAK 807.20 (a) (2) | Tak | |
| Urządzenie badane w ramach zwolnienia z wymogu badania wyrobu medycznego (IDE) | NO 812.1 (a) | NO 812.1(a),807.40 (c) | NIE | |
| Zagraniczny eksporter urządzeń znajdujący się w obcym kraju | TAK 807.40 (a) | TAK 807.40 (a) | Tak | |
| Zagraniczni producenci (w tym monterzy zestawów) | TAK 807.40 (a) | TAK 807.40 (a) | Tak | |
| Prowadzi akta skarg zgodnie z wymogami 21 CFR 820.198. | Tak | Tak | Tak | |
| Producent akcesoriów, które są pakowane lub etykietowane do dystrybucji komercyjnej w celach związanych ze zdrowiem dla użytkownika końcowego | TAK 807.20 (a) (5) | TAK 807.20 (a) (5) | Tak | |
| Producent komponentów, które są dystrybuowane wyłącznie do producenta gotowego wyrobu | NO 807.65 (a) | NIE | NIE | |
| Podmioty dokonujące ponownego etykietowania lub przepakowywania | TAK 807.20 (a) (3) | TAK 807.20 (a) (3) | Tak | |
| Podmiot dokonujący ponownej produkcji | Tak | Tak | Tak | |
| Podmiot przetwarzający wyrób jednorazowego użytku | TAK 807.20 (a) | TAK 807.20 (a) | Tak | |
| Twórcy Specyfikacji | Tak | Tak | Tak | |
Rejestracja placówki w US FDA jest kluczowym wymogiem dla zagranicznych placówek zaangażowanych w produkcję, sprzedaż, przepakowywanie lub import wyrobów medycznych w US. Rejestracja ta zapewnia zgodność z rygorystycznymi przepisami i standardami US FDA. Freyr zapewnia cenne wsparcie placówkom poszukującym fachowej pomocy podczas procesu rejestracji placówki. Wykorzystując swoją wiedzę i zrozumienie przepisów US FDA, Freyr pomaga zagranicznym placówkom w spełnianiu wymogów zgodności, co ostatecznie prowadzi do płynniejszego i bardziej efektywnego wejścia na rynek wyrobów medycznych w US. Aby dowiedzieć się więcej o procesie rejestracji placówki w US FDA, skontaktuj się z nami już dziś. Bądź na bieżąco! Zachowaj zgodność!









