24 września 2016 r.; biorąc pod uwagę, że termin na zapewnienie zgodności z wymogami unikalnego identyfikatora wyrobu (UDI) dla wyrobów klasy II upływa już za miesiąc, zakładamy, że wszyscy producenci wyrobów medycznych są dobrze przygotowani i posiadają kompleksowy plan działania w zakresie regulacji. Oprócz solidnego zrozumienia wymogów zarządzania, od producentów oczekuje się gotowości do audytu w zakresie zgodności. Od walidacji rekordów identyfikatora wyrobu (DI) i identyfikatora produktu (PI) po pomyślne zgłoszenia do GUDID, powinni być zaznajomieni z danymi do przesłania i procedurami, których należy przestrzegać. Zarówno przed zgłoszeniem, jak i po nim, posiadanie lepszej wiedzy na temat procedur może chronić producentów przed wyzwaniami związanymi z agregacją danych, przesyłaniem rekordów DI, zarządzaniem raportami dotyczącymi wyrobów, śledzeniem potwierdzeń od organów zdrowia itp.
Aby wyposażyć producentów w lepszą pozycję w takich scenariuszach, przedstawiamy łatwą do zrozumienia infografikę przedstawiającą wyzwania i rozwiązania w zakresie zgodności z UDI, która może zaoszczędzić Twój czas na rozszyfrowanie złożoności zgodności oraz lepsze zaplanowanie i ustrukturyzowanie planu działania.
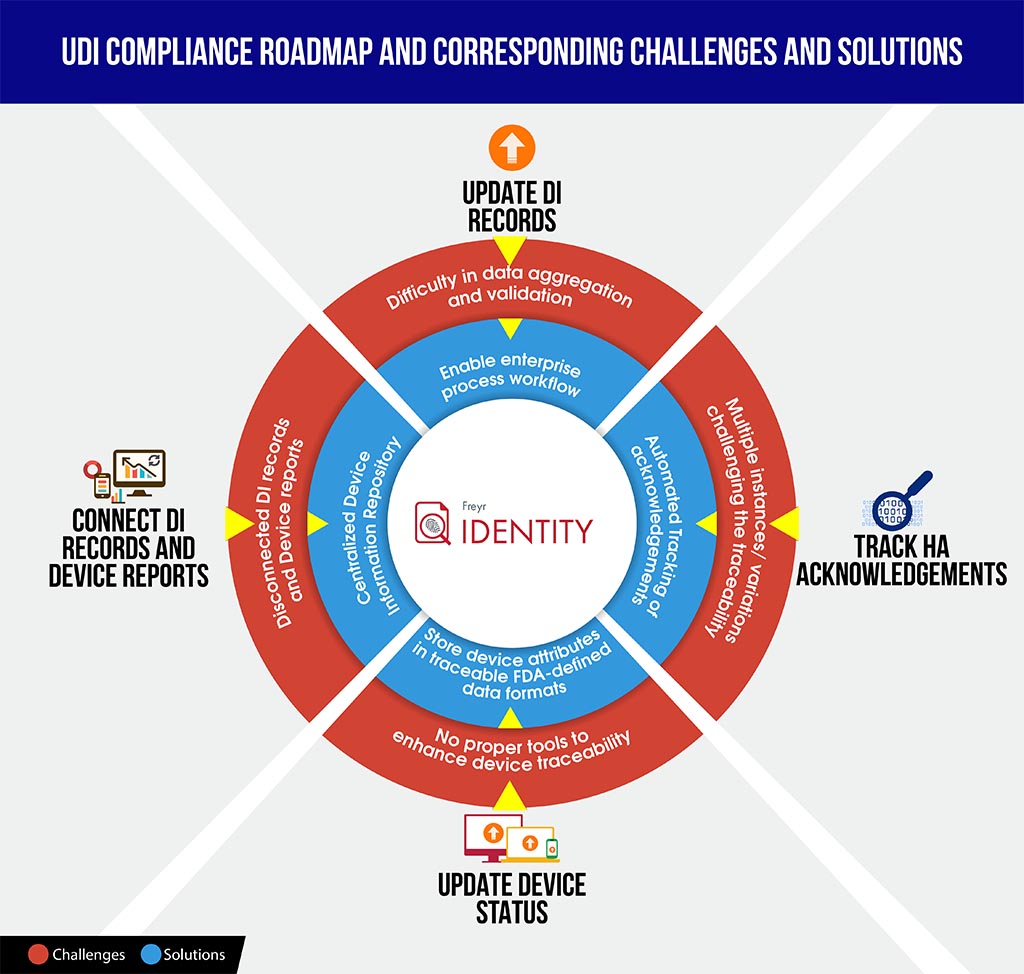
Aby sprawnie przeprowadzić Państwa organizację przez ten złożony proces zgodności, Freyr oferuje najlepsze z obu światów – oprogramowanie UDI na żądanie, w pełni konfigurowalne, Freyr IDENTITY, a także Centrum Doskonałości UDI (CoE), które oferuje najlepsze w swojej klasie, ekonomiczne i konfigurowalne usługi UDI, dostosowane do Państwa unikalnych i wymagających potrzeb.









