Zgłoszenia zaplanowane na 24 września 2016 r.
Teraz, gdy wdrożono drugą fazę zgodności z UDI dla wyrobów medycznych klasy III I/LS/LS, wielu producentów wyrobów, zwłaszcza typu klasy II, zastanawia się, jak najlepiej przygotować się na termin składania danych dla wyrobów klasy II, przypadający na 24 września 2016 r. Aby ich uprzedzić, w Freyr zidentyfikowaliśmy niektóre z warunków wstępnych, które powinni wziąć pod uwagę, aby dostosować wyroby klasy II do wymogów UDI określonych przez FDA.
Nowe rozporządzenie wymaga, aby wszystkie wyroby medyczne klasy II były oznakowane i pakowane z unikalnym identyfikatorem wyrobu (UDI) i wprowadzane do Globalnej Bazy Danych Unikalnych Identyfikatorów Wyrobów (GUDID) FDA. Biorąc pod uwagę zmienność wymagań dotyczących zgodności w połączeniu z krótszymi terminami składania wniosków, wyzwaniem dla producentów wyrobów jest poznanie szczegółów procesów zgodności. Jednocześnie muszą oni zapewnić, aby żadna z kluczowych cech wyrobu nie została pominięta podczas zbierania rozproszonych danych o wyrobie z różnych systemów i uzgadniania ich w arkuszach kalkulacyjnych w celu tworzenia raportów zgodności.
Aby pomóc producentom wyrobów łatwo przejść przez ten krytyczny czasowo i złożony proces zgodności, bez błędów, Freyr opracował następujące warunki wstępne, których należy przestrzegać.
Określ datę zgodności z UDI: Od czasu wydania przez FDA ostatecznej zasady, niektóre daty zgodności urządzeń zostały zmienione i przedłużone. Aby skrupulatnie zaplanować strategie i procesy zgodności oraz uniknąć pośpiesznych zmian w ostatniej chwili, etykietujący powinni określić dokładną datę zgodności.
Data zgodności dla urządzeń klasy II Wymogi zgodności 24 września 2016Urządzenia klasy III, które muszą być oznakowane UDI, muszą posiadać UDI jako trwałe oznakowanie na samym urządzeniu, jeśli jest ono przeznaczone do wielokrotnego użytku i do ponownego przetworzenia przed każdym użyciem. Etykiety i opakowania wyrobów medycznych klasy II muszą zawierać UDI Daty na etykietach tych wyrobów muszą być sformatowane zgodnie z wymaganiami Klasa II samodzielne oprogramowanie musi dostarczyć swój UDI zgodnie z wymogami Dane dotyczące wyrobów klasy II, które muszą być oznakowane UDI, należy przesłać do bazy danych GUDID Dla większości wyrobów, termin zgodności dla bezpośredniego znakowania różni się od pozostałych wymagań. W zależności od kategorii produktu, czy jest przeznaczony do ponownego użycia, czy do ponownego przetworzenia, określ termin zgodności UDI dla bezpośredniego znakowania, jak pokazano tutaj:
Terminy zgodności dla bezpośredniego znakowania Kategoria wyrobu – Ponownie używane i przetwarzane 24 wrz 2015 Urządzenia podtrzymujące i wspomagające życie, niezależnie od klasy wyrobu. 24 września 2016 Urządzenia klasy III oraz urządzenia licencjonowane na podstawie ustawy o publicznej służbie zdrowia 24 września 2018 Wyrób klasy II 24 września 2020 Urządzenia klasy I i urządzenia niesklasyfikowane Oceń potrzebę bezpośredniego oznakowania numeru UDI: Wszystkie wyroby medyczne, które są używane więcej niż raz lub które mają być ponownie przetwarzane przed każdym użyciem, muszą posiadać bezpośrednie oznakowanie UDI. Wyjątek stanowią wyroby do implantacji, które nie wymagają bezpośredniego oznakowania zgodnie z zasadą UDI. Wyroby jednorazowego użytku, nawet jeśli są ponownie przetwarzane, również nie muszą posiadać trwałego UDI – 21 CFR 801.45(d)(3). Dlatego należy ocenić potrzebę bezpośredniego oznakowania w oparciu o kategorię produkowanych wyrobów medycznych.
- Plan zapewnienia kompleksowej zgodnościNależy zapoznać się z wymogami FDA dotyczącymi konkretnych produktów, aby zapewnić zgodność. Przeprowadź dokładną analizę luk, aby zidentyfikować braki związane z danymi lub technologią, co pozwoli sprostać niektórym z głównych wyzwań w procesie dotrzymywania ścisłych terminów FDA. Niektóre z wyzwań mogą obejmować uzyskanie informacji DI lub PI oraz zarządzanie dużymi ilościami nieustrukturyzowanych danych z różnych źródeł. Zamiast pracować do późna, aby w ostatniej chwili uzgodnić wszystkie dane dotyczące wyrobów medycznych, zaplanuj kompleksową zgodność z wyprzedzeniem, korzystając ze sprawdzonych systemów i narzędzi wspierających integrację danych, jakość danych i zarządzanie danymi.
![]()
Uzyskaj numer DI i członkostwo w Agencji: UDI składa się z Identyfikatora Urządzenia (DI – unikalny numer oparty na wersji lub modelu urządzenia) oraz Identyfikatora Produktu (PI – zawiera numer partii, numer seryjny lub datę ważności). Część DI numeru UDI będzie służyć jako klucz główny do wyszukiwania informacji o urządzeniu w GUDID. Aby przypisać DI, FDA akredytowała trzy Agencje Wydające – GS1, HIBCC i ICCBBA. W tym scenariuszu etykietujący muszą uzyskać członkostwo w jednej z agencji, aby otrzymać numer DI, który należy wprowadzić do GUDID FDA.
![]()
Identyfikator Atrybuty Agencje wydające UDI DI (Identyfikator Urządzenia – Dane Statyczne)
Wymaga synchronizacji z GUDIDUnikalny numer
Producent
Producent wyrobu
Model wyrobu
GSI
HIBCC
ICCBBAPI (Identyfikator Produktu – Dane Dynamiczne)
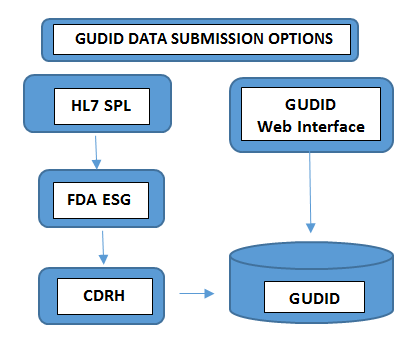
Wymagane na wszystkich poziomach opakowaniaNumer partii, Numer seryjny, Data produkcji, Data ważności, - Prześlij DaneSposób przesyłania danych do GUDID zależy od liczby obsługiwanych portfolio produktów. Producenci wyrobów z minimalną liczbą urządzeń decydują się na ręczne przesyłanie informacji UDI za pośrednictwem bezpłatnego interfejsu internetowego GUDID FDA. W tym przypadku, za pośrednictwem bezpiecznego interfejsu internetowego GUDID, można przesłać tylko jeden rekord DI naraz. W innym przypadku, producenci z większą liczbą portfolio produktów wybierają opcję przesyłania HL7 SPL, aby elektronicznie zbierać dane i konwertować skonsolidowane dane do formatu SPL przed przesłaniem ich do Electronic Submission Gateway (ESG) FDA, używając numeru DUNS. Należy pamiętać, że konto GUDID nie jest zależne od typu przesyłania. Konto służy do identyfikacji użytkownika, czyli podmiotu odpowiedzialnego za etykietowanie, aby umożliwić przesyłanie danych dotyczących wyrobów za pomocą obu opcji.
![]()
- Załóż Konto GUDID: Etykieciarz / producent wyrobów medycznych wymaga jednego lub więcej kont GUDID w zależności od liczby przypisanych ról; między innymi koordynator GUDID, użytkownik wprowadzający dane itp. Aby jednak autoryzować każdą rolę do wprowadzania danych, producent potrzebuje zgody FDA przed utworzeniem konta. Proces tworzenia odpowiedniego konta GUDID polega na wysłaniu prośby e-mail do FDA, po czym wnioskodawca, czyli Ty, otrzyma dokument z prośbą o utworzenie konta do wypełnienia. Po odesłaniu wypełnionego dokumentu do FDA pocztą elektroniczną, agencja dokona przeglądu formularza, a następnie wyśle e-mail z danymi do logowania do konta GUDID.
Wdrożenie UDI to złożony i czasochłonny proces. W trakcie spełniania wymagań FDA dotyczących UDI, producenci wyrobów medycznych napotykają wiele wyzwań związanych z zarządzaniem danymi, ich integracją i przesyłaniem. Ponieważ termin zgodności dla wyrobów klasy II upływa już za rok, Freyr zaleca firmom rozpoczęcie prac nad tym już teraz.
Aby przeprowadzić Państwa organizację przez ten złożony proces zgodności, Freyr oferuje najlepsze z obu światów – oprogramowanie UDI na żądanie, w pełni konfigurowalne, Freyr IDENTITY, a także Centrum Doskonałości (CoE), które oferuje najlepsze w swojej klasie, ekonomiczne i konfigurowalne usługi UDI, dostosowane do Państwa unikalnych i wymagających potrzeb.