Przez lata, wraz z postępem oprogramowania i cyfryzacji, nastąpiła znacząca zmiana w sposobie zarządzania i dostarczania wyrobów medycznych. Integracja oprogramowania z wyrobami medycznymi gwałtownie wzrosła, prowadząc do niesamowitych postępów w dostarczaniu rozwiązań opieki zdrowotnej w różnych dziedzinach, takich jak diagnostyka, zapobieganie chorobom oraz leczenie urazów lub chorób.
Wpływ oprogramowania na bezpieczeństwo i działanie wyrobów medycznych bywa jednak wątpliwy, zwłaszcza gdy samo urządzenie jest produktem wyłącznie programowym. Dlatego przepisy dotyczące oprogramowania wyrobów medycznych są stale weryfikowane w celu określenia, czy oprogramowanie należy uznać za wyrób medyczny (SaMD). Niedawno rada doradcza Komisji Europejskiej – Grupa Koordynacyjna ds. Wyrobów Medycznych (MDCG) – skupiła się na poprawie przepisów dotyczących oprogramowania wyrobów medycznych i opublikowała wytyczne opisujące podejście, które należy zastosować przy określaniu, czy oprogramowanie jest wyrobem medycznym, czy nie. Co zawierają te wytyczne? Przyjrzyjmy się.
Zakres Wytycznych
Wytyczne MDCG obejmują zarówno oprogramowanie wyrobów medycznych, jak i oprogramowanie wyrobów medycznych do diagnostyki in vitro (IVD). Zgodnie z dokumentem, oprogramowanie wyrobu medycznego (MDSW) jest definiowane jako oprogramowanie przeznaczone do użytku samodzielnie lub w połączeniu, w celu określonym w definicji „wyrobu medycznego” w Rozporządzeniu w sprawie wyrobów medycznych 2017/745 (MDR) lub Rozporządzeniu w sprawie wyrobów medycznych do diagnostyki in vitro 2017/746 (IVDR). Określa ono kryteria, które należy zastosować do ustalenia, czy oprogramowanie podlegające przeglądowi jest wyrobem medycznym, czy też nie, i ma na celu dostarczenie dodatkowych wyjaśnień i zaleceń dotyczących MDSW dla producentów wyrobów medycznych i innych stron.
Po pierwsze, wytyczne określają najważniejsze terminy używane w kontekście MDSW, które obejmują:
Przeznaczenie: Zastosowanie, do którego wyrób jest przeznaczony zgodnie z danymi dostarczonymi przez producenta na etykiecie, w instrukcji używania, w materiałach promocyjnych lub sprzedażowych, lub oświadczeniach, a także zgodnie z określeniem producenta w ocenie klinicznej.
Akcesorium: Artykuł, który, choć sam w sobie nie jest wyrobem medycznym, jest przeznaczony przez producenta do użytku wraz z jednym lub kilkoma wyrobami medycznymi, aby umożliwić ich użycie zgodnie z przeznaczeniem lub wspomóc funkcjonalność wyrobu medycznego w odniesieniu do jego przeznaczenia. Dodatkowo, MDCG wspomina, że akcesorium w postaci oprogramowania może sterować lub wpływać na użycie wyrobu medycznego, a instrukcje użytkowania i inna dokumentacja dostarczona przez producenta powinny zawierać szczegóły dotyczące sposobu wyboru odpowiedniego oprogramowania i akcesoriów.
Oprogramowanie: Oznacza zestaw instrukcji, które przetwarzają dane wejściowe i tworzą dane wyjściowe.
Określanie oprogramowania wyrobów medycznych
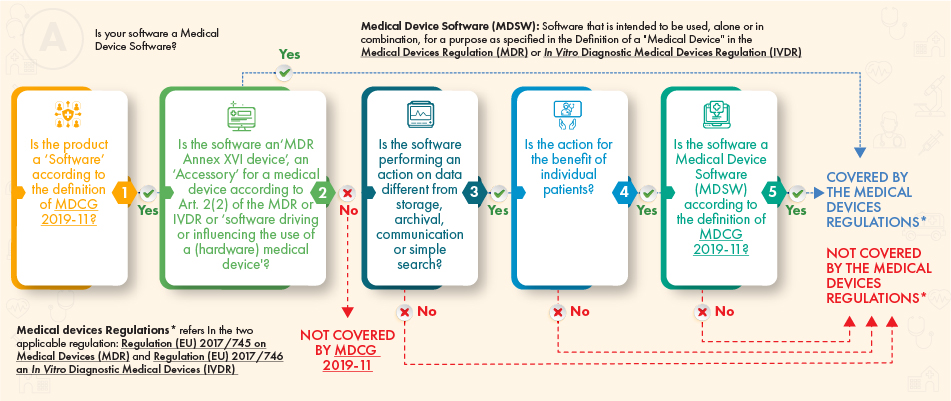
Zgodnie z powyższym schematem wytycznych, przedmiotowe oprogramowanie powinno podlegać regulacji, jeśli spełnia następujące kryteria:
- Definicja wyrobu medycznego, akcesorium do niego, lub napędza działanie wyrobu medycznego, lub
- Wykonuje dodatkowe przetwarzanie danych (nie tylko przechowywanie lub komunikację), a jego działanie przynosi korzyści pacjentom i spełnia definicję oprogramowania wyrobu medycznego zgodnie z wytycznymi MDCG.
Określenie oprogramowania dla wyrobów medycznych do diagnostyki in vitro
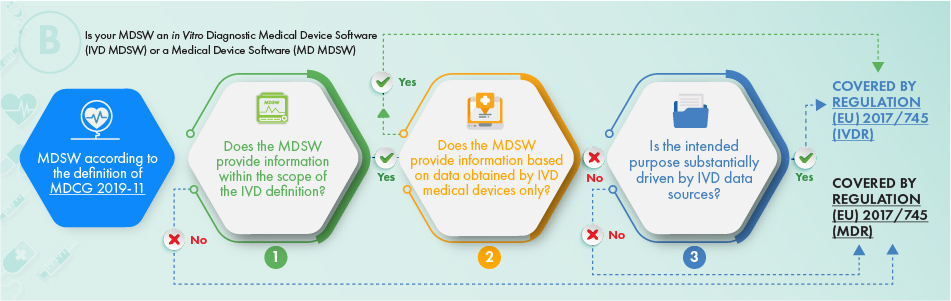
Powyższy schemat przedstawia podejście, które należy zastosować w odniesieniu do produktów przeznaczonych do diagnostyki in vitro. Aby ustalić, czy dane oprogramowanie powinno podlegać regulacji, należy wziąć pod uwagę następujące kryteria:
- Definicja wyrobu medycznego, akcesorium do niego, lub napędza działanie wyrobu medycznego, lub
- Dostarcza informacji zazwyczaj dostarczanych przez wyroby medyczne do diagnostyki in vitro i tylko informacji zebranych z wyrobu medycznego do diagnostyki in vitro, lub
- Zamierzone zastosowanie oprogramowania jest związane z kwestiami IVDR.
Zgodnie z wytycznymi MDCG, rodzaj połączenia między oprogramowaniem wyrobu medycznego a wyrobem nie wpływa na kwalifikację oprogramowania jako wyrobu zgodnie z MDR i IVDR. Oprogramowanie wyrobu medycznego może istnieć jako samodzielny produkt lub być wbudowane w urządzenie sprzętowe i wyjaśnia następujące wymogi regulacyjne:
- Biorąc pod uwagę jego kwalifikację i klasyfikację, samodzielne oprogramowanie jako wyrób medyczny musi być poddane pełnemu zakresowi procedur regulacyjnych zgodnie z obowiązującymi przepisami.
- Oprogramowanie wyrobu medycznego, które jest integralnym elementem lub częścią sprzętowego wyrobu medycznego, mogłoby zostać wprowadzone do obrotu w ramach uproszczonej procedury. Podlegałoby ono ocenie nie oddzielnie, lecz podczas ogólnej oceny samego sprzętowego wyrobu medycznego.
Podsumowując, wytyczne MDCG obejmują kluczowe aspekty związane z klasyfikacją oprogramowania wyrobów medycznych oraz określeniem wymagań regulacyjnych, które należy zastosować. Producenci wyrobów medycznych, twórcy oprogramowania i inne strony muszą przestrzegać i wdrażać zalecenia MDCG, aby zapewnić zgodność. Aby uzyskać dalsze informacje na temat klasyfikacji oprogramowania jako wyrobu medycznego, skonsultuj się z ekspertem regulacyjnym. Bądź na bieżąco. Zachowaj zgodność.









