
510(k) to zgłoszenie przed wprowadzeniem do obrotu, składane do FDA w celu wykazania, że urządzenie, które ma być wprowadzone na rynek, jest tak samo bezpieczne i skuteczne, czyli zasadniczo równoważne z urządzeniem legalnie wprowadzonym do obrotu (urządzenie referencyjne). Urządzenia o umiarkowanym ryzyku są zobowiązane do złożenia zgłoszenia 510(k), co obejmuje mniejszość urządzeń klasy I i III oraz większość urządzeń klasy II.
Istnieją trzy (03) rodzaje programów 510(k): tradycyjny, skrócony i specjalny. Ścieżka bezpieczeństwa i wydajności została wprowadzona w 2019 roku i opierała się na programie skróconym. Program eSTAR wprowadzony w 2020 roku umożliwia kompleksowe składanie dokumentacji wyrobów medycznych za pośrednictwem interaktywnego formularza PDF.
Kto potrzebuje certyfikatu 510(k)?
510(k) to zasadniczo nazwa procesu/ścieżki, którą przechodzą producenci wyrobów medycznych zamierzający wprowadzić na rynek swoje wyroby o umiarkowanym do wysokiego ryzyka w US, aby wykazać, że produkt wprowadzany na rynek jest tak samo bezpieczny i skuteczny jak wyrób legalnie wprowadzony do obrotu.
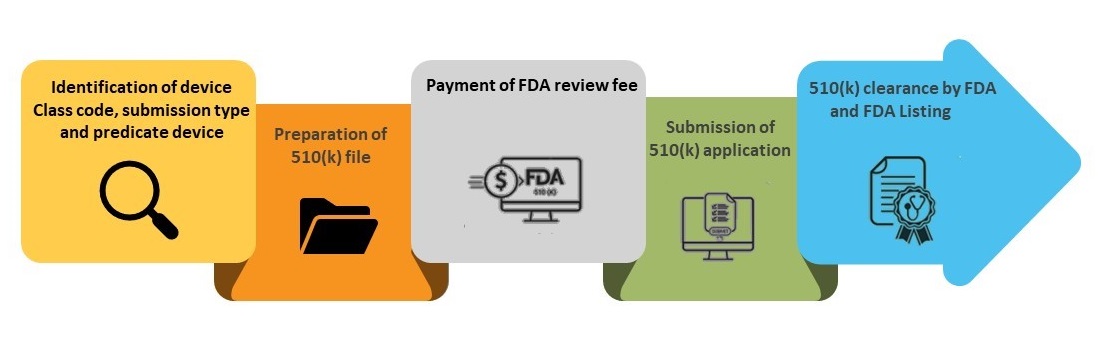
Poniżej przedstawiono szczegółowy proces krok po kroku uzyskania zatwierdzenia 510(k).
Krok 1 – Identyfikacja kodu klasy wyrobu, typu zgłoszenia oraz wyrobu referencyjnego
- Zidentyfikuj kod produktu i numer regulacji - Aby określić wymagania testowe dla 510(k), należy najpierw zidentyfikować kod produktu i numer regulacji. Można rozpocząć wyszukiwanie w bazie danych FDA, aby znaleźć 7-cyfrowy numer regulacji, dla którego identyfikacja odpowiada zamierzonemu zastosowaniu danego wyrobu.
- Kod produktu FDA składa się z trzech (03) liter. Informacje dotyczące klasyfikacji produktu, opisu regulacji i wymogów GMP można znaleźć za pomocą tego kodu.
- Wybór typu zgłoszenia- Zgłaszający może wybrać jeden z trzech (03) wcześniej wymienionych typów zgłoszeń. Tradycyjne 510(k) jest przeznaczone dla zgłoszeń po raz pierwszy, Specjalne 510(k) jest dla producentów wyrobów medycznych, którzy chcą zgłosić zmiany do istniejącego wyrobu, a skrócone 510(k) można wybrać, gdy wyrób jest zgodny z ustalonymi dobrowolnymi normami konsensusu. W przypadku skróconego 510(k), zgłaszający musi polegać na dokumentach wytycznych FDA.
- Identyfikacja wyrobu referencyjnego- Producent wyrobu medycznego musi udowodnić, że wyrób, który zamierza wprowadzić na rynek, ma takie samo przeznaczenie i cechy techniczne jak wyrób legalnie wprowadzony na rynek, znany również jako wyrób referencyjny. Jeśli istnieją jakiekolwiek różnice w cechach technicznych, zgłaszający musi udowodnić, że różnica ta nie wiąże się z żadnymi obawami dotyczącymi bezpieczeństwa i skuteczności.
Krok 2 – Przygotowanie dokumentacji 510(k)
Następnym krokiem jest przygotowanie pliku 510(k), wytycznych i informacji, które są dostępne na stronie internetowej FDA. Obejmuje to listę kontrolną akceptacji dla wszystkich trzech (03) typów programów 510(k) oraz mikrostronę zatytułowaną Content for 510(k), która zawiera informacje dotyczące oświadczeń o wskazaniach do stosowania, porównania istotnej równoważności i proponowanego etykietowania, a także inne przydatne informacje.
Etapy procesu zgłoszenia 510(k)
Krok 3 – Opłata za przegląd FDA
Wszystkie rodzaje wniosków 510(k) podlegają opłacie użytkownika. W roku finansowym 2023 standardowa opłata za 510(k) wynosi 19 870 USD. Dla firm certyfikowanych w ramach Centrum Diagnostyki i Zdrowia Radiologicznego (CDRH), znanych również jako małe firmy, opłata wynosi 4967 USD. Opłata może ulec zmianie w kolejnym roku finansowym.
Krok 4 – Złożenie wniosku 510(k)
Zgłaszający może przesłać elektroniczną kopię (eCopy) lub zgłoszenie przedrynkowe w formie elektronicznego szablonu i zasobu (eSTAR) za pośrednictwem portalu CDRH.
Od 1 października 2023 roku wszystkie zgłoszenia 510(k), chyba że są zwolnione zgodnie z ostatecznymi wytycznymi, muszą być składane jako zgłoszenia elektroniczne za pomocą eSTAR.
Po złożeniu 510(k) przypisywany jest unikalny numer kontrolny, znany jako „numer 510(k)” lub „numer K”. FDA przeprowadza dwie weryfikacje: jedną, aby sprawdzić, czy uiszczono należną opłatę użytkownika, a drugą, aby zweryfikować, czy dostarczono ważną eKopię lub eSTAR.
- Do 7. dnia FDA wysyła pismo potwierdzające w przypadku uiszczenia odpowiedniej opłaty użytkownika i dostarczenia ważnej kopii elektronicznej (eCopy) lub eSTAR. W przeciwnym razie FDA wysyła pismo o wstrzymaniu z powodu nierozwiązanych kwestii.
- Do 15. dnia, FDA przeprowadza przegląd akceptacyjny. FDA informuje wnioskodawcę, czy wniosek 510(k) został przyjęty do merytorycznego przeglądu, czy też został wstrzymany w ramach odmowy przyjęcia (RTA).
- Do 60. dnia FDA przeprowadza merytoryczny przegląd. FDA komunikuje się poprzez
merytoryczną interakcję, aby poinformować, że FDA albo przejdzie do interaktywnego przeglądu, albo wniosek 510(k) zostanie wstrzymany i zostaną poproszone o dodatkowe informacje.
Krok 5 – Zezwolenie FDA i wpis do bazy danych FDA 510(k)
Celem FDA jest ogłoszenie decyzji w sprawie poprawek do ustawy o opłatach dla użytkowników wyrobów medycznych (MDUFA) w ciągu 90 dni FDA. Dni FDA to dni kalendarzowe między datą otrzymania zgłoszenia 510(k) a datą decyzji MDUFA, z wyłączeniem dni, w których zgłoszenie było wstrzymane z powodu prośby o dodatkowe informacje. Decyzje MDUFA dotyczące zgłoszeń 510(k) obejmują ustalenia dotyczące istotnej równoważności (SE) lub braku istotnej równoważności (NSE).
Po podjęciu decyzji FDA wysyła pismo z decyzją do wnioskodawcy pocztą elektroniczną. Wniosek 510(k), który otrzyma pismo z decyzją SE, jest uznawany za “zatwierdzony.” Następnie jest on umieszczany w bazie danych 510(k) wraz ze wskazaniami do stosowania wyrobu medycznego oraz streszczeniem 510(k) lub oświadczeniem 510(k) jako załącznikami.
Można stwierdzić, że staranne planowanie i wykonanie, poparte dokładną dokumentacją oraz dogłębnym zrozumieniem środowiska regulacyjnego, są kluczowe dla pomyślnego złożenia wniosku 510(k) do FDA.
Aby uzyskać pomoc w procesie składania wniosku 510(k) dla wyrobu medycznego, możesz napisać do nas na adres sales@freyrsoltions.com lub umówić się na rozmowę z naszymi ekspertami, którzy pomogą Ci przejść przez procedury. Bądź na bieżąco. Zachowaj zgodność.









