
A ideia de submissões regulamentares eletrónicas para produtos farmacêuticos precede a própria ferramenta eCTD. No final da década de 1980, iniciativas como a CANDA (Computer-Aided New Drug Application) foram exploradas pela FDA dos US (Food and Drug Administration) e agências europeias. Estes primeiros esforços visavam aumentar a eficiência e o acesso aos dados para os revisores.
A Chegada do Padrão eCTD (2003):
A Conferência Internacional sobre Harmonização (ICH) interveio em 2003 com um marco: a norma eCTD (Documento Técnico Comum eletrónico). Este formato padronizado foi concebido para estabelecer uma linguagem universal para as submissões eletrónicas em todo o mundo.
O Surgimento das Ferramentas eCTD:
Com a adoção do padrão eCTD, a procura por ferramentas eCTD especializadas aumentou significativamente. Estas ferramentas trouxeram vários benefícios importantes:
- Criação de Conteúdo Simplificada: Os utilizadores podiam criar e organizar documentos sem esforço, de acordo com a estrutura eCTD.
- Validação Robusta: As ferramentas eCTD garantiam que as submissões cumpriam as especificações técnicas, evitando atrasos causados por erros de formatação.
- Gestão Eficiente do Ciclo de Vida: Gerir revisões, acompanhar versões e manter a conformidade regulamentar torna-se mais fácil.
Estas inovações revolucionaram o processo de submissão regulamentar, tornando-o mais eficiente e fiável.
Como o Software da Freyr Digital Automatiza a Criação de eCTD
A solução de software avançada da Freyr Digital, Freyr SUBMIT PRO, aborda estes desafios ao automatizar aspetos chave da criação de eCTD, aumentando assim a eficiência e reduzindo o erro humano.
Otimização de Recursos: Ao automatizar tarefas repetitivas, o nosso software liberta recursos humanos valiosos. Os profissionais podem focar-se em atividades mais estratégicas e de alto valor, como análise de dados, desenvolvimento de estratégia regulamentar e envolvimento das partes interessadas. Esta mudança não só aumenta a produtividade, como também reduz os custos operacionais, proporcionando um retorno significativo do investimento.
Risco Minimizado de Erro Humano: A automação minimiza o risco de erro humano ao garantir que os dados são transferidos com precisão e que os documentos são formatados corretamente. As verificações de validação e os mecanismos de deteção de erros incorporados no software melhoram ainda mais a qualidade e a conformidade das submissões regulamentares. Isto reduz a necessidade de retrabalho e ajuda a garantir aprovações atempadas.
Monitorização de Submissões para uma Visão Abrangente das Submissões eCTD
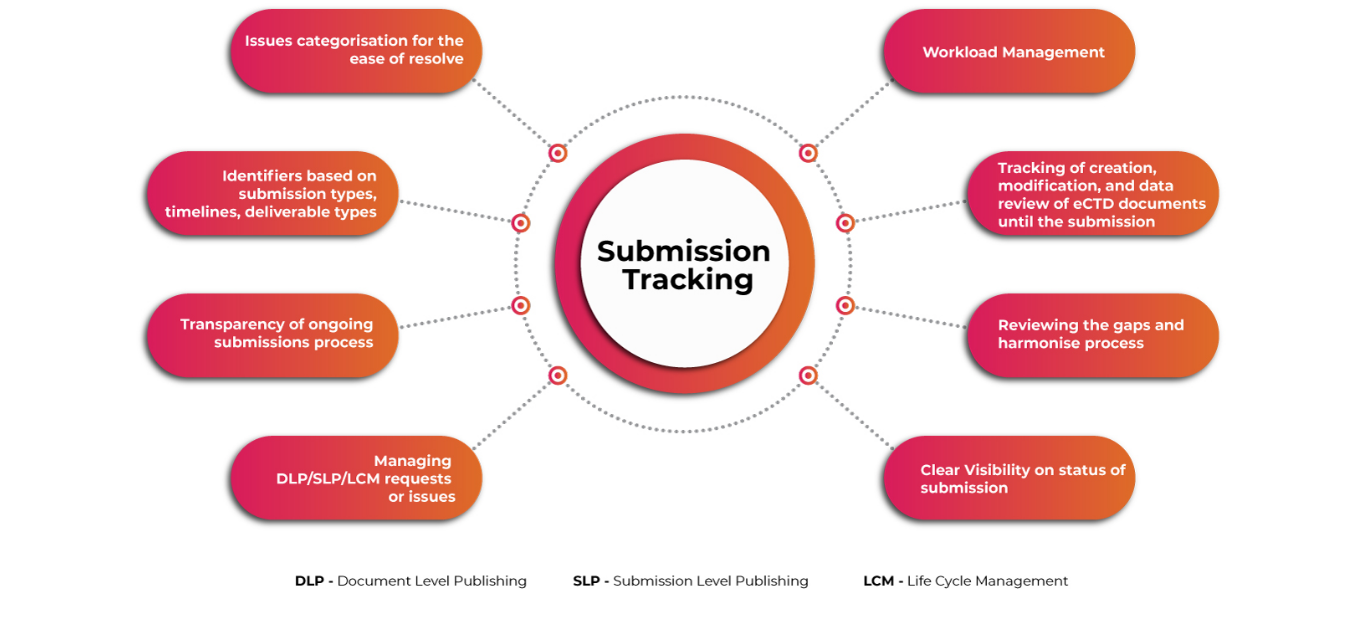
Um sistema automatizado e de fácil utilização para planear e acompanhar atividades complexas de submissão eCTD global, gestão do fluxo de trabalho de atividades, e armazenamento e gestão de submissões regulamentares e informações de submissão é essencial para garantir que os requerentes enfrentem os desafios associados com bastante antecedência. Obter visibilidade das operações de submissão e publicação a um nível granular torna todo o processo de submissões mais suave e rápido.
Acompanhamento de Submissões
A mais recente atualização no eCTD
A transição para o eCTD 4.0 anuncia uma maior eficiência e padronização global no processo de aprovação de medicamentos farmacêuticos. Ao preparar-se para esta transição, a sua empresa pode navegar pela mudança sem problemas e capitalizar as inúmeras oportunidades que esta nova era oferece. Embora a mudança para o eCTD 4.0 possa apresentar desafios, estes são superáveis com dedicação e determinação de todos os países envolvidos. Embora sejam necessários um investimento e um esforço significativos, os benefícios substanciais do eCTD 4.0 tornam o empreendimento verdadeiramente valioso.
Revisão do Processo de Submissão: O eCTD 4.0 promete revolucionar a forma como as empresas farmacêuticas submetem dados de desenvolvimento de medicamentos às autoridades de saúde. O seu objetivo é simplificar o processo de submissão.
Cronograma de Implementação: A FDA planeia aceitar novas submissões no formato eCTD 4.0 a partir de 2024. Fases futuras abordarão as submissões existentes na versão 3.2.2 e a comunicação bidirecional.
Compatibilidade Progressiva: O eCTD 4.0 inclui compatibilidade progressiva, permitindo o ciclo de vida e a reutilização de documentos do conteúdo da v3.2.2. Isto simplifica a conversão de submissões v3.2.2 para eCTD 4.0.
Critérios de Validação: As especificações para os critérios de validação do eCTD 4.0 estão disponíveis. Estes critérios garantem a qualidade e a precisão das submissões.
Conformidade Global: Até 2026, as entidades reguladoras em todo o mundo poderão exigir a conformidade com os padrões eCTD 4.0. Embora atualmente seja voluntário, a aplicação começará entre 2026 e 2029.
O futuro do eCTD:
É essencial adotar a IA e tornar a sua função regulamentar dinâmica, pois isso agrega valor ao seu negócio. A Freya Fusion é uma plataforma de Gestão de Informação Regulamentar (RIM) de ponta, impulsionada por IA e nativa da cloud, que oferece desempenho, segurança e escalabilidade excecionais, tudo isto mantendo uma rigorosa conformidade com as GxP. Aprimorada com funcionalidades avançadas de IA/ML e automação, a Freya Fusion destaca-se no domínio digital, proporcionando uma funcionalidade superior e uma experiência de utilizador excecional. Os avanços da IA da Freyr Digital prometem módulos de Produção e Rastreamento de Submissões, que incluem funcionalidades para compilação, publicação e validação contínuas de submissões regulamentares, garantindo uma conformidade meticulosa com as Diretrizes eCTD. Manter-se à frente no jogo da conformidade regulamentar com SaaS impulsionado por IA certamente beneficiará a sua empresa. Seja com um sistema de alerta precoce para mudanças regulamentares, revisão e análise simplificadas de documentos regulamentares ou análises preditivas para gestão de riscos, a Freyr Digital tem tudo o que precisa. Contacte hello@freyrdigital.com para descobrir as nossas inovações impulsionadas por IA/ML que simplificam as operações regulamentares na indústria médica.
Mantenha-se atualizado com as últimas novidades e avanços tecnológicos. Faça parceria connosco para otimizar as suas operações regulatórias, aumentar a produtividade e elevar a qualidade das submissões. Solicite uma demonstração hoje e experimente a combinação perfeita de experiência e ferramentas. Impulsione a sua organização de boa para excelente. Contacte-nos hoje.









