
Para a maioria Assuntos Regulamentares , a renovação do registo não é apenas mais um marco administrativo. É o momento em que anos de registos de qualidade, dados pós-comercialização e históricos de alterações são analisados sob o escrutínio regulamentar.
No entanto, as renovações são frequentemente abordadas de forma reativa.
Os ficheiros são reunidos à última da hora. Os dados do PMS estão espalhados por diferentes pastas. Os certificados são registados em folhas de cálculo. E, de repente, o que deveria ter sido um processo estruturado transforma-se numa corrida contra o tempo.
As renovações de dispositivos médicos não fracassam por falta de empenho das equipas. Fracassam porque o planeamento da renovação começa demasiado perto da data de validade.
Uma estratégia de renovação sólida muda esta situação. Encaram a renovação como uma atividade contínua do ciclo de vida, e não como um exercício de apresentação de última hora.
Vamos analisar o que isso significa realmente para RA .
Por que é que as renovações de dispositivos médicos requerem uma estratégia
A maioria dos registos de dispositivos tem uma validade de 3 a 5 anos, dependendo do mercado. Algumas regiões adotam renovações anuais, enquanto outras aplicam modelos de manutenção com pagamentos periódicos. Independentemente da estrutura, assim que uma licença expira, o dispositivo não pode ser legalmente fabricado, importado ou distribuído.
Os pedidos de renovação são considerados de alto risco porque as autoridades procedem a uma reavaliação:
- Desempenho pós-comercialização
- Tendências das reclamações e eventos adversos
- Alterações no sistema de fabrico e de qualidade
- Dados clínicos e de segurança
- Histórico de conformidade regulamentar
Em muitas regiões, incluindo a Índia e a UE, as entidades reguladoras exigem dados consolidados do PMS, provas das medidas de correção e prevenção (CAPA) e documentação técnica atualizada como parte do processo de renovação.
É por isso que a renovação deve ser encarada como uma disciplina operacional que se estende por todo o ciclo de vida do produto.
Não como uma tarefa sujeita a prazos.
Comece por um calendário regulatório; a sua primeira linha de defesa
Uma das principais causas de falhas na renovação deve-se a um acompanhamento fragmentado. Mercados diferentes. Prazos diferentes. Requisitos diferentes.
Um calendário regulatório centralizado deve incluir:
- Números de certificados e datas de validade por país
- Períodos de apresentação de pedidos de renovação
- Prazos para o pagamento das taxas de retenção
- Validade da certificação ISO 13485 do certificado CE
- Marcos internos (12 meses, 6 meses, 3 meses antes da renovação)
Do RA prático RA , o planeamento deve começar pelo menos 12 meses antes do termo do prazo.
Atualmente, muitas equipas utilizam plataformas RIMS unificadas para manter uma visão única do estado dos registos em todos os mercados, o que ajuda a evitar a dependência de folhas de cálculo e, ao mesmo tempo, mantém os prazos de renovação visíveis e passíveis de ação.
freya fusion o primeiro da sua categoria a permitir que as organizações disponham de uma única fonte de informação fiável para todos os seus dados relativos à conformidade.
Documentação essencial de que vai sempre precisar
A documentação de renovação segue de perto o modelo do registo inicial, mas com um enfoque adicional na continuidade e no desempenho.
A maioria das autoridades prevê que:
- Carta de apresentação indicando claramente a intenção de renovar
- Declaração de conformidade contínua (fabrico, conceção, propriedade)
- Ficheiro mestre de dispositivos e ficheiro mestre de instalações atualizados (se aplicável)
- ISO 13485 válido
- Certificados CE ou aprovações de garantia de qualidade, quando exigido
- Licenças de fabrico e certificação de BPF
- Declaração de Conformidade
- Histórico de correspondência regulamentar
Quaisquer alterações ocorridas durante o período de validade devem ser comunicadas através dos canais adequados de pós-aprovação. As alterações não comunicadas são uma das formas mais rápidas de suscitar questões por parte das autoridades reguladoras.
É aqui que a gestão estruturada de documentos se revela fundamental. RA beneficiam quando todas as submissões, revisões e aprovações se encontram num único ambiente controlado, em vez de estarem dispersas por unidades de disco e caixas de entrada.
A vigilância pós-comercialização é o cerne da renovação
Se há um aspeto que as entidades reguladoras devem analisar atentamente durante o processo de renovação, esse aspeto é a vigilância pós-comercialização.
As autoridades esperam obter provas de que o dispositivo continuou a funcionar de forma segura e eficaz em condições reais de utilização.
Normalmente, isto inclui:
- Dados de vendas por ano e modelo de dispositivo
- Registos de reclamações e relatórios de eventos adversos
- Análise das causas profundas de cada problema
- Registos CAPA com provas de encerramento
- Histórico de recolhas (global e específico por país)
- Análise de tendências ao longo de todo o período de validade
Os dispositivos de maior risco podem também exigir:
- Relatórios do PMS
- Atualizações do Relatório de Avaliação Clínica
- PMCF
- Relatórios periódicos de atualização de segurança
Os resultados positivos em termos de renovação dependem da consistência com que esses dados são recolhidos ao longo do tempo, e não da qualidade da sua compilação final.
Atualmente, muitas RA integram o acompanhamento do PMS diretamente nos seus fluxos de trabalho regulamentares, utilizando plataformas unificadas como freya fusion, o que permite que as reclamações, as CAPAs e os registos permaneçam interligados, facilitando a rastreabilidade durante a preparação da renovação.
Alinhe o seu sistema de qualidade com a preparação para a renovação
O seu SGQ não é algo distinto da renovação. É a base da renovação.
As entidades reguladoras procuram provas em áreas-chave, tais como:
- Controlo de documentos e histórico de versões
- Gestão da mudança para a produção, rotulagem e embalagem
- Qualificação e auditorias de fornecedores
- Tratamento de reclamações e análise de tendências
- Eficácia do CAPA
- Auditorias internas
- Registos de formação e competências
Uma abordagem prática consiste em realizar uma análise das lacunas antes da renovação, cerca de seis meses antes da apresentação do pedido:
- Verificar se os certificados permanecerão válidos após a revisão
- Confirmar se os dados do PMS estão completos
- Verificar os encerramentos da CAPA
- Consultar os registos de alterações
- Certifique-se de que os registos de formação estão atualizados
Esta auditoria proativa evita frequentemente a necessidade de medidas corretivas de última hora.
Prepare-se antecipadamente para a complexidade de vários mercados
As renovações raramente ocorrem de forma isolada. As carteiras globais envolvem diferentes agentes, distribuidores, organismos notificados e autoridades.
A coordenação inclui normalmente:
- Fabricante que fornece fichas técnicas e dados do sistema de gestão de produtos
- Agentes locais responsáveis pela gestão de pedidos e licenças
- Distribuidores que partilham dados relativos a vendas e reclamações
- Organismos notificados que emitem certificados de auditoria
Sem uma atribuição clara de responsabilidades e prazos definidos, os atrasos multiplicam-se.
Um sistema centralizado que acompanha os requisitos específicos de cada jurisdição, o estado dos pedidos e as comunicações regulamentares pode reduzir significativamente os atritos. É aqui que freya fusion RA , reunindo registos, documentos e a colaboração entre as partes interessadas num único espaço de trabalho regulamentar unificado.
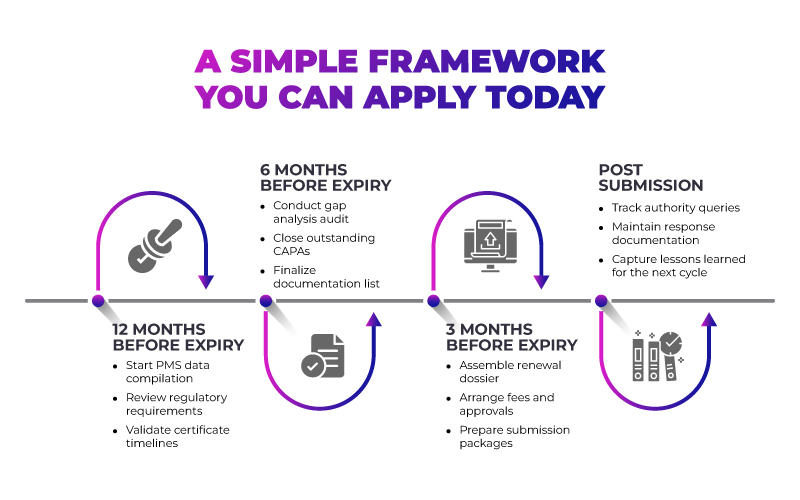
Esta abordagem faseada transforma a renovação num processo previsível, em vez de uma crise recorrente.
A renovação tem a ver com continuidade, não apenas com conformidade
A renovação do registo de dispositivos médicos visa, em última análise, garantir um acesso ininterrupto ao mercado. Quando gerida de forma estratégica, reforça os sistemas de qualidade, melhora a disciplina no âmbito do sistema de monitorização pós-comercialização e promove a confiança nas autoridades reguladoras.
RA já realizam um trabalho árduo todos os dias. O desafio consiste em conferir a esse trabalho estrutura, visibilidade e continuidade.
Aqui, plataformas como freya fusion entram em cena. Ao unificar registos, documentos, PMS e colaboração, ajuda RA a passar de renovações reativas para uma gestão proativa do ciclo de vida regulatório.
Pronto para simplificar as renovações dos seus dispositivos médicos?
Se as renovações ainda parecem fragmentadas, manuais ou stressantes, talvez seja altura de repensar a forma como as suas operações regulatórias estão estruturadas.
Veja como freya fusion, com as suas funcionalidades AI-First, apoia RA de dispositivos médicos com acompanhamento centralizado do registo, controlo de documentos e visibilidade do ciclo de vida, tudo concebido para profissionais da área regulatória, e não para equipas de TI.
Marque uma demonstração hoje mesmo e dê o primeiro passo para renovar a confiança, garantir a conformidade contínua e assegurar uma continuidade de mercado mais tranquila.









