
El etiquetado de los productos farmacéuticos es uno de los aspectos más controlados del cumplimiento normativo. Un error insignificante puede tener consecuencias importantes tanto para la seguridad de los pacientes como para la reputación de una empresa. Tenga en cuenta estos datos:
- El 20 % de Dispositivos Médicos farmacéuticas y Dispositivos Médicos notifican cada mes problemas de control de calidad relacionados con el etiquetado.
- Diversos estudios han demostrado que el 40 % de las etiquetas de los medicamentos en determinados mercados no cumplen los requisitos normativos, y a menudo carecen de información clave sobre seguridad.
- A nivel mundial, entre el 35 % y el 40 % de las retiradas de productos se deben a errores de envasado y etiquetado, según los resúmenes deFDA US
- En las auditorías normativas, más del 50 % de las observaciones se refieren a la documentación relativa al etiquetado, desde la información sobre prescripción hasta artwork las traducciones.
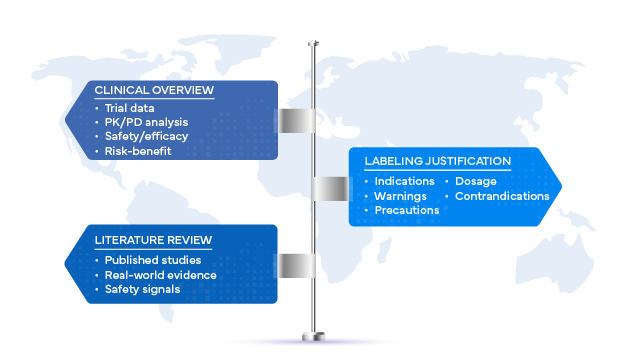
Estas estadísticas ponen de relieve una realidad: las decisiones sobre el etiquetado deben ser precisas, estar basadas en la evidencia y estar plenamente justificadas. La base de esa justificación reside en el resumen clínico y en las revisiones sistemáticas de la literatura.
El papel de la visión general clínica
El resumen clínico, tal y como lo define ICH (R2), es más que una mera formalidad reglamentaria. Se trata de un análisis estructurado y crítico de todos los datos clínicos disponibles que respaldan el desarrollo de un producto. Cuando se vincula al etiquetado, desempeña un papel decisivo a la hora de garantizar que la seguridad, la eficacia y el perfil de riesgo-beneficio queden claramente reflejados en la información de prescripción.
Entre las principales aportaciones del resumen clínico al etiquetado se incluyen:
- Relacionar directamente los resultados de los ensayos clínicos con las afirmaciones sobre el producto
- Justificación de la inclusión de advertencias, precauciones y contraindicaciones
- Garantizar la coherencia entre los resultados en materia de seguridad y las decisiones sobre el etiquetado
- Presentar a las autoridades reguladoras un análisis transparente de la relación beneficio-riesgo, basado en datos empíricos
Por ejemplo, si los datos del ensayo revelan un efecto adverso estadísticamente significativo en un subgrupo, el resumen clínico respalda la justificación para incluir advertencias específicas para ese subgrupo en la ficha técnica.
Por qué son imprescindibles las revisiones bibliográficas
Si bien los datos de los ensayos clínicos constituyen la base para justificar el etiquetado, las revisiones sistemáticas de la literatura amplían la base empírica al incorporar resultados que van más allá de los estudios realizados por los promotores. Estas revisiones sintetizan publicaciones revisadas por pares, datos del mundo real y datos de seguridad posteriores a la comercialización para ofrecer a las autoridades reguladoras una perspectiva más amplia e imparcial.
Una revisión bibliográfica exhaustiva ayuda a las empresas a:
- Verificar las afirmaciones sobre seguridad mediante fuentes independientes
- Detectar señales de alerta temprana o reacciones adversas que no se hayan puesto de manifiesto en los ensayos clínicos
- Resultados comparativos con respecto a productos de la competencia o efectos generales del sector
- Armonizar las fichas técnicas básicas (CCDS) con los documentos de productos locales (LPD) específicos de cada región
Por ejemplo, los estudios publicados o los metaanálisis pueden revelar reacciones adversas poco frecuentes pero graves, lo que refuerza la justificación para incluir o actualizar una precaución en la ficha técnica.
Requisitos normativos para la justificación del etiquetado
Las autoridades sanitarias mundiales, entre ellas laFDA US , EMA, MHRA y PMDA, esperan que las justificaciones de las etiquetas reflejen rigor científico, transparencia y coherencia. Los evaluadores reglamentarios suelen valorar:
- Jerarquía de la evidencia: dar prioridad a los datos de ensayos controlados aleatorios, sin dejar de tener en cuenta los estudios observacionales o de la práctica clínica pertinentes
- Coherencia entre documentos: garantizar que el resumen clínico, el resumen de seguridad clínica (SCS) y la etiqueta propuesta estén en consonancia
- Justificación clara: explicar por qué se incluye (o se excluye) cada indicación, recomendación de dosis o advertencia
Si no se aportan pruebas claras que justifiquen el etiquetado, esto puede dar lugar a consultas por parte de las autoridades reguladoras, a la prolongación de los plazos de revisión o incluso al rechazo de la solicitud.
Buenas prácticas para justificar las decisiones sobre el etiquetado
Las empresas farmacéuticas pueden reforzar sus solicitudes de autorización de etiquetado adoptando estas buenas prácticas:
- Colaboración interdepartamental: involucrar a los equipos clínicos, de seguridad y de asuntos regulatorios para lograr una interpretación integral
- Aprovecha la tecnología: utiliza herramientas basadas en la inteligencia artificial para la revisión bibliográfica con el fin de acelerar la selección y la extracción de información
- Mantener registros documentales: documentar los criterios de inclusión y exclusión de los estudios para cumplir con las auditorías reglamentarias
- Comparación a nivel mundial: alinearse con los productos de la competencia y las directrices en constante evolución para subsanar las deficiencias en materia de cumplimiento
- Actualizar de forma continua: incorporar la bibliografía más reciente y los datos de farmacovigilancia a las estrategias de etiquetado en curso
Conclusión
Dado que el escrutinio regulatorio se encuentra en su punto más alto y el coste del incumplimiento normativo va en aumento, las empresas no pueden permitirse basarse en suposiciones a la hora de redactar las etiquetas de sus productos. Una sólida revisión clínica, combinada con un análisis exhaustivo de la bibliografía, garantiza que cada afirmación esté respaldada por pruebas científicas transparentes.
En Freyr Solutions, ayudamos a las empresas farmacéuticas internacionales a lidiar con esta complejidad. Nuestra end-to-end en etiquetado reglamentario, documentación clínica y estrategias de cumplimiento garantiza que sus decisiones en materia de etiquetado estén científicamente fundamentadas, sean conformes con la normativa y estén armonizadas a nivel mundial.
Asóciese hoy mismo con Freyr para reforzar su estrategia de etiquetado con argumentos basados en datos científicos en los que confían las autoridades reguladoras y de los que dependen los pacientes.










