
La intercambiabilidad con un producto biológico de referencia es un paso crucial en el proceso de aprobación de los biosimilares. Garantiza que un biosimilar pueda sustituir al producto de referencia sin un riesgo significativo de eficacia reducida o mayores preocupaciones de seguridad. Este blog busca comprender la última actualización de la FDA sobre las consideraciones para lograr la intercambiabilidad y las mejores prácticas de la industria para alcanzar la excelencia reglamentaria.
Definición de la intercambiabilidad
Lograr la intercambiabilidad es un proceso complejo y riguroso que requiere cumplir con estrictos requisitos reglamentarios. El desafío radica en demostrar que el biosimilar no solo coincide con el producto de referencia en términos de seguridad y eficacia, sino que también proporciona los mismos resultados clínicos en cualquier paciente. El incumplimiento de estos requisitos puede resultar en retrasos o denegaciones de aprobación, lo que afecta el acceso al mercado y la atención al paciente.
Requisitos reglamentarios para la intercambiabilidad
La FDA describe criterios específicos para demostrar la intercambiabilidad en sus documentos de orientación. Estos criterios incluyen:
- Estudios analíticos comparativos: Se requieren estudios analíticos exhaustivos para demostrar que el biosimilar es muy similar al producto de referencia. Estos estudios evalúan la estructura molecular, la función y la composición del biosimilar.
- Estudios Clínicos: Los estudios clínicos son necesarios para confirmar que el biosimilar no presenta diferencias clínicamente significativas con respecto al producto de referencia en términos de seguridad, pureza y potencia. Esto a menudo implica estudios comparativos de farmacocinética (PK) y farmacodinámica (PD).
- Estudios de intercambio: La FDA exige estudios de intercambio para evaluar el impacto de alternar entre el biosimilar y el producto de referencia. Estos estudios son cruciales para asegurar que el cambio no afecte la eficacia o la seguridad del tratamiento.
- Estrategias de Evaluación y Mitigación de Riesgos (REMS): Si corresponde, las REMS deben abordarse para asegurar que el biosimilar pueda utilizarse de forma intercambiable sin preocupaciones de seguridad adicionales.
Pasos estratégicos para lograr la intercambiabilidad
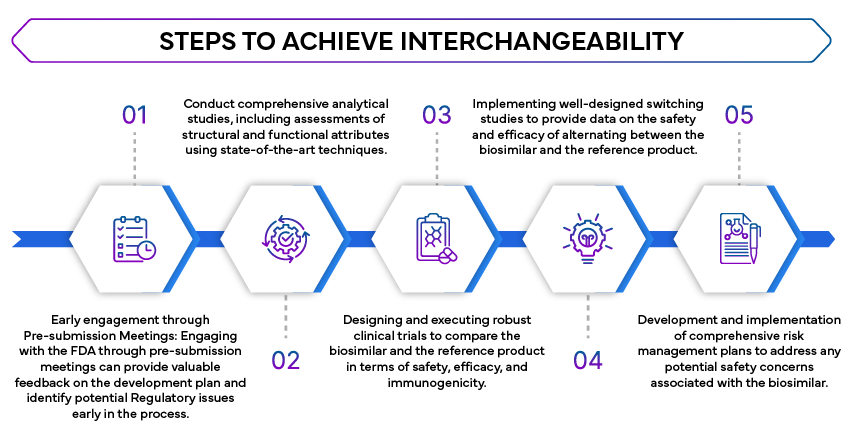
El papel de un socio reglamentario
Las asociaciones reglamentarias pueden mejorar significativamente la probabilidad de lograr la intercambiabilidad. A continuación, se explica cómo un socio reglamentario puede ayudar:
- Orientación experta: Ofrece asesoramiento experto sobre los requisitos normativos y las estrategias para cumplir las directrices de la FDA.
- Soporte de Documentación: Asiste en la preparación de documentos de presentación de alta calidad que cumplen con los estándares reglamentarios.
- Diseño de Estudios Clínicos: Apoya el diseño y la ejecución de estudios clínicos y de cambio sólidos.
- Interacciones con las Autoridades Sanitarias: Facilita una comunicación eficaz con las Autoridades Sanitarias, asegurando una retroalimentación oportuna y constructiva.
- Gestión de Riesgos: Desarrollar estrategias integrales de gestión de riesgos para mitigar posibles problemas de seguridad.
Ventajas de contar con un socio reglamentario
| Ventajas | Descripción | |
| 1. | Experiencia en Requisitos Reglamentarios. | Profundo conocimiento de los panoramas y requisitos reglamentarios globales. |
| 2. | Documentación optimizada | Asegura la preparación de documentación precisa y conforme. |
| 3. | Proceso de presentación eficiente | Reduce el tiempo y el costo mediante una gestión eficiente de las presentaciones. |
| 4. | Mayor cumplimiento | Minimiza el riesgo de retrasos y rechazos mediante un cumplimiento exhaustivo. |
| 5. | Gestión efectiva de riesgos | Identificación proactiva y mitigación de riesgos potenciales. |
Resumen
Lograr la intercambiabilidad con un producto de referencia es un proceso exigente pero esencial para la aprobación exitosa de biosimilares. Requiere una comprensión exhaustiva de los requisitos reglamentarios, una planificación meticulosa y datos clínicos sólidos. Asociarse con un proveedor de servicios reglamentarios experimentado puede aumentar en gran medida las posibilidades de éxito, asegurando que el biosimilar cumpla con los estrictos criterios establecidos por las autoridades reglamentarias. Al aprovechar la orientación experta, la documentación exhaustiva y la gestión estratégica de riesgos, los patrocinadores pueden navegar por el complejo camino hacia la intercambiabilidad de manera más efectiva.










