
En los últimos años, el panorama de los Asuntos Regulatorios ha experimentado una transformación significativa. En el centro de este cambio se encuentra un énfasis creciente en la centralidad en elpaciente, con autoridades sanitarias (HA) de todo el mundo reconociendo el papel inestimable que desempeñan los pacientes en el desarrollo y la aprobación de nuevos productos medicinales. Este cambio no es solo una tendencia; es una reimaginación fundamental de cómo abordamos las presentaciones reglamentarias y, en última instancia, cómo servimos a quienes más importan: los pacientes.
El Problema:
Tradicionalmente, las presentaciones reglamentarias se centraban principalmente en cumplir los requisitos técnicos y científicos, a menudo pasando por alto el impacto directo en las experiencias y resultados de los pacientes. Este enfoque, aunque exhaustivo, a veces no logra captar los matices de las necesidades, preferencias y el uso en el mundo real de los productos medicinales por parte de los pacientes. Como resultado, existía una desconexión entre las aprobaciones reglamentarias y el valor real entregado a los pacientes.
Enfoques Reglamentarios Centrados en el Paciente:
Las autoridades sanitarias, en particular la FDA y la EMA, han logrado avances significativos en la incorporación de las perspectivas de los pacientes en sus marcos reglamentarios.
Este enfoque que prioriza al paciente es evidente en varias áreas clave:
- Desarrollo de medicamentos centrado en el paciente (PFDD):
El programa PFDD de la FDA es una iniciativa pionera que recopila sistemáticamente la opinión de los pacientes para informar el desarrollo de medicamentos y la toma de decisiones reglamentarias. Este programa incluye sesiones de escucha a pacientes, reuniones públicas y el desarrollo de documentos de orientación para mejorar la participación del paciente a lo largo del ciclo de vida del producto. - Evidencia del Mundo Real (RWE):
Existe un reconocimiento creciente del valor de los datos del mundo real para comprender el rendimiento de un producto en diversas poblaciones de pacientes. Las Autoridades Sanitarias están ahora más abiertas a considerar la RWE en las presentaciones reglamentarias, proporcionando una visión más completa de los beneficios y riesgos de un producto. - Resultados Notificados por los Pacientes (PROs):
La inclusión de los PROs en los ensayos clínicos y las presentaciones reglamentarias ha adquirido una importancia creciente. Estas medidas capturan directamente la experiencia del paciente, proporcionando información valiosa sobre los síntomas, la calidad de vida y la satisfacción con el tratamiento. - Compromiso temprano y asesoramiento científico:
Las autoridades sanitarias están animando a los patrocinadores a involucrarse desde el principio en el proceso de desarrollo, a menudo incluyendo a representantes de pacientes en estas discusiones. Este diálogo temprano ayuda a alinear los planes de desarrollo con las necesidades de los pacientes y las expectativas reglamentarias. - Participación del paciente en las evaluaciones de beneficio-riesgo:
Tanto la FDA como la EMA han desarrollado marcos para incorporar las perspectivas de los pacientes en las evaluaciones de beneficio-riesgo, asegurando que las decisiones reglamentarias reflejen lo que más importa a los pacientes.
Tabla: Iniciativas Clave Centradas en el Paciente de las Principales Autoridades Sanitarias
| Autoridad Sanitaria | Iniciativa | Descripción |
|---|---|---|
| FDA | Desarrollo de Medicamentos Centrado en el Paciente (PFDD) | Enfoque sistemático para recopilar la opinión de los pacientes |
| EMA | Grupo de Trabajo de Pacientes y Consumidores (PCWP) | Foro de diálogo con organizaciones de pacientes y consumidores. |
| MHRA | Participación de Pacientes y Ciudadanos | Estrategia para involucrar a los pacientes en los procesos reglamentarios |
| Health Canada | Marco de colaboración para medicamentos y productos sanitarios canadienses | Fomenta la participación del paciente en las actividades reglamentarias |
Papel de los Proveedores de Servicios Reglamentarios:
En este panorama en evolución, el papel de los profesionales y socios de Asuntos Regulatorios se ha vuelto más crucial que nunca. Sirven de puente entre los patrocinadores, las autoridades sanitarias y los pacientes, garantizando que las estrategias reglamentarias se alineen con los enfoques centrados en el paciente.
Las responsabilidades clave incluyen:
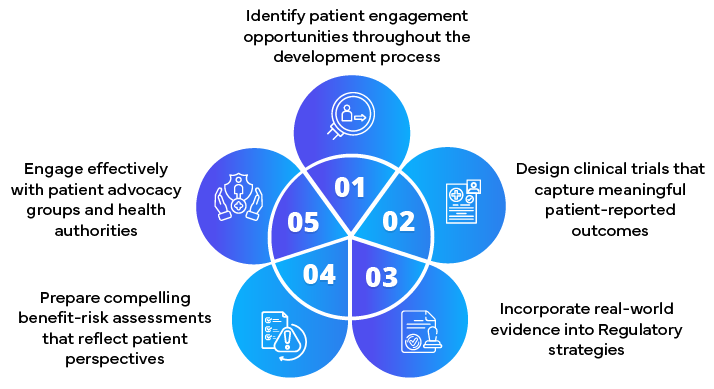
- Desarrollo de estrategias de participación del paciente
- Incorporación de la opinión del paciente en las presentaciones reglamentarias
- Asesoramiento sobre la recopilación y presentación de datos centrados en el paciente
- Facilitando la interacción temprana con las autoridades sanitarias.
- Estar al día con los requisitos reglamentarios en evolución y centrados en el paciente
Papel de los Socios Reglamentarios para lograr presentaciones centradas en el paciente
Resumen:
El cambio hacia la centralidad en el paciente en Asuntos Regulatorios representa una oportunidad significativa para desarrollar y aprobar productos médicos que realmente satisfagan las necesidades de los pacientes. Al adoptar este enfoque, los patrocinadores no solo pueden navegar por las vías reglamentarias de manera más efectiva, sino también entregar productos que marquen una diferencia significativa en la vida de los pacientes. A medida que las autoridades sanitarias continúan perfeccionando sus enfoques centrados en el paciente, la experiencia de los proveedores de servicios reglamentarios o socios se vuelve invaluable para garantizar que las presentaciones no solo cumplan con los requisitos técnicos, sino que también resuenen con las experiencias y prioridades de los pacientes.
En esta nueva era de los Asuntos Regulatorios, priorizar a los pacientes no es solo una buena práctica, es la clave del éxito.









